Clear Sky Science · nl
Astma-gemedieerde controle van de groei van optische gliomen via T-cel–microglia-interacties: Een wiskundig model
Wanneer ademhalingsproblemen verbinden met hersentumoren
Astma en hersentumoren lijken mijlenver uit elkaar te liggen: het ene beïnvloedt hoe we ademen, het andere hoe we zien, denken en bewegen. Toch hebben artsen een raadselachtig patroon opgemerkt — kinderen met astma blijken minder vaak bepaalde tumoren van de oogzenuw te ontwikkelen. Dit artikel onderzoekt hoe een chronische longaandoening onverwacht de hersenen zou kunnen beschermen, met behulp van een wiskundig model om de verborgen chemische gesprekken tussen immuuncellen en tumorcellen te volgen.
Een traag groeiende tumor met grote gevolgen
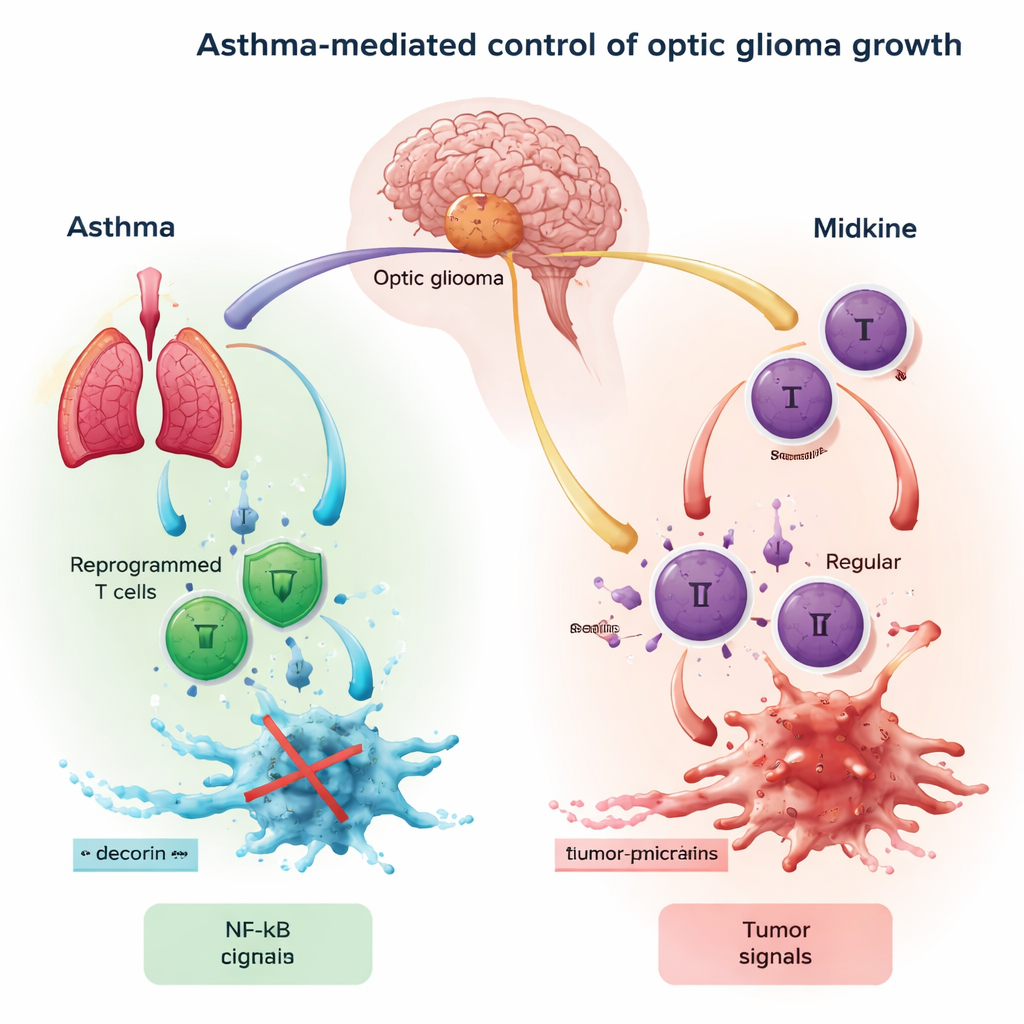
Optische gliomen zijn over het algemeen traag groeiende tumoren die zich vormen langs de oogzenuw, meestal bij kinderen met een genetische aandoening genaamd neurofibromatose type 1 (NF1). Hoewel deze tumoren als “laaggradig” worden beschouwd, kunnen ze toch gezichtsverlies en hormonale problemen veroorzaken. Bij NF1 zorgt een defect gen ervoor dat een signaalproteïne genaamd RAS overactief wordt. Die overactiviteit zet de productie van een andere molecule, midkine, aan, die als een luidspreker in de oogzenuw functioneert, immuuncellen aantrekt en de lokale omgeving op manieren verandert die meestal het tumorvoordeel dienen in plaats van het bestrijden.
Een tumor voedend gesprek tussen zenuw- en immuuncellen
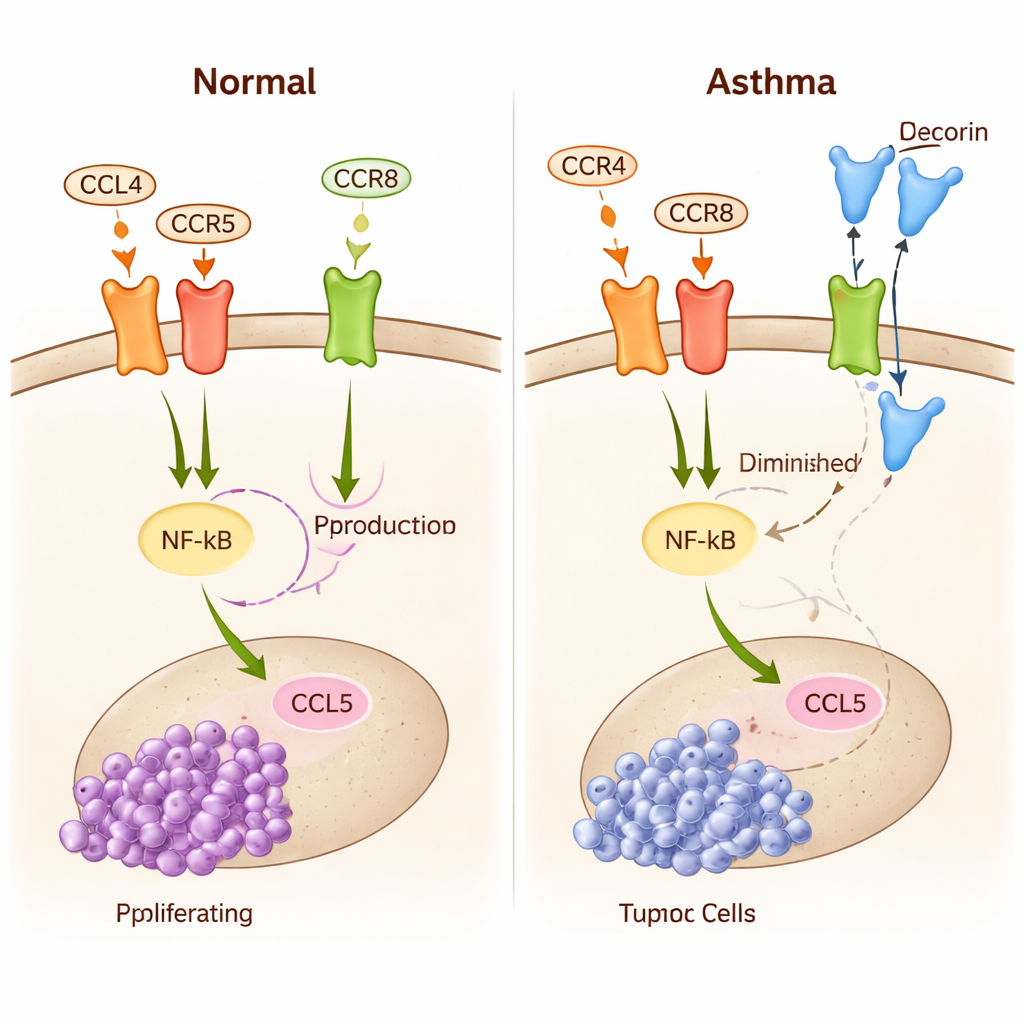
De auteurs richten zich op een keten van gebeurtenissen die de oogzenuw, immuuncellen en tumorgroei verbindt. Midkine van de oogzenuw activeert eerst T-cellen, een type witte bloedcel, en zet hen aan tot het vrijgeven van een signaal genaamd CCL4. Dat signaal bindt vervolgens aan receptoren (CCR5 en CCR8) op microglia, de residentiële immuuncellen van de hersenen. Wanneer voldoende CCL4 zich aan deze receptoren hecht, schakelt het een hoofdschakelaar binnen microglia in, bekend als NF-κB. Eenmaal geactiveerd, stimuleert NF-κB de productie van een ander signaal, CCL5, dat optische glioma-cellen aanmoedigt om te groeien, te migreren en immuunaanvallen te omzeilen. In wezen vormt de midkine–CCL4–NF-κB–CCL5-as een cirkelvormig “ga”-signaal voor tumorexpansie.
Hoe astma T-cellen herprogrammeert tot tumorremmers
Astma staat vooral bekend als een ziekte van chronische luchtwegontsteking. Maar bij mensen met astma raken sommige T-cellen “herprogrammeerd” naar een andere staat: ze verliezen veel van hun directe cel-dodende capaciteit en scheiden in plaats daarvan moleculen uit die hun omgeving hervormen. Een van deze moleculen is decorine, een klein eiwit met erkende antitumoreigenschappen. Het kernidee in dit werk is dat astma-geprimede T-cellen vanuit de long naar de hersenen kunnen reizen en decorine loslaten in de nabijheid van het optische glioom. Decorine concurreert met CCL4 voor de CCR8-receptor op microglia, blokkeert daarmee effectief een deel van het tumorvoedende gesprek en schakelt NF-κB en CCL5 in de immuuncellen van de hersenen omlaag.
Wiskunde gebruiken om een onzichtbaar netwerk te volgen
Omdat dit signaalweb te complex is om alleen uit intuïtie te doorgronden, bouwden de onderzoekers een gedetailleerd wiskundig model met behulp van differentiaalvergelijkingen. Het model volgt de niveaus van sleutelmoleculen (midkine, CCL4, decorine, NF-κB, CCL5), de activiteit van receptoren op microglia en de groei van tumorcellen in de loop van de tijd. Ze gebruikten experimentele gegevens om te kalibreren hoe sterk elke interactie plaatsvindt en simuleerden vervolgens veel scenario’s. Het model toont hoe kleine veranderingen in bindingssterkte — hoe gemakkelijk CCL4 of decorine zich aan hun receptoren hechten — de microglia tussen twee modi kunnen schakelen: een tumorbevorderende staat met hoge NF-κB en CCL5, en een tumorsuppressieve staat met sterke decorinebinding en zwakke CCL4-signalen. Een eenvoudige index op basis van de verhouding van decorine-gebonden tot CCL4-gebonden receptoren voorspelt nauwkeurig of de tumor de neiging heeft te groeien of juist te stagneren.
Slimmere immuun-gebaseerde behandelingen ontwerpen
Buiten het verklaren waarom astma mogelijk beschermt tegen optische gliomen, wordt het model gebruikt om behandelstrategieën te verkennen. Het suggereert dat therapieën die decorineniveaus verhogen of de greep van CCL4 op zijn receptoren verzwakken de tumorgroei kunnen vertragen. De auteurs testen digitaal benaderingen zoals herhaaldelijk infunderen van decorine-producerende T-cellen of het gebruik van de immuunsignaalstof IL-2 om deze gunstige cellen in het lichaam uit te breiden. Interessant genoeg laten de simulaties zien dat niet alleen de totale dosis, maar ook de timing van dergelijke behandelingen ertoe doet: matige, goed gespreide toedieningen kunnen microglia in de tumorsuppressieve staat houden even effectief als grotere, minder frequente doses, met mogelijk minder bijwerkingen.
Wat dit betekent voor patiënten en gezinnen
Voor niet-specialisten is de kernboodschap dat de chronische ontsteking bij astma, normaal gesproken gezien als schadelijk, soms het immuunsysteem zodanig kan hervormen dat het bepaalde hersentumoren tegengaat. Door T-cellen te veranderen in fabriekjes voor decorine lijkt astma het evenwicht in de oogzenuw te verschuiven van een groeivriendelijke omgeving naar een vijandigere omgeving voor kanker. Hoewel niemand astma als therapie voorstelt, zouden de hier blootgelegde mechanismen nieuwe behandelingen kunnen inspireren die de beschermende aspecten nabootsen — met op maat gemaakte T-celtherapieën of medicijnen die de blokkerende werking van decorine imiteren — om kinderen met risico op optisch glioom te beschermen.
Bronvermelding: Lee, D., Lawler, S. & Kim, Y. Asthma-mediated control of optic glioma growth via T cell-microglia interactions: A mathematical model. npj Syst Biol Appl 12, 26 (2026). https://doi.org/10.1038/s41540-026-00647-w
Trefwoorden: optisch glioom, astma, decorine, T-cellen, wiskundige modellering