Clear Sky Science · nl
Optimale controletheorie als methode voor het ontwerpen van adaptieve multidrug‑therapieën
Waarom het temmen van kanker, niet het uitroeien, soms beter werkt
Behandeling van kanker streeft meestal naar het zo snel mogelijk doden van zoveel mogelijk tumorcellen. Toch kan deze agressieve aanpak averechts werken: ze vernietigt vaak de drugsensitieve cellen en maakt onbedoeld ruimte vrij voor drugresistente cellen om te domineren. Dit artikel verkent een tegenintuïtief idee — met behulp van wiskunde en twee kankermedicijnen samen de gevoelige en resistente cellen in concurrentie houden, zodat de tumor veel langer beheersbaar blijft.
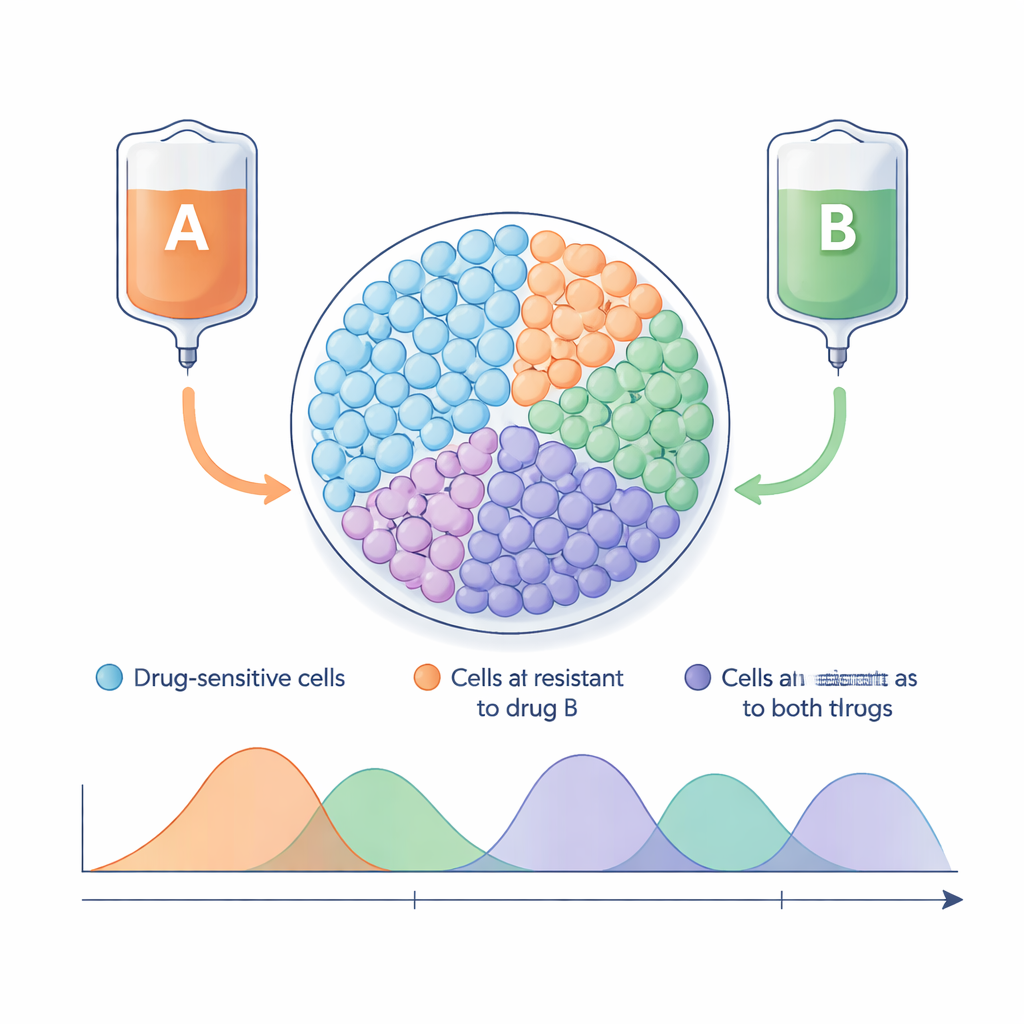
Het heroverwegen van hoe tumoren zich onder behandeling ontwikkelen
Tumoren zijn geen homogene massa’s van identieke cellen. Ze zijn gemengde gemeenschappen met cellen die gemakkelijk door behandeling worden gedood en anderen die al resistent zijn tegen één of meerdere middelen. Standaard chemotherapieschema’s richten zich op maximale celdoding en houden zelden rekening met hoe deze diversiteit de tumor laat evolueren onder medicatiedruk. Wanneer een krachtige behandeling de gevoelige cellen wegneemt, kunnen resistente exemplaren vrijwel ongestoord groeien, wat leidt tot terugval. Adaptieve therapie keert deze logica om: in plaats van volledige uitroeiing na te streven, probeert ze een stabiele populatie gevoelige cellen in leven te houden zodat die resistente concurrenten kunnen verdringen en de totale tumor op een voor de patiënt aanvaardbare grootte houden.
Wiskunde gebruiken om slimmere multidrug‑schema’s te ontwerpen
De onderzoekers bouwden een wiskundig model van een tumor die uit vier celtypen bestaat: cellen die gevoelig zijn voor beide middelen, cellen die alleen tegen middel A resistent zijn, cellen die alleen tegen middel B resistent zijn, en cellen die tegen beide resistent zijn. Het model gaat ervan uit dat deze cellen beperkte ruimte en hulpbronnen delen, zodat hun groei vertraagt naarmate de totale tumor een maximumgrootte nadert. Daarnaast kunnen de twee medicijnen in de loop van de tijd worden op- of afgeschakeld. Het team paste vervolgens optimale controletheorie toe, een tak van de wiskunde die wordt gebruikt om de beste manier te vinden om dynamische systemen te sturen, om een klinische vraag te beantwoorden: hoe moeten we de doseringen van de twee middelen in de tijd variëren om de tumor zo lang mogelijk onder een gekozen groottegrens te houden?
Cellen competitie laten voeren is beter dan maximale doses toedienen
De analyse toonde algemene regels voor het gebruik van de medicijnen. Wanneer de tumor dicht bij de toegestane groottegrens werd gehouden, concurreerden gevoelige en deels resistente cellen sterk met de volledig resistente cellen, waardoor hun uitbreiding vertraagde. De meest succesvolle regimes, genoemd competition maintenance (CM)-schema’s, moduleerden de doseringen opzettelijk zodat de totale tumorgrootte rond deze drempel bleef schommelen. Soms werden beide middelen in een vaste verhouding samen gebruikt en geleidelijk verhoogd; andere keren werd eerst adaptief één middel gegeven en later het tweede toegevoegd. Daarentegen presteerden regimes die zwaar leunden op het continu toedienen van één of beide middelen op maximale toegestane dosis meestal slechter, omdat ze te veel concurrentie wegnamen en uiteindelijk door volledig resistente cellen werden overgenomen.
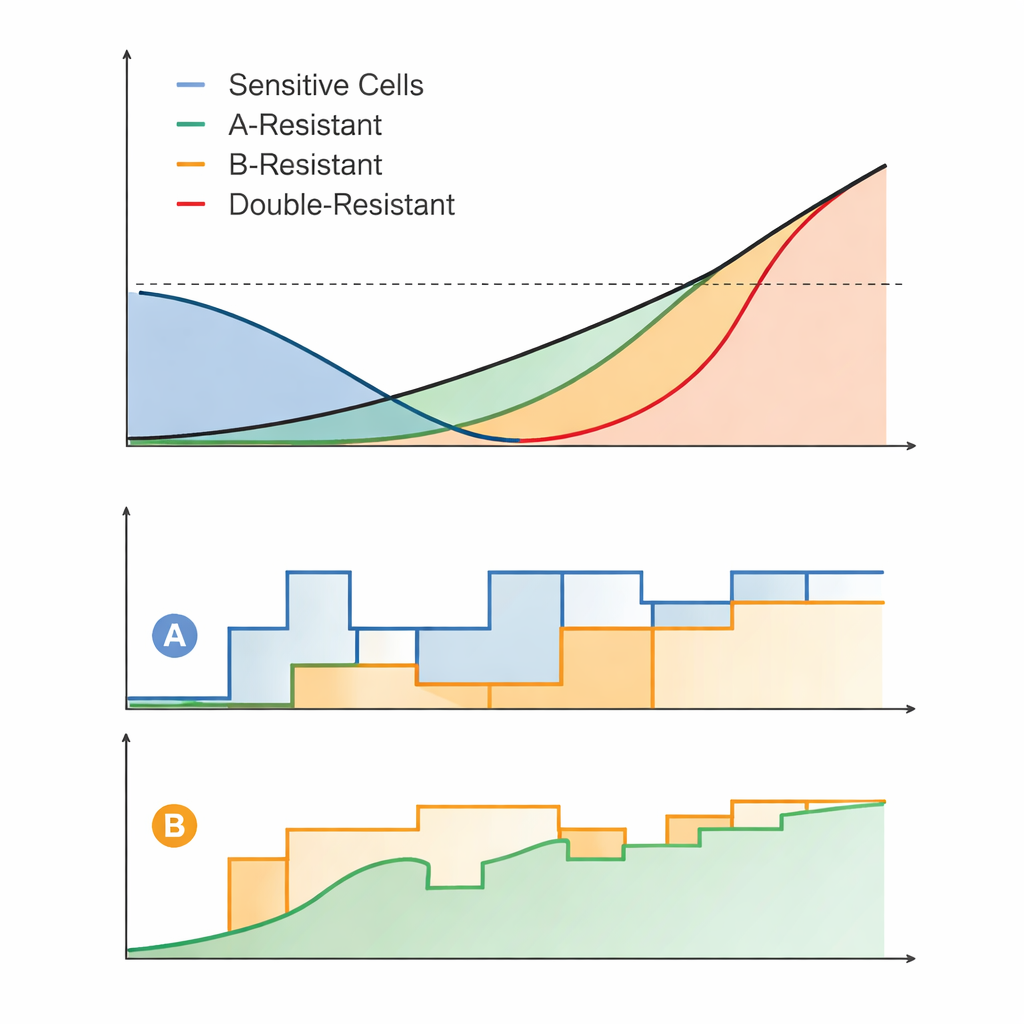
Van ideale wiskunde naar praktische behandelplannen
Het voortdurend perfect bijstellen van doseringen is onrealistisch in de kliniek of zelfs in labo‑experimenten, dus de auteurs ontwikkelden "praktische" versies van hun CM‑regimes. In deze vereenvoudigde schema’s werden de geneesmiddeldoseringen slechts eenmaal per dag en in grove stappen aangepast. Zelfs met deze beperkingen hielden de praktische adaptieve regimes de tumor meestal veel langer onder controle dan strategieën die op de huidige standaard leken, zoals het constant toedienen van beide middelen op hoge dosis of het overschakelen van het ene volle dosis‑middel naar het andere pas nadat de tumor hergroeide. Het voordeel van op competitie gebaseerde strategieën was vooral duidelijk wanneer de toegestane tumorgrootte‑drempel en de maximale medicatiedoses niet extreem laag waren, omstandigheden waaronder het mogelijk is om sterke competitie in stand te houden.
Wat dit betekent voor toekomstige kankerzorg
In het algemeen laat de studie zien dat, in een situatie waarin geneesmiddelresistentie al aanwezig is, de sleutel tot het verlengen van controle niet zozeer zit in hoe slim we tumorcellen doden, maar in hoe goed we competitie tussen gevoelige en resistente cellen behouden bij een beheersbare tumoromvang. Optimale controletheorie bood een systematische manier om veel mogelijke tweemiddelregimes te verkleinen en te vergelijken, waarbij robuuste patronen werden benadrukt in plaats van één kwetsbaar “perfect” schema. Hoewel het werk is gebaseerd op een vereenvoudigd labo‑model en experimenteel testen vereist, ondersteunt het een groeiende zienswijze: voor sommige gevorderde vormen van kanker kan de beste strategie zijn de ziekte te beheren als een chronisch, evoluerend ecosysteem in plaats van te proberen haar koste wat het kost te vernietigen.
Bronvermelding: Widdershins, A., Hansen, E., Read, A. et al. Optimal control theory as a method for designing multidrug adaptive therapy regimens. npj Syst Biol Appl 12, 27 (2026). https://doi.org/10.1038/s41540-025-00613-y
Trefwoorden: adaptieve therapie, drugresistentie, optimale controle, kankerevolutie, multidrug‑regimes