Clear Sky Science · nl
Polysachariden en de colon-slijmbarrière: een overzicht van biofysische interacties en functionele effecten
Waarom de gladde bekleding van de darm ertoe doet
Diep in je dikke darm ligt een slijmerige, onzichtbare schild: een slijmlaag die biljoenen microben op afstand houdt van je eigen cellen. Dit overzichtsartikel onderzoekt hoe complexe suikers, polysachariden genoemd—uit voedsel, zeewieren, schimmels en medische producten—interageren met die slijmbarrière. Inzicht in deze wisselwerking tussen dieet en slijm helpt verklaren waarom bepaalde vezels goed zijn voor de darmgezondheid, hoe sommige behandelingen kunnen beschermen tegen colitis en andere darmaandoeningen, en hoe slimmere afleveringssystemen voor geneesmiddelen op den duur medicijnen precies daar kunnen afleveren waar ze het meest nodig zijn.
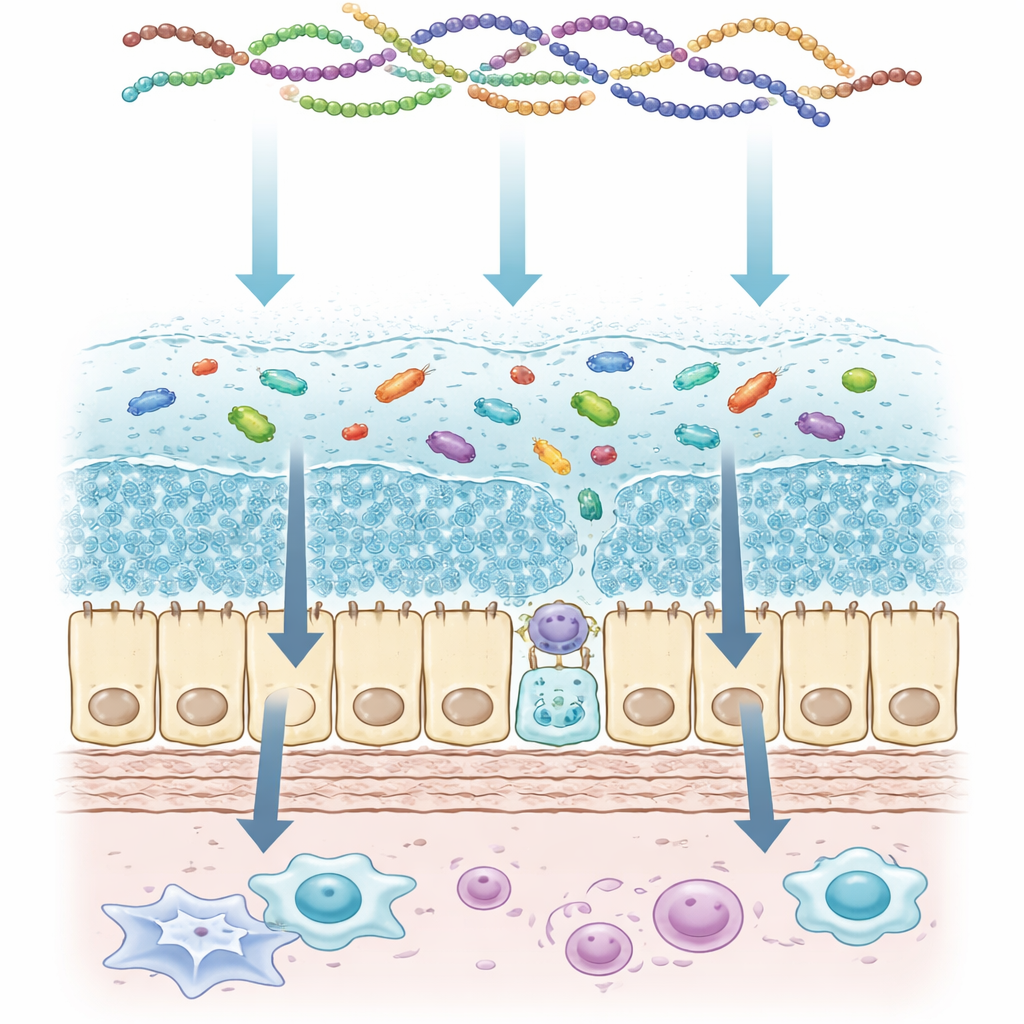
De twee lagen veiligheidsdeken van de colon
De auteurs beginnen met het beschrijven van de architectuur van het colon-slijm als een tweelaagse structuur. Het dichtst bij de darmwand ligt een dichte binnenlaag die nesten met bacteriën vrijwel voorkomt en fungeert als een strakke schild. Daarboven bevindt zich een lossere buitenlaag die dienstdoet als een gecontroleerd habitat voor vriendelijke microben. Gespecialiseerde cellen, gobletcellen genoemd, produceren en scheiden continu grote slijmmoleculen uit, die snel ontvouwen en gel vormen zodra ze het darmslijmoppervlak bereiken. Deze gelvormende moleculen zijn rijkelijk voorzien van suikertakjes, die het slijm zijn dikte, waterbindend vermogen en negatieve lading geven. Wanneer deze structuur afbreekt—door ontsteking, infectie of genetische defecten—komen bacteriën dichter bij de wand, slaan immuunalarmen aan en kunnen chronische darmaandoeningen ontstaan.
Verschillende suikers, verschillende manieren van hechten
Polysachariden zijn lange ketens van eenvoudige suikers, maar hun gedrag in slijm hangt af van details zoals grootte, vertakking en elektrische lading. Neutrale ketens zoals resistente zetmelen en inuline weven zich voornamelijk door waterstofbruggen en fysieke verstrengeling in het slijmnetwerk. Negatief geladen ketens uit pectines, alginaten en zeewiergommen kunnen zwak associëren met of juist worden afgestoten door het al negatieve slijm, afhankelijk van lokale ionen en het fijne ladingspatroon van beide partners. Positief geladen ketens, vooral chitosan uit schaaldieren en schimmels, worden sterk aangetrokken tot slijm en kunnen er dichte complexen mee vormen. De review legt uit dat deze interacties niet door één enkele kracht worden beheerst, maar door een mix van elektrostatieve aantrekking, waterstofbinding, hydrofobe contacten en subtiele van der Waals-krachten die samen bepalen hoe diep een polysacharide in de gel binnendringt en hoe stevig het hecht.
Model-darmwanden op chips, schotels en plakjes
Om deze complexe interacties te ontrafelen, gebruiken onderzoekers een gereedschapskist aan experimentele modellen. Vlakke celkweken kunnen worden verrijkt met slijmproducerende cellen om te onderzoeken hoe specifieke polysachariden de slijmproductie, dikte of doorlaatbaarheid veranderen. Drie-dimensionale organoïden, gekweekt uit stamcellen, bouwen miniatuur darmbuisjes die hun eigen slijm afscheiden, terwijl microfluïdische “gut-on-a-chip”-platforms realistische stroming, rek en levende bacteriën toevoegen. Ex vivo-opstellingen houden vers geïsoleerd darmweefsel gedurende korte periodes in leven en behouden natuurlijke slijmlagen en immuuncellen. Elk model heeft afwegingen: eenvoudige schotels zijn gemakkelijk maar kunstmatig, chips en organoïden zijn realistischer maar technisch veeleisend. Door resultaten over deze systemen heen te vergelijken, kunnen wetenschappers directe fysieke effecten van polysachariden op slijm onderscheiden van indirecte effecten die worden voortgestuwd door microben en het immuunsysteem.
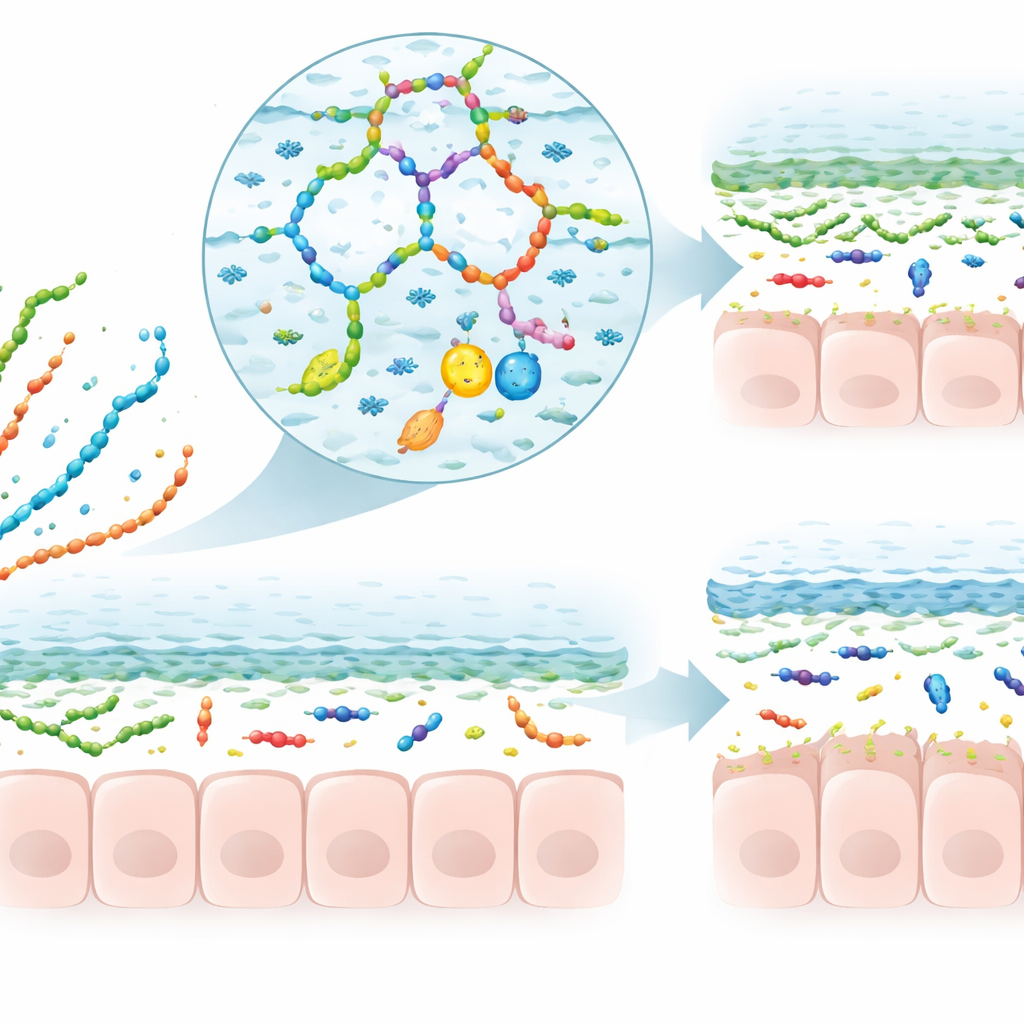
Vormgeven van slijm, microben en de immuunrespons
De review bekijkt vervolgens wat functioneel gebeurt wanneer polysachariden slijm ontmoeten. Sommige positief geladen ketens kunnen de gel tijdelijk losser maken of reorganiseren, wat beïnvloedt hoe gemakkelijk deeltjes en geneesmiddelen erdoorheen bewegen. Andere vormen gemengde netwerken met slijm die de laag verdikken of stabiliseren. Veel dieetpolysachariden worden niet door ons verteerd maar door darmbacteriën gefermenteerd, die ze omzetten in korte-keten vetzuren en andere kleine moleculen. Deze fermentatieproducten signaleren aan gobletcellen om meer slijm te maken, sturen de suikerversieringen op het slijm bij en ondersteunen een microbiegemeenschap die de neiging heeft veilig in de buitenste laag te blijven. In diermodellen van colitis verhogen bepaalde plantaardige en paddenstoelenpolysachariden het aantal gobletcellen, herstellen ze de slijmdikte en houden ze bacteriën verder van de darmwand, vaak gepaard met minder ontsteking en oxidatieve stress.
Voedsel en therapieën ontwerpen die met slijm samenwerken
Tot slot stellen de auteurs dat polysachariden doelbewust ontworpen of geselecteerd kunnen worden om de slijmbarrière te ondersteunen in plaats van die per ongeluk te beschadigen. Door specifieke structurele eigenschappen—zoals lading en moleculair gewicht—te koppelen aan meetbare uitkomsten zoals slijmdikte, viscositeit en penetratievermogen, doen zij aanbevelingen voor het kiezen van polysachariden die de barrière versterken, geneesmiddelen effectiever naar de colon vervoeren of de microbiota zacht sturen richting gezondheidbevorderende activiteiten. Voor niet-specialisten is de kernboodschap dat de slijmlaag die de colon bekleedt niet gewoon passief slijm is; het is een actief grensvlak waar de chemie van ons dieet, onze gastmicroben en onze immuunverdediging elkaar ontmoeten. Doordacht ontworpen polysachariden zouden belangrijke instrumenten kunnen worden om dat grensvlak intact te houden en onze darmen in balans.
Bronvermelding: Cheong, KL., Biney, E., Wang, M. et al. Polysaccharides and the colon mucus barrier: a review of biophysical interactions and functional impacts. npj Sci Food 10, 98 (2026). https://doi.org/10.1038/s41538-026-00750-6
Trefwoorden: colon-slijmbarrière, dieetpolysachariden, darmmicrobiota, mucoadhesieve geneesmiddellevering, inflammatoire darmaandoening