Clear Sky Science · nl
Extracellulaire vesicles uit gekookt vlees ssc-miR-1 veroorzaken stofwisselingsstoornissen in de muizenlever via het PI3k/AKT-pad
Waarom de inhoud van gekookt vlees ertoe kan doen
Veel mensen maken zich zorgen of veel rood vlees eten slechter is voor de gezondheid dan wit vlees zoals kip. Deze studie kijkt voorbij vet en cholesterol naar een nieuwere verdachte: piepkleine pakketjes die vrijkomen uit gekookt vlees, zogenaamde extracellulaire vesicles. Deze microscopische blaasjes dragen genetische "boodschappen" die ons lichaam kan opnemen. De onderzoekers vroegen zich af of vesicles uit gekookt varkens- en kippenvlees de lever kunnen aanzetten tot gewichtstoename, vetophoping en slechte glucoseregulatie. Hun resultaten suggereren dat een deel van de risico’s van rood vlees mogelijk voortkomt uit deze verborgen lading, en niet alleen uit voedingsstoffen. 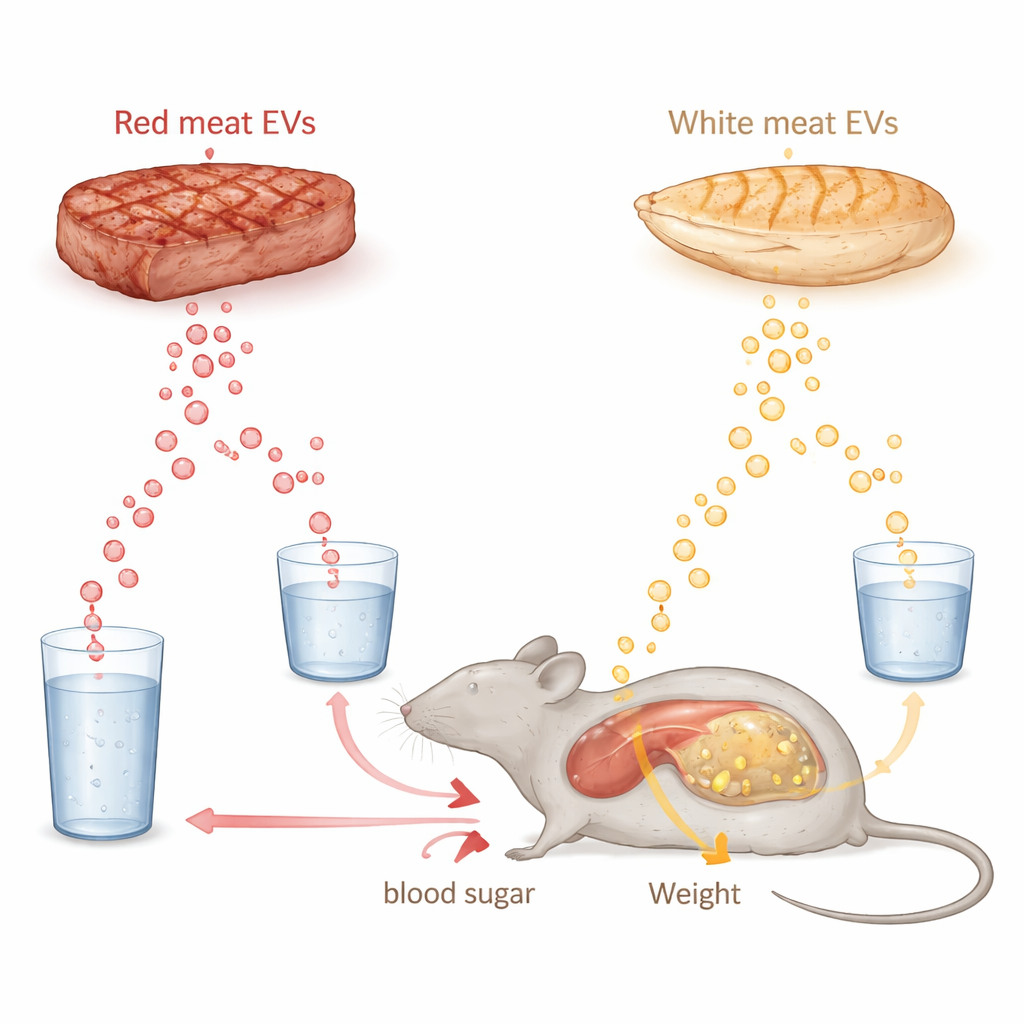
Kleine blaasjes van ons avondeten
Wanneer dierlijke cellen afbreken of communiceren, stoten ze nanoschaal zakjes af die uit vet- en proteïnemembranen bestaan, bekend als extracellulaire vesicles. Het team toonde aan dat zulke vesicles het gebruikelijke koken van varkens- en kippenvlees overleven en geïsoleerd kunnen worden uit het kookwater. Deze blaasjes, ongeveer honderd miljardsten van een meter groot, bevatten nog steeds moleculaire inhoud zoals microRNA’s — korte stukjes genetisch materiaal die genen omhoog of omlaag kunnen bijstellen. Vesicles afkomstig van varken waren gemiddeld iets groter dan die van kip en bevatten veel van een specifiek microRNA genaamd ssc-miR-1, terwijl kipvesicles rijker waren aan een verwant microRNA genaamd gga-miR-133a-3p.
Muisjes water geven met vesicles in plaats van vlees
Om te begrijpen hoe deze vesicles de gezondheid van het gehele organisme kunnen beïnvloeden, voegden de wetenschappers ze tien weken lang toe aan het drinkwater van muizen, zonder het standaardvoer te veranderen. Vergeleken met controlemuizen die alleen zoutoplossing kregen, kregen zowel muizen die red-meat vesicles dronken als muizen die white-meat vesicles dronken meer gewicht en een hogere body-mass index. De groep met rood vlees toonde de grootste veranderingen: ze renden minder op bewegingswielen, verwerkten een suikerbelasting slecht en reageerden traag op insuline. Bij onderzoek van de lever vonden de onderzoekers extra vetdruppels, vooral bij muizen die blootgesteld waren aan vesicles uit rood vlees, wat wijst op een vroeg stadium van vetslever en verstoorde stofwisseling.
Boodschappen die levergenen verstoren
In de lever maten de onderzoekers welke genen aan- of uitgezet waren na langdurige blootstelling aan de vesicles. Honderden genen wijzigden hun activiteit, waaronder veel die betrokken zijn bij hoe cellen brandstof verbranden, vetten verwerken en op insuline reageren. Vooral vesicles uit rood vlees duwden genpatronen in de richting van atherosclerose, niet-alcoholische vette leverziekte en andere metabole problemen. High-throughput sequencing toonde dat het meest aanwezige microRNA in rood-vlees vesicles, miR-1, goed gepositioneerd is om deze routes te beïnvloeden. Computerpredicties en laboratoriumtests gaven aan dat miR-1 zich kan hechten aan de instructies voor sleutelproteïnen in groeiregulatie en suikerverwerking, waaronder een groeifactor (IGF1) en een signaalproteïne genaamd PI3K.
In levercellen: hoe suikerverwerking verstoord raakt
Om het mechanisme verder te onderzoeken, gingen de onderzoekers over op een kweeklijn van muislevercellen in petrischalen. Ze toonden aan dat cellen gemakkelijk vesicles uit rood vlees opnamen en dat extra miR-1 de celgroei vertraagde door IGF1-niveaus te verlagen. Belangrijker voor de stofwisseling bleek dat miR-1 direct PI3K blokkeert, een centrale schakel in het insulinesignaleringspad. Toen het team een insulineresistente celmodel creëerde, maakte toevoeging van miR-1 de situatie erger: de cellen namen minder suiker op, slaagden minder glycogeen op en lieten zwakkere activiteit zien van PI3K, zijn partner AKT, en GLUT4, de poort die glucose in cellen brengt. Een chemische stof die PI3K opnieuw activeert kon deze effecten deels ongedaan maken, wat het idee ondersteunt dat miR-1 uit vesicles van rood vlees dit pad saboteert. 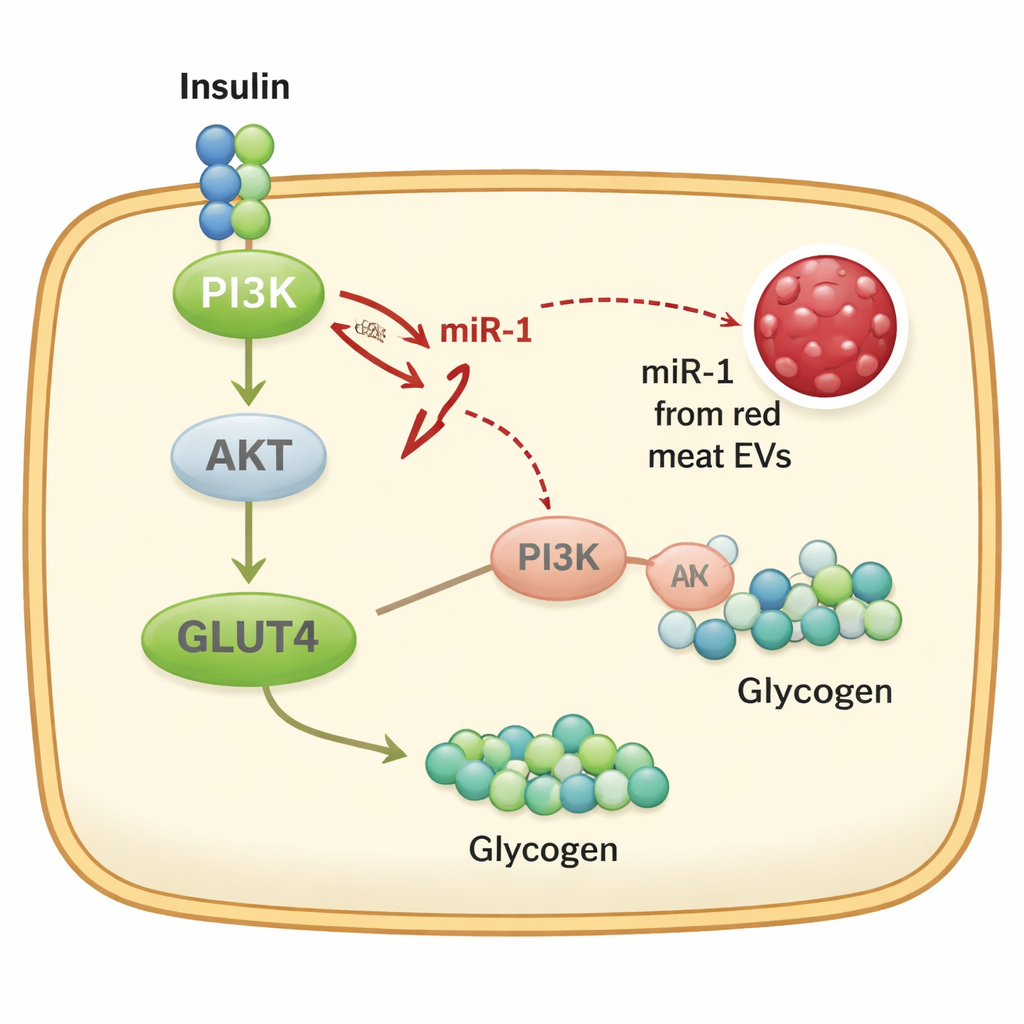
Wat dit betekent voor dagelijks eten
Voor niet-specialisten is de kernboodschap dat gekookt vlees de stofwisseling kan beïnvloeden niet alleen via vet, eiwit en ijzer, maar ook via microscopische informatiefpakketjes die het koken overleven en door het lichaam worden opgenomen. Bij muizen bevorderden vesicles uit zowel varken als kip gewichtstoename en tekenen van insulineresistentie, waarbij vesicles uit varken sterkere effecten hadden. Een enkel microRNA gedragen door vesicles uit rood vlees was voldoende om de suikerverwerking in levercellen te verslechteren door een belangrijk insulinesignaal te dempen. Hoewel meer onderzoek nodig is om te bevestigen hoe sterk dit op mensen en normale voedingspatronen van toepassing is, opent de studie een nieuw perspectief op waarom hoge inname van rood vlees vaak samenhangt met diabetes en vetslever — en suggereert ze dat minder rood vlees eten de blootstelling aan deze subtiele moleculaire invloed kan verminderen.
Bronvermelding: Shen, L., Ma, J., Liang, S. et al. Cooked meat-derived extracellular vesicles ssc-miR-1 induces metabolic disorders in the mice liver via PI3k/AKT pathway. npj Sci Food 10, 59 (2026). https://doi.org/10.1038/s41538-026-00709-7
Trefwoorden: rood vlees, extracellulaire vesicles, microRNA, insulineresistentie, vetslever