Clear Sky Science · nl
Dubbele celtherapie uit vetweefsel bevordert arteriogenese en behoud van ledematen via vasculaire integratie bij kritisch ledemaatischemie
Ledematen redden door nieuwe bloedvaten te laten groeien
Wanneer slagaders in de benen geleidelijk verstopt raken, kunnen mensen invaliderende pijn, hardnekkige zweren en zelfs amputatie ontwikkelen. Deze ernstige fase, kritisch ledemaatsischemie genoemd, is berucht moeilijk te behandelen omdat veel patiënten geen bypassoperatie of andere standaardprocedures kunnen ondergaan. De hier samengevatte studie onderzoekt een nieuwe strategie: het gebruik van twee typen stamachtige cellen uit het eigen vet van een persoon om het lichaam te helpen robuuste nieuwe bloedvaten te laten vormen die verhongerd weefsel van het ledemaat kunnen redden.
Een veelvoorkomende ziekte met beperkte opties
Perifeer arterieel vaatlijden ontstaat wanneer slagaders in de benen vernauwen en de bloedstroom verstikken. In de ernstigste vorm, kritisch ledemaatsischemie, kunnen mensen aanhoudende pijn, zwartgekleurde tenen en een hoog risico op verlies van een deel van het ledemaat ervaren. Huidige therapieën zoals cholesterolverlagende medicijnen, angioplastiek of chirurgische bypass kunnen helpen, maar veel patiënten reageren niet of zijn te ziek voor deze ingrepen. Eerdere pogingen met één type stamcel stimuleerden meestal fragiele, kleine vaatjes die niet voldoende doorstroming bieden om het ledemaat betrouwbaar te redden. Onderzoekers wilden daarom een meer volledige “vervangende leidingsysteem” bouwen door twee samenwerkende celtypen te combineren.
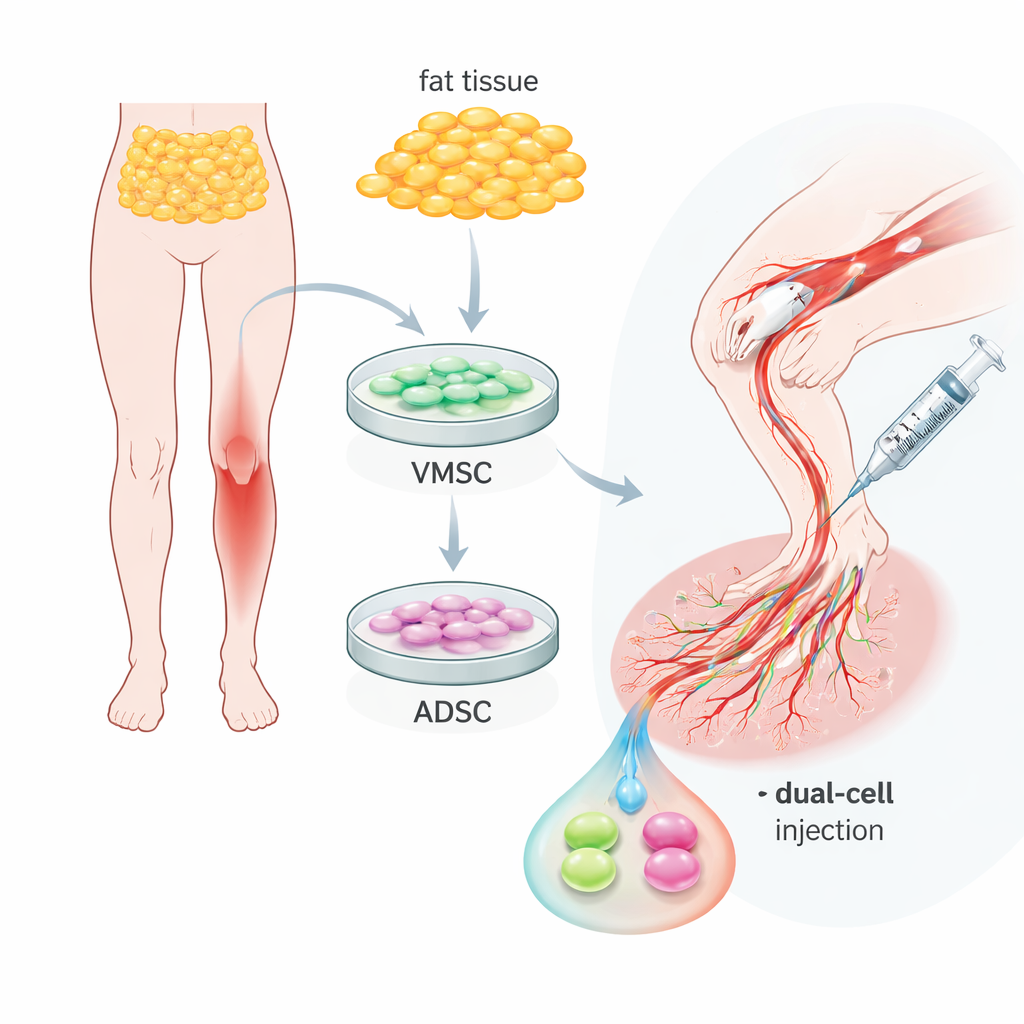
Twee nuttige celtypen in gewoon lichaamsvet
Het team richtte zich op vetweefsel—gewoon lichaamsvet—dat met relatief kleine ingrepen kan worden verzameld. Uit hetzelfde monster isoleerden ze twee verwante maar onderscheidende celpopulaties. De ene groep, genoemd vasculaire multipotente stamcellen, gedroeg zich veelal als vroege bloedvatbekledingscellen: ze droegen oppervlaktemarkers die typisch zijn voor endotheelcellen en konden zich in petrischaaltjes organiseren tot capillairachtige buisjes. De tweede groep, adipose-afgeleide stamcellen, leek meer op ondersteunende cellen die zich om vaten heen wikkelen en markers dragen die passen bij gladde spier- en perivasculaire cellen. Beide typen konden goed vermenigvuldigen en zich differentiëren naar vet-, bot- of kraakbeencellen, wat hun flexibiliteit bevestigde, maar hun natuurlijke rollen rond bloedvaten waren duidelijk verschillend en complementair.
Samenwerking onder stress
Om de harde, ontstoken omgeving van een ziek ledemaat na te bootsen, stelden de onderzoekers de cellen bloot aan een sterke ontstekingsprikkel. Beide celtypen overleefden en pasten hun gedrag aan door mengsels van groeifactoren en enzymen vrij te geven die cellen helpen te migreren en het omliggende weefsel te hervormen. Wanneer de endotheelachtige cellen alleen op een gel die vaatvorming bevordert werden gekweekt, konden ze basale buisjes vormen, terwijl de ondersteunende cellen voornamelijk klonterden. Namun, wanneer ze werden gemengd in een verhouding van twee tegen één, werden de buisjes dichter, continuër en beter bestand tegen ontstekingsstress. Dit suggereerde dat de twee celtypen samen niet alleen meer vaten kunnen vormen, maar ook meer volwassen en stabiele netwerken.
Testen van dubbele celtherapie in zieke muisledematen
Vervolgens gingen de wetenschappers over naar een muismodel van kritisch ledemaatsischemie, gecreëerd door het onderbreken van een hoofdslagader van het been. In het verhongerde beenspierweefsel injecteerden ze de gemengde humane cellen. Over vier weken verloren onbehandelde muizen vaak tenen of hele voeten, en hun spieren vertoonden littekenvorming en sterke ontsteking. Daarentegen behielden dieren die de duale celbehandeling kregen grotendeels hun ledematen. Doorstromingsscans toonden aan dat de circulatie in behandelde benen herstelde tot ongeveer 70 procent van normaal, vergeleken met minder dan 20 procent in de controlegroep. Microscopische en driedimensionale beeldvorming onthulden waarom: behandelde spieren bevatten veel meer middelgrote en grote vaten—arteriolenachtige vertakkingen—met sterke ‘mouwen’ van ondersteunende cellen, in plaats van slechts een warboel van kleine, instabiele capillairen.
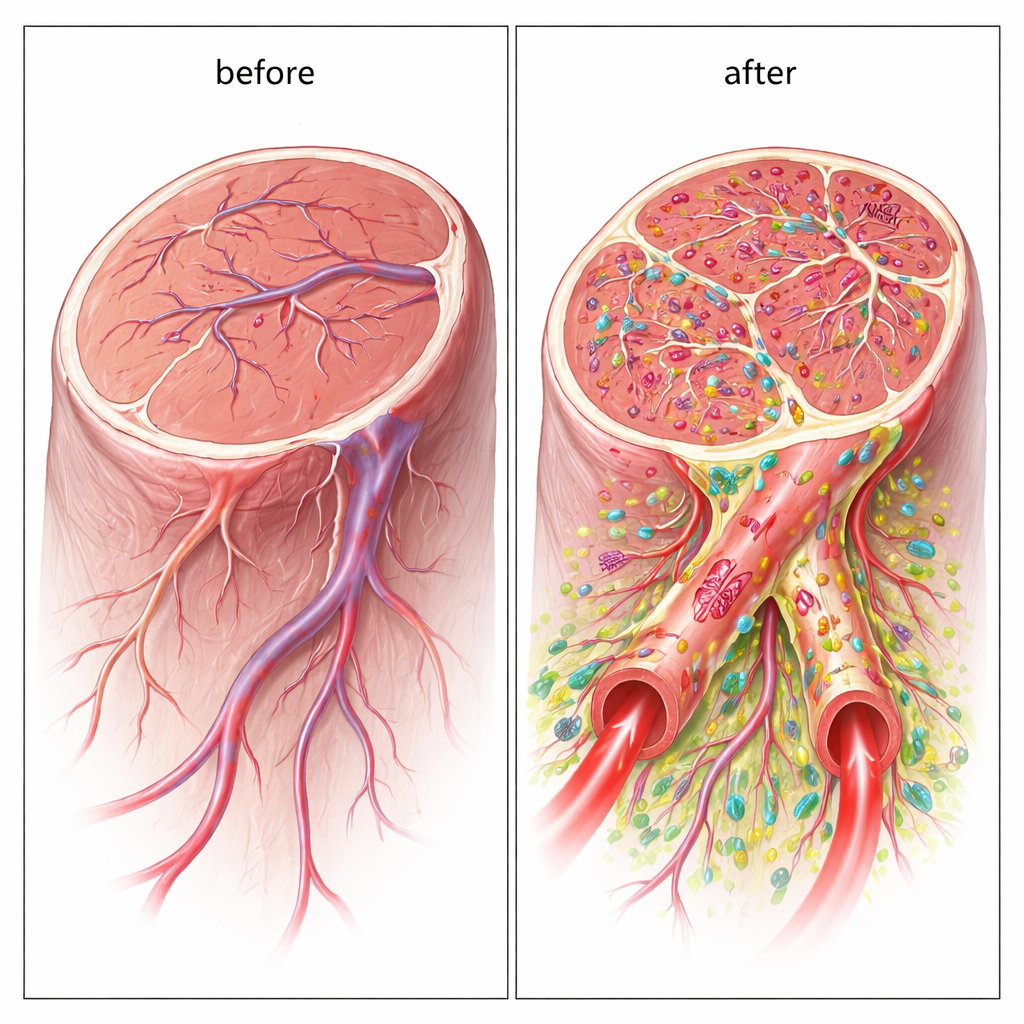
Hybride vaten opgebouwd uit donorcellen
Belangrijk is dat de nieuwe vaten niet alleen werden gestimuleerd door de cellen; ze bevatten daadwerkelijk de getransplanteerde menselijke cellen als onderdeel van hun wanden. Met human-specifieke markers vonden de onderzoekers dat de endotheelachtige cellen hielpen de binnenbekleding te vormen, terwijl de ondersteunende cellen zich om de buitenkant wikkelden. Veel van deze hybride vaten waren breed genoeg om als echte bloedgeleiders te functioneren, en fluorescerende tracers bevestigden dat er bloed doorheen stroomde. Dit directe bouwen van grote, geperfundeerde vaten onderscheidt de dubbele celbenadering van de meeste eerdere stamceltherapieën, die hoofdzakelijk vertrouwen op chemische signalen in plaats van blijvende structurele integratie.
Wat dit voor patiënten zou kunnen betekenen
Voor niet-specialisten is de kernboodschap dat wetenschappers mogelijk leren hoe ze doodgaande ledematen kunnen ‘herleidingen’ met behulp van iemands eigen vetafgeleide cellen. Door twee celtypen te koppelen—één die de binnentube vormt en één die de buitenste ondersteuning bouwt— genereert de therapie sterke, goed beklede slagaders en arteriolen in plaats van fragiele uitlopers. Bij muizen was dit voldoende om de bloedstroom te herstellen en verlies van ledematen te voorkomen. Hoewel meer werk nodig is om de veiligheid en effectiviteit op lange termijn bij mensen te bewijzen, wijst de studie op een toekomst waarin een minimaal invasieve vetafname aangepaste celmengsels kan leveren om de circulatie bij patiënten met een hoog amputatierisico te herbouwen.
Bronvermelding: Kim, D.Y., Hwang, D.Y., Park, G. et al. Adipose-derived dual cell therapy enhances arteriogenesis and limb preservation through vascular integration in critical limb ischemia. npj Regen Med 11, 13 (2026). https://doi.org/10.1038/s41536-026-00458-x
Trefwoorden: kritieke ledemaatsischemie, stamceltherapie, cellen afkomstig uit vetweefsel, neovascularisatie, perifeer arterieel vaatlijden