Clear Sky Science · nl
Remming van CDK8 herstelt verstoord ischemisch botbreukherstel
Waarom bloedtoevoer ertoe doet wanneer botten breken
De meeste gebroken botten groeien uiteindelijk weer aan elkaar, maar bij miljoenen mensen per jaar stokt dat proces. Slechte bloedtoevoer rond een breuk — bekend als ischemie — vergroot de kans aanzienlijk dat een breuk langzaam, slecht of helemaal niet geneest. Deze studie onderzoekt op cellulair niveau waarom dat gebeurt en test een experimentele pil die lijkt te duwen van littekenachtige reparatie terug naar echte botregeneratie.
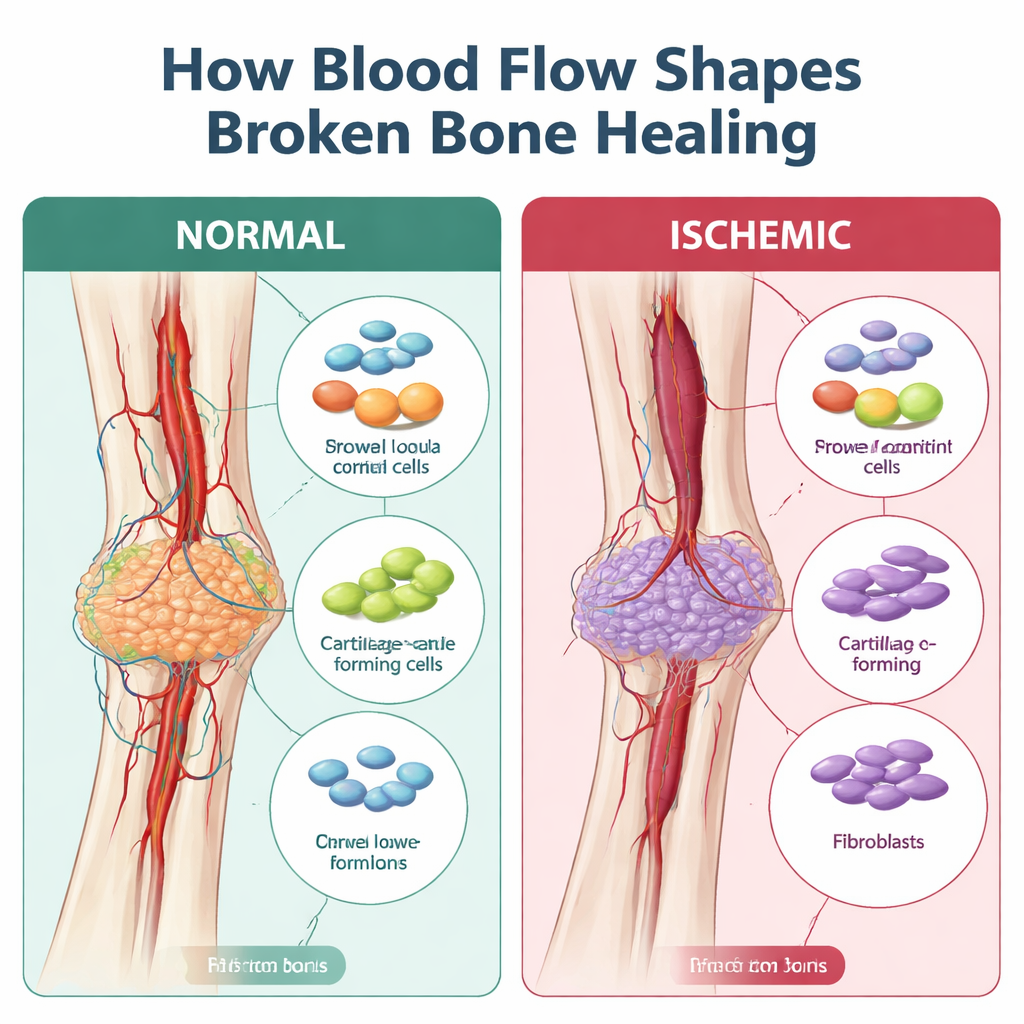
Wanneer genezing verandert in littekenvorming in plaats van opbouw
Bot geneest normaal gesproken door een zachte brug van kraakbeen te vormen die geleidelijk wordt vervangen door hard bot. Deze brug, het callus, hangt af van een aanvoer van stam-achtige ondersteunende cellen, immuuncellen en bloedvaten die de reparatie coördineren. Bij ischemische breuken toonde eerder werk aan dat het callus vaak kleiner, zwakker en gevuld is met vezelig weefsel — meer als een litteken dan een stevige plooi nieuw bot. Wat ontbrak, was een gedetailleerde kaart van welke cellen fout gaan, en wanneer, tijdens deze omweg van juiste genezing.
Enkele cellen onthullen een omweg naar fibrose
De onderzoekers gebruikten een muismodel waarbij een beenarterie chirurgisch wordt beschadigd op het moment van de breuk, wat nauw aansluit bij het verlies van bloedtoevoer dat wordt gezien bij ernstige verwondingen of bij mensen met vaatziekten of die roken. Ze voerden vervolgens single-cell RNA-sequencing uit, een techniek die de actieve genen in duizenden individuele cellen uitleest, op breukcallussen vier en zeven dagen na het letsel. In goed doorbloede breuken zat het vroege callus vol immuuncellen die snel plaatsmaakten voor uitbreidende stromale cellen — de ondersteunende cellen die kraakbeen en bot worden. Onder ischemische omstandigheden waren er echter veel minder kraakbeen- en botvormende cellen en veel meer fibroblasten, de cellen die vezelig weefsel aanleggen. Computationele ‘traject’-analyse liet zien dat stromale cellen in ischemisch bot vaak via een fibroblast-achtig stadium afsloegen in plaats van soepel volwassen te worden van vroege voorlopers naar kraakbeen, wat overeenkomt met het meer littekenachtige callus dat onder de microscoop werd gezien.
Een moleculaire rem op botopbouwende cellen
Bij het doorgronden van de genactiviteit van deze cellen vond het team een sterk signaal van cellulaire stress in ischemische callussen, waaronder hoge niveaus van heatshock-eiwitten. Een van de meest opvallende veranderingen was een stijging in activiteit van een gen genaamd Cdk8, dat codeert voor een regulerende enzymcomponent in een belangrijk transcriptiecomplex en kan vertragen of herleiden hoe cellen op signalen reageren. Cdk8 is in andere contexten bekend als een rem op celdifferentiatie. Hier was het bijzonder verhoogd in vroege stromale voorlopercellen in ischemisch bot. Menselijke mesenchymale stromale cellen die in laboratoriumomstandigheden met weinig zuurstof werden gekweekt — wat slechte bloedtoevoer nabootst — verhoogden ook CDK8, wat een directe koppeling laat zien tussen zuurstoftekort en deze potentiële “rem” op kraakbeen- en botvorming.
CDK8 uitschakelen om reparatie te herstellen
De onderzoekers vroegen zich vervolgens af of het blokkeren van CDK8 stromale cellen vrij kon maken om de juiste genezing te hervatten. In celkweek leidde behandeling van muis- en humane voorlopercellen met selectieve CDK8-remmers tot verhoging van belangrijke kraakbeengenes en meer productie van kraakbeenmatrix, en verbeterde ook mineralisatie wanneer dezelfde cellen werden gestimuleerd om bot te vormen. Het team testte vervolgens een oraal beschikbare CDK8/19-remmer genaamd SNX631-6 bij muizen met ischemische breuken. Wanneer toegediend tijdens het vroege, kraakbeenvormende venster, nam de hoeveelheid kraakbeen in het callus toe. Wanneer de behandeling werd verlengd tot de latere overgang van kraakbeen naar bot, lieten de callussen meer totaal bot, een hogere mineraalinhoud en grotere totale omvang zien op micro-CT-scans en weefseldoorsneden, wat wijst op robuustere structurele reparatie.
Van labinzichten naar mogelijke nieuwe therapieën
Samengevat suggereren de resultaten dat ischemie genezende cellen deels richting een gestreste, fibrotische afloop stuurt door CDK8 op te voeren, waardoor hun vermogen om kraakbeen en bot te vormen wordt geremd. Het blokkeren van dit enzym lijkt die rem los te laten, waardoor meer kraakbeen vroeg ontstaat en later meer bot wordt gelegd, zelfs wanneer de bloedtoevoer beperkt is. Omdat CDK8-remmers al worden getest bij kankerpatiënten, zouden ze op den duur mogelijk kunnen worden hergebruikt om mensen met een hoog risico op slechte breukgenezing — zoals ouderen, rokers of mensen met vaatziekte — te helpen sterk bot te laten herstellen in plaats van broos littekenweefsel.
Bronvermelding: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
Trefwoorden: genezing van botbreuken, ischemie, CDK8-remmer, mesenchymale stromale cellen, fibrose