Clear Sky Science · nl
Innesteling van wild-type alveolaire type II-epitheelcellen in muizen met een tekort aan surfactant-eiwit C
Waarom het repareren van kleine luchtblaasjes ertoe doet
Ademen lijkt moeiteloos, maar is afhankelijk van een fijn vliesje dat surfactant heet en dat de miljoenen kleine luchtblaasjes in onze longen bekleedt. Als surfactant ontbreekt of niet goed functioneert — zoals bij sommige zeldzame longziekten op kinderleeftijd — kunnen kinderen aanhoudende ademhalingsproblemen en littekenvorming in de longen krijgen. Op dit moment is de enige echte genezing een longtransplantatie, een optie die wordt beperkt door donortekorten en aanzienlijke risico’s. Deze studie onderzoekt een ander idee: beschadigde longen herstellen door gezonde, surfactant-producerende cellen te implanteren, wat mogelijk de weg opent naar zachtere, meer gerichte behandelingen.
Wanneer de verzorgers van de long het laten afweten
In elk luchtblaasje (alveolus) bevinden zich gespecialiseerde ‘verzorgende’ cellen, de alveolaire type II-cellen. Zij produceren en recyclen surfactant, wat voorkomt dat de luchtblaasjes inklappen en het ademen vergemakkelijkt. Bij sommige kinderen verstoren mutaties in genen die nodig zijn voor surfactantproductie — waaronder het surfactant-eiwit C-gen (SFTPC) — deze cellen. Het gevolg is een interstitiële longaandoening bij kinderen (chILD), gekenmerkt door ontstoken, verdikt longweefsel, littekens en soms respiratoire insufficiëntie. Artsen kunnen slechts ondersteunende medicatie en zuurstof bieden; voor de ernstigst getroffenen is longtransplantatie het laatste redmiddel. De auteurs onderzochten of het vervangen van een deel van de defecte verzorgende cellen door gezonde exemplaren de longschade zou kunnen vertragen of omkeren.
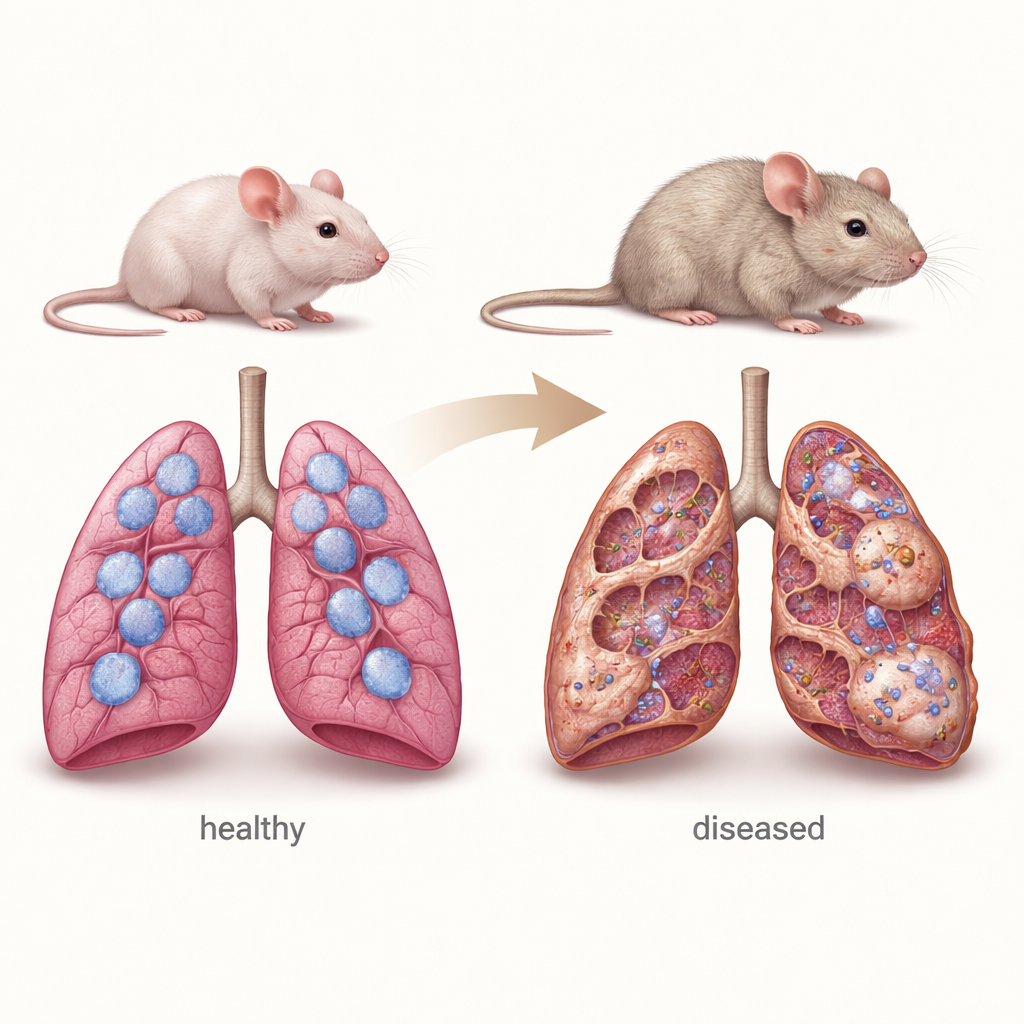
Een muismodel ter vervanging van een kinderlongziekte
Om kernkenmerken van chILD na te bootsen, gebruikten de onderzoekers muizen die het Sftpc-gen helemaal misten. Deze dieren worden geboren met ogenschijnlijk normale longen, maar naarmate ze ouder worden ontwikkelen ze kenmerken van chronische longaandoening: verdikte wanden tussen de luchtblaasjes, extra littekenweefsel rijk aan collageen, overmatige groei van type II-cellen en ophoping van immuuncellen. Gedetailleerde metingen toonden aan dat hun longarchitectuur tussen 4 en 12 maanden gestaag verslechtert, wat lijkt op de langzame progressie die bij veel menselijke patiënten wordt gezien. Het team vond ook dat deze muizen bijzonder gevoelig zijn voor het chemotherapiemiddel bleomycine, dat veel in laboratoria wordt gebruikt om longschade en fibrose te induceren, wat benadrukt hoe kwetsbaar hun surfactant-deficiënte longen zijn.
Beschadigde longen voorbereiden om nieuwe cellen te accepteren
Nieuwe cellen succesvol transplanteren in een reeds druk bezet orgaan is niet triviaal. De auteurs onderzochten of een zorgvuldig gekozen, lage dosis bleomycine als een soort ‘conditionerende’ behandeling kon fungeren — sommige defecte residentiële cellen beschadigen en zo ruimte maken voor nieuwkomers zonder de long te vernietigen. Bij Sftpc-deficiënte muizen verergerde zelfs een kleine hoeveelheid bleomycine de littekening en verlaagde het de niveaus van verschillende belangrijke type II-celmarkers, wat schade bevestigde. Toch was bij de laagste dosis de schade beperkt en bleef de eigen herstelreactie van de long actief. Dit evenwicht suggereerde een venster waarin getransplanteerde cellen de beste kans zouden hebben om zich te hechten, te overleven en bij te dragen aan herstel.
Gezonde surfactantcellen trekken in en gaan aan het werk
Het team isoleerde vervolgens gezonde type II-cellen uit normale muizen en bracht een miljoen van deze cellen rechtstreeks in de luchtwegen van Sftpc-deficiënte muizen, tien dagen na toediening van lage dosis bleomycine. Met een combinatie van eiwitkleuring en genetische tests toonden ze aan dat donorcellen efficiënt innestelden, vooral in jongere dieren. Deze getransplanteerde cellen maakten rijp surfactant-eiwit C — volledig afwezig in de gastheer — wat aangeeft dat ze niet alleen aanwezig waren, maar ook functioneel actief. De nieuwe cellen bleven ten minste twee maanden aanwezig. Belangrijk was dat muizen die celtransplantaties kregen minder longschade en minder ernstig beschadigde gebieden hadden vergeleken met muizen die alleen bleomycine kregen, wat suggereert dat zelfs gedeeltelijke vervanging van zieke cellen de voortgaande schade kan afremmen.
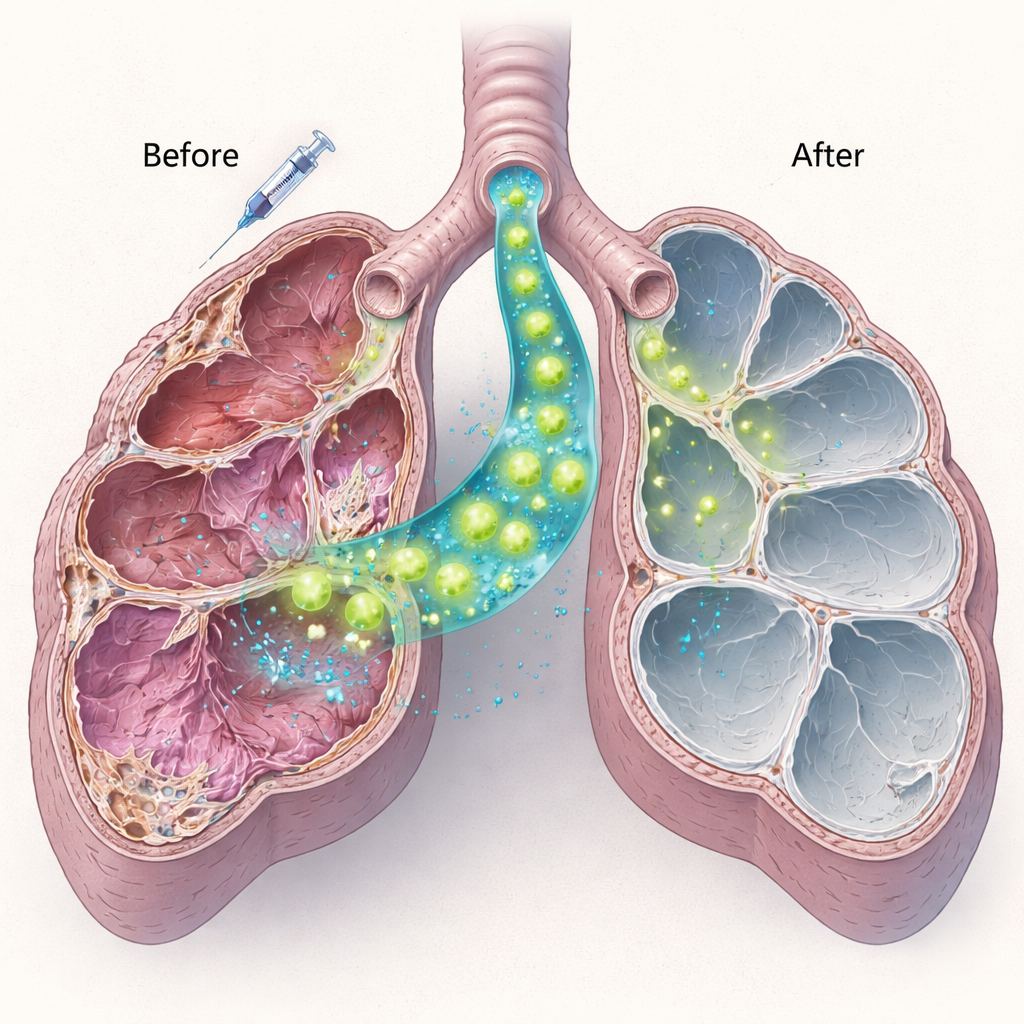
Van proof-of-concept naar toekomstige therapieën
Voor niet-specialisten is de kernboodschap dat deze studie een realistisch pad toont naar het herstellen, in plaats van vervangen, van longen bij bepaalde genetische kinderziekten. Door aan te tonen dat een bescheiden aantal gezonde surfactant-producerende cellen wortel kan schieten in een chronisch zieke long, het ontbrekende eiwit kan maken en de schade kan verminderen, biedt het werk een basis voor toekomstige therapieën op basis van gen-gecorrigeerde of stamcelafgeleide longcellen. Er blijven veel obstakels, waaronder het vinden van veiligere manieren om menselijke longen voor een dergelijke behandeling voor te bereiden en het waarborgen van langdurig voordeel. Toch verlegt dit onderzoek de discussie van symptoombeheer naar het potentieel om de eigen machinerie van de long voor gezond ademen te herbouwen.
Bronvermelding: Predella, C., Lapsley, L., Ni, K. et al. Engraftment of wild-type alveolar type II epithelial cells in surfactant protein C deficient mice. npj Regen Med 11, 11 (2026). https://doi.org/10.1038/s41536-026-00455-0
Trefwoorden: interstitiële longaandoening bij kinderen, surfactant-eiwit C, alveolaire type II-cellen, celtherapie, pulmonale fibrose