Clear Sky Science · nl
Profilering van 5-hydroxymethylcytosine in bloed onthult voorkeurstoename bij exon-introngrenzen en voorspellende waarde voor de ziekte van Parkinson
Waarom bloed aanwijzingen kan geven over Parkinson
De ziekte van Parkinson staat het meest bekend om tremoren en bewegingsproblemen, maar de vroege biologische veranderingen die tot deze symptomen leiden, zijn moeilijk te detecteren. Deze studie stelt een eenvoudige, praktische vraag met grote implicaties: kan een standaard bloedmonster subtiele chemische markeringen op DNA laten zien die zowel de biologie van Parkinson weerspiegelen als helpen mensen met de ziekte te onderscheiden van gezonde personen? Door zich te richten op deze DNA-markeringen zoeken de onderzoekers naar een brug tussen alledaagse milieu-exposities, onze genen en de geleidelijke achteruitgang van hersencellen die bij Parkinson wordt gezien.
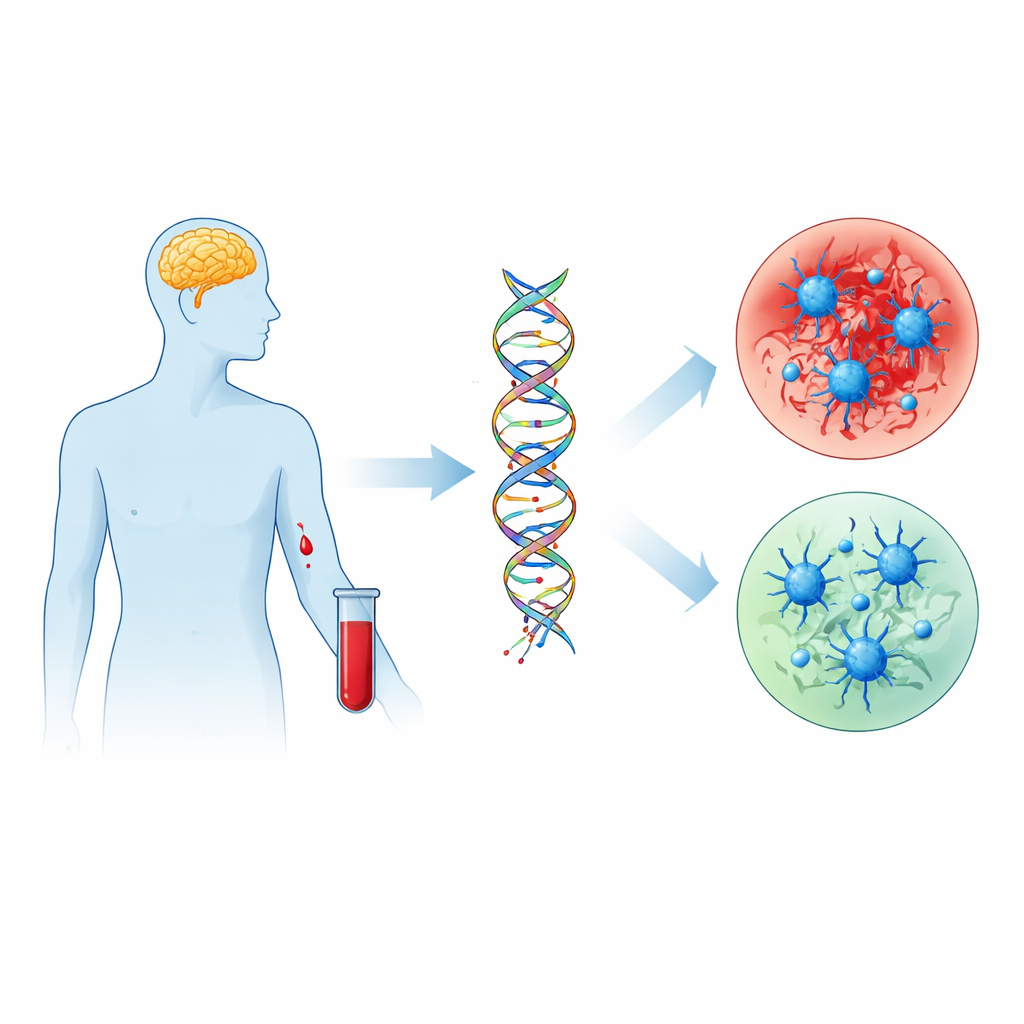
Kleine markeringen op DNA als chemische voetafdrukken
In elke cel draagt DNA niet alleen genetische code maar ook kleine chemische tags die helpen bepalen welke genen aan of uit staan. Twee van die tags, genoemd 5-methylering van cytosine (5-methylcytosine) en 5-hydroxymethylering van cytosine (5-hydroxymethylcytosine), werken als instelbare dimmers voor genactiviteit. Eerder onderzoek suggereerde dat deze tags veranderen in de hersenen van mensen met Parkinson, maar hersenweefsel is moeilijk te bestuderen bij levende patiënten. In deze studie richtten de wetenschappers zich in plaats daarvan op witte bloedcellen van 109 mensen met Parkinson en 49 neurologisch gezonde vrijwilligers. Ze maten de algemene niveaus van deze DNA-markeringen en gebruikten vervolgens hoogdichtheids-DNA-chips om in kaart te brengen waar in het genoom de tags waren veranderd.
Een wereldwijde daling van één belangrijke DNA-markering
Het team vond een consistente vermindering van de totale hoeveelheid 5-hydroxymethylcytosine in bloedcellen van mensen met Parkinson, terwijl het verwante merkteken 5-methylcytosine niet verschilde tussen de groepen. Dit patroon bleef bestaan nadat rekening was gehouden met leeftijd, geslacht, veelvoorkomende genetische risicovarianten en Parkinsonmedicatie zoals levodopa. Een statistisch model dat leeftijd, geslacht en de twee DNA-markeringen combineerde kon mensen met Parkinson in ongeveer 88 procent van de gevallen correct identificeren, waarbij 5-hydroxymethylcytosine naar voren kwam als een van de meest informatieve kenmerken. Deze globale niveaus volgden echter niet duidelijk de ziekteprogressie, wat suggereert dat ze meer wijzen op de aanwezigheid van Parkinson dan op het stadium ervan.
Waar de DNA-veranderingen de voorkeur tonen
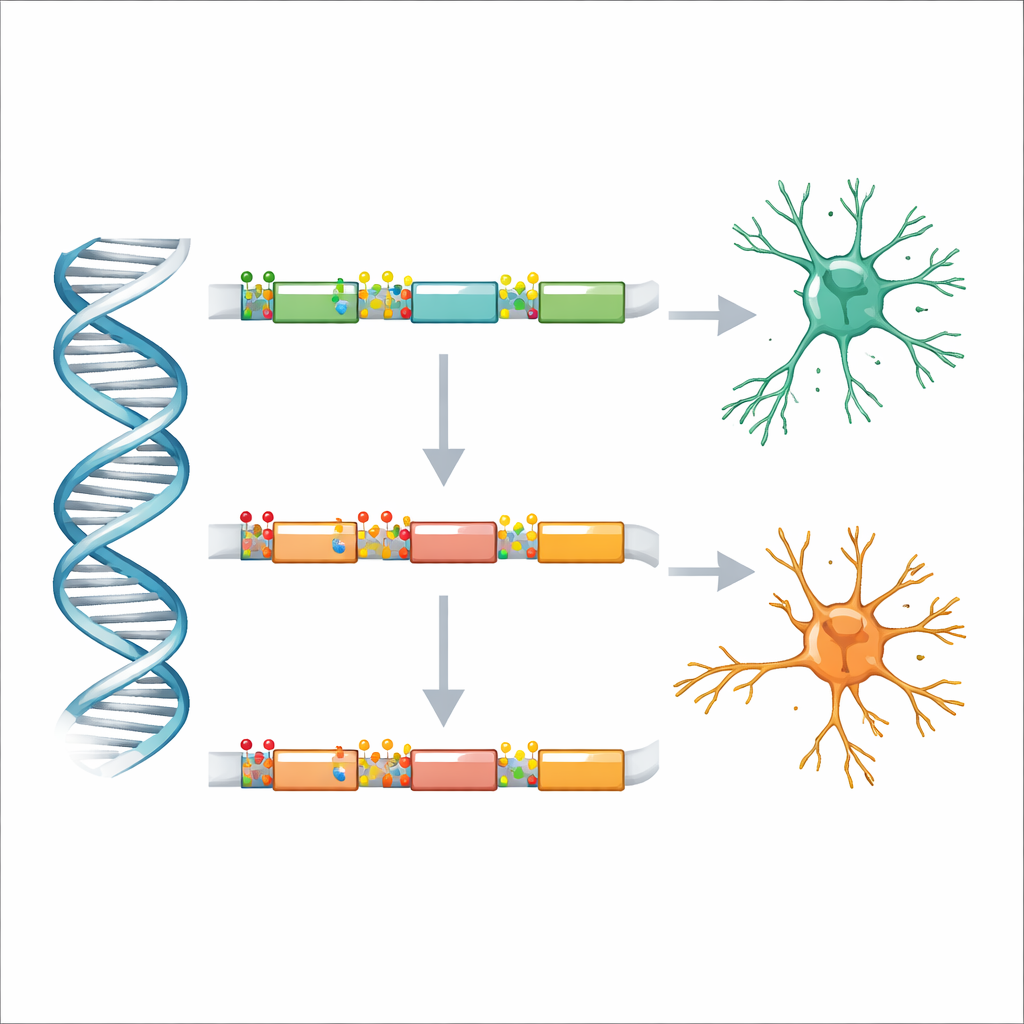
Bij nadere bestudering langs het genoom zagen de onderzoekers dat gewijzigde DNA-markeringen niet willekeurig verspreid waren. In plaats daarvan clusterden beide typen veranderingen binnen genen, met name in de DNA-streken die introns worden genoemd en tussen de eiwitcoderende stukken, de exons, liggen. Binnen deze introns lagen de sterkst getroffen regio’s dicht bij de grenzen waar een intron een exon ontmoet. Deze grenszones zijn belangrijk omdat ze sturen hoe RNA wordt geknipt en samengevoegd wanneer een gen wordt afgelezen, en bepalen welke versies van een eiwit worden geproduceerd. De studie suggereert dat bij Parkinson de DNA-markeringen vooral verstoord zijn op deze kritieke kruispunten, wat mogelijk cellen richting verschillende eiwitvarianten duwt.
Genetische netwerken die zenuwen, bloedvaten en immuniteit omvatten
De genen onder deze gewijzigde DNA-markeringen verwezen naar biologische systemen die al in verband werden gebracht met Parkinson. Regio’s met veranderde methylatie waren gelinkt aan zenuwcelcommunicatie, hersenontwikkeling en de vorming en herstructurering van bloedvaten. Regio’s met veranderde hydroxymethylatie daarentegen waren verrijkt voor genen betrokken bij immuunsignalering en bredere cel-tot-celcommunicatie. Veel benoemde genen hebben bekende rollen in het behoud van dopamine-producerende neuronen, het controleren van synapsen of het vormen van de immuun- en vasculaire omgeving van de hersenen. Gezamenlijk suggereren de patronen dat Parkinson een gecoördineerde verschuiving kan inhouden in hoe genen die zenuwfunctie, bloedstroom en immuunactiviteit beheersen worden gereguleerd.
Wat dit voor patiënten kan betekenen
Voor niet-specialisten is de belangrijkste conclusie dat een eenvoudige bloedafname DNA-"interpunctiemarkeringen" kan vastleggen die verschillen bij mensen met Parkinson, en dat deze verschillen het sterkst zijn op de kruisingen waar genen worden gespleten tot definitieve boodschappen. De studie is verkennend en gebaseerd op relatief kleine aantallen, dus ze kan nog geen oorzaak-en-gevolg aantonen of op zichzelf een klinische test ondersteunen. Toch versterkt ze het idee dat 5-hydroxymethylcytosine in bloed kan dienen als een praktisch biomarker om Parkinson te signaleren en om te onderzoeken hoe genregulatie, immuunreacties en veranderingen in bloedvaten bijdragen aan de ziekte. Met grotere vervolgonderzoeken kunnen deze chemische sporen op DNA helpen de diagnose en monitoring te verplaatsen van de hersenen — waar bemonstering moeilijk is — naar de bloedbaan, waar die veel toegankelijker is.
Bronvermelding: Antczak, P., Brandt, P., Radosavljević, L. et al. Profiling of 5-hydroxymethylcytosine in blood reveals preferential enrichment at exon-intron junctions and predictive value for Parkinson’s disease. npj Parkinsons Dis. 12, 76 (2026). https://doi.org/10.1038/s41531-026-01322-x
Trefwoorden: Ziekte van Parkinson, epigenetica, DNA-hydroxymethylatie, bloedbiomarkers, genregulatie