Clear Sky Science · nl
De olfactorische sensorische kaart is verstoord in een transgeen muismodel van de ziekte van Parkinson met overexpressie van menselijke wildtype α-synucleïne
Waarom verlies van reuk belangrijk is bij Parkinson
Veel mensen zien de ziekte van Parkinson vooral als een bewegingsstoornis, maar bij de meeste patiënten is het eerste dat achteruitgaat juist hun reukzin. Dit verlies kan decennia vóór tremor of stijfheid optreden, waardoor het een krachtig vroeg waarschuwingssignaal is. De hier beschreven studie stelt een eenvoudig maar onbeantwoord vraagstuk: wat gaat er precies mis in de reukcircuits van de hersenen wanneer Parkinson-gerelateerde veranderingen beginnen? Door dit te onderzoeken in een zorgvuldig geconstrueerd muismodel, laten de onderzoekers zien hoe een belangrijke Parkinson-eiwit de interne “geurkaart” van de hersenen verstoort en wijzen ze op een nieuwe, gemakkelijk toegankelijke bron van vroege ziekte-indicatoren.
De geurkaart van de hersenen
In onze neuzen bevinden zich miljoenen gespecialiseerde reukcellen die elk reageren op bepaalde odorantmoleculen. Deze cellen sturen lange, dunne vezels naar de voorkant van de hersenen, waar ze samenkomen in kleine knooppunten die glomeruli worden genoemd in de olfactorische bol. Elk geurtype activeert een specifiek patroon van glomeruli, waardoor een precieze sensorische kaart ontstaat die het brein in staat stelt koffie van kaneel of rook van parfum te onderscheiden. Bij gezonde muizen projecteren cellen die één type geurreceptor dragen (M72 genoemd) en een ander type (P2 genoemd) betrouwbaar naar precies twee goed gedefinieerde glomeruli per bol, wat een sterk geordende en reproduceerbare kaart oplevert.
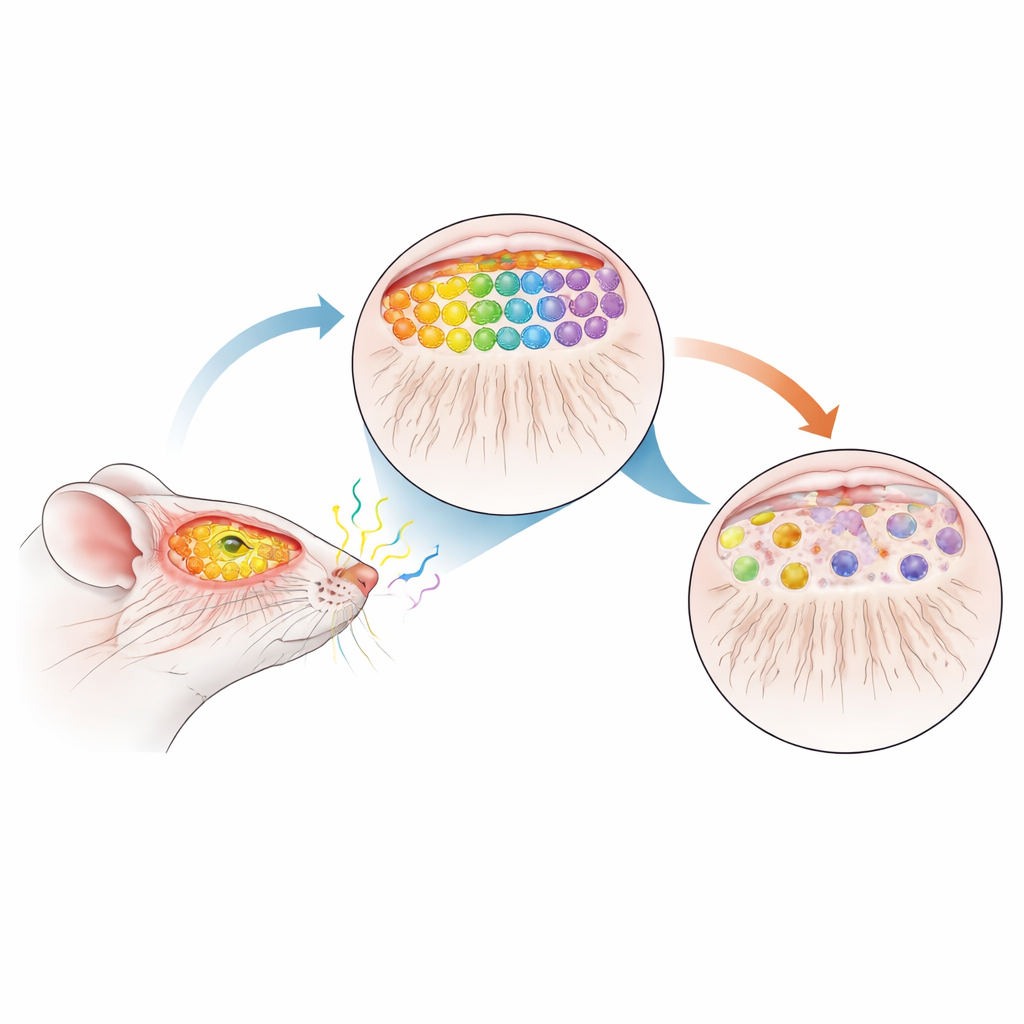
Een muis als plaatsvervanger voor vroeg Parkinson
Om te onderzoeken hoe de ziekte van Parkinson deze kaart zou kunnen verstoren, gebruikte het team muizen die een overproductie hebben van normale menselijke α-synucleïne, hetzelfde eiwit dat bij mensen met Parkinson in de hersenen samenklontert. Ze kruisten deze dieren vervolgens met M72- en P2-getagde muizen zodat ze geselecteerde reukcellen en hun verbindingen visueel konden volgen. Belangrijk is dat de extra α-synucleïne pas na de geboorte wordt aangezet en geleidelijk met de leeftijd ophoopt, wat het trage, progressieve verloop van de menselijke ziekte nabootst. Op een leeftijd van 12 maanden—ongeveer middenlevensduur voor een muis en vergelijkbaar met een prodromale, of pre-diagnostische, fase bij mensen—onderzoekten de onderzoekers het olfactorische systeem van de dieren in detail.
Wanneer de geurkaart uit elkaar valt
Door de getagde neuronen te kleuren en hun trajecten te volgen, vonden de wetenschappers een opvallende ineenstorting van de geurkaart in muizen die α-synucleïne overexpressen. Het aantal M72- en P2-cellen in de neus daalde sterk—ongeveer driekwartverlies voor M72 en bijna de helft voor P2—terwijl hun vezels naar de bol sterk verminderd waren. In plaats van keurig samen te komen op twee robuuste glomeruli, vormden de resterende vezels vaak meerdere, kleinere glomeruli van wisselende grootte en positie. Deze “extra” knooppunten verschenen niet op consistente locaties van muis tot muis, wat wijst op een verlies van de normale topografische precisie. Een breed merker voor reukcelterminals, VGLUT2, was ook met ongeveer 44% gereduceerd in de bol, wat aangeeft dat deze degeneratie veel verder ging dan de twee getagde receptortypen.
Verbindingen tussen kapotte circuits en verlies van reuk
De structurele schade vertaalde zich in meetbare geurproblemen. Oudere α-synucleïne-muizen deden er langer over om verstopte voeding te vinden, toonden een slechter vermogen om het ene odorant van het andere te onderscheiden, en lieten geen voorkeur zien voor gebieden die met hun eigen geur waren gemarkeerd—gedragstests die samen hyposmie en verminderde odorantdiscriminatie onthullen. Ze hadden ook veel sterkere geurconcentraties nodig om te reageren, wat een verminderde gevoeligheid aantoont. Deze tekorten verschenen niet bij jongere muizen, bij wie de getagde neuronen en hun kaarten er nog grotendeels normaal uitzagen, wat de timing van functioneel verlies koppelt aan de latere ineenstorting van de sensorische kaart in plaats van aan vroege ontwikkeling. Opmerkelijk is dat, hoewel het problematische eiwit overvloedig aanwezig was in de olfactorische bol, het niet detecteerbaar was in de sensorische bekleding van de neus zelf, wat wijst op veranderingen binnen de bolcircuits—met name in mitralcellen die geurinformatie doorgeven—als de waarschijnlijke oorzaak van de kaartverstoring.
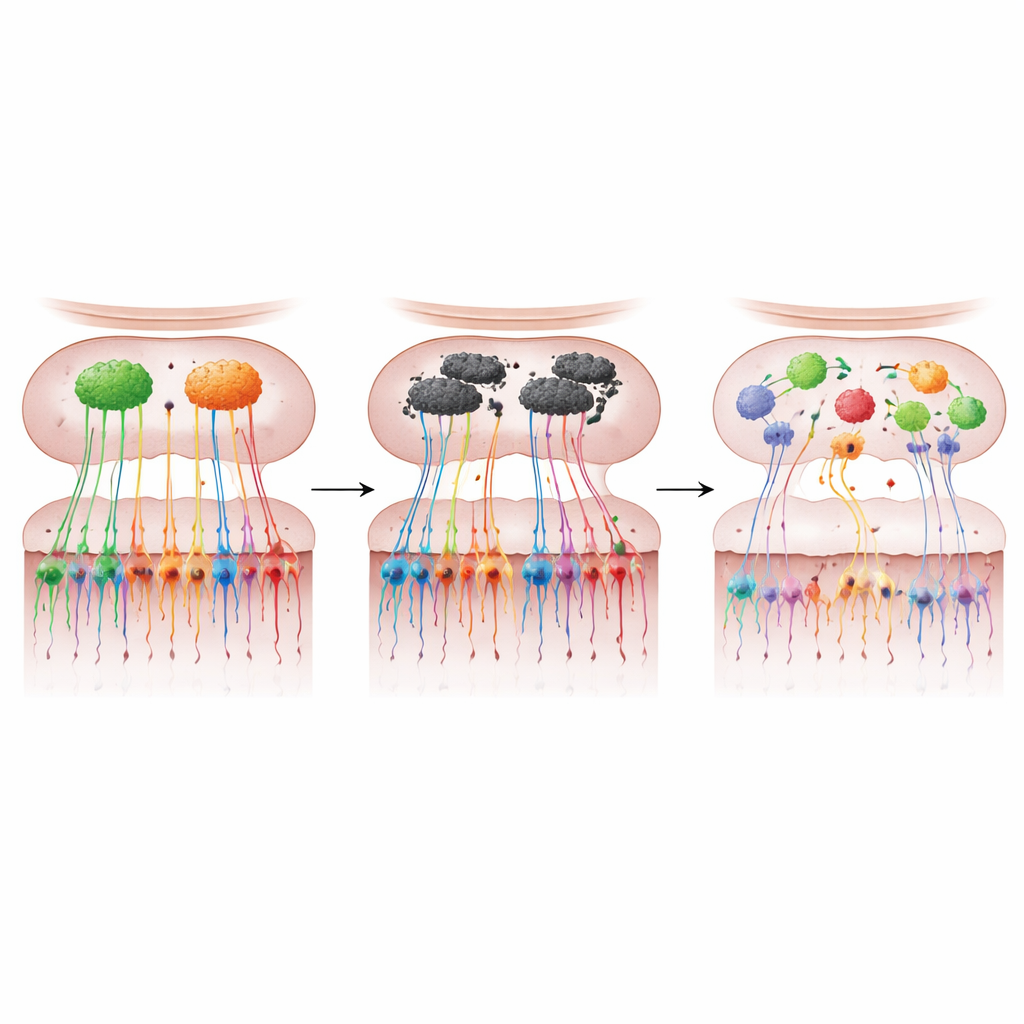
Reukcellen als vensters naar vroege ziekte
Samengevat ondersteunt dit werk een duidelijke boodschap voor niet-specialisten: in dit Parkinson-achtige muismodel leidt overproductie van α-synucleïne in de olfactorische bol tot zowel verlies als foutieve bedrading van reukneuronen, vervormt de geurkaart van de hersenen en veroorzaakt vroege reukproblemen. Omdat de sensorische cellen van de neus zich ontwikkelingsmatig verhouden tot de hersenen maar met minimaal invasieve swabs of biopsieën te bemonsteren zijn, betogen de auteurs dat soortgelijke veranderingen bij mensen een krachtige vroege biomarker voor de ziekte van Parkinson zouden kunnen opleveren. Het in kaart brengen van de moleculaire vingerafdrukken van deze cellen kan, zo suggereren ze, niet alleen helpen personen jaren vóór het optreden van bewegingssymptomen te identificeren, maar ook nieuwe inzichten bieden in hoe de ziekte begint en zich verspreidt—en hoe ze mogelijk vertraagd of voorkomen kan worden.
Bronvermelding: Biju, K.C., Hernandez, E.T., Stallings, A.M. et al. Olfactory sensory map is perturbed in a human wild-type α-synuclein overexpressing transgenic mouse model of Parkinson’s disease. npj Parkinsons Dis. 12, 70 (2026). https://doi.org/10.1038/s41531-026-01288-w
Trefwoorden: Ziekte van Parkinson, geurstoornis, alpha-synucleïne, sensorische kaart, biomarkers