Clear Sky Science · nl
LRRK2R1627P-mutatie versterkt door omgevingsfactoren geïnduceerde chronische ontsteking en α-synucleïne-aggregatie in de darm van ratten
Waarom de darm belangrijk is bij een hersenziekte
De ziekte van Parkinson staat vooral bekend om tremoren en bewegingsproblemen, maar toenemend bewijs wijst erop dat de oorsprong mogelijk ver van de hersenen ligt, diep in de darm. Deze studie onderzoekt hoe een specifieke genetische verandering die bij Aziatische populaties met Parkinson in verband wordt gebracht, samen met veroudering en blootstelling aan toxines, geleidelijk de darm van ratten kan beschadigen. Door te volgen wat er in de darm gebeurt gedurende het leven van de dieren, traceren de onderzoekers hoe alledaagse afweermechanismen kunnen omslaan in chronische ontsteking, en zo een omgeving creëren waarin eiwitten die met de ziekte samenhangen zich ophopen en mogelijk uiteindelijk de hersenen bedreigen.
Een risicogen in het spijsverteringskanaal
De wetenschappers concentreerden zich op een variant van het gen LRRK2, dat al lang in verband wordt gebracht met de ziekte van Parkinson en bepaalde inflammatoire darmziekten. Ze creëerden ratten die de corresponderende mutatie droegen, genoemd LRRK2R1627P, en vergeleken die levenslang met normale ratten. Hoewel de hoeveelheid LRRK2-mRNA in de darm niet veranderde, waren het totale LRRK2-eiwit en een belangrijke activiteitssignatuur ervan verminderd, wat aangeeft dat de mutatie de normale functie van dit eiwit in de darm verzwakt. Deze subtiele moleculaire wijziging veroorzaakte geen directe dramatische schade, maar veranderde stilletjes de manier waarop darmcellen zichzelf vernieuwen en organiseren naarmate de dieren ouder werden.
Een verouderende darm onder langzaam, persistent gewicht
Na verloop van maanden ontwikkelden de ratten met de mutatie duidelijke tekenen van verstoorde darmstructuur. Hun dunne darmen werden korter en de fijne, vingervormige villi en zakjes (crypten) die voedingsstoffen opnemen, werden kleiner. Bepaalde gespecialiseerde cellen in het epitheel die beschermend slijm en antimicrobiële stoffen produceren — gobletcellen en Panethcellen — namen af, terwijl eiwitten die burencellen helpen om strakke, lekbestendige verbindingen te vormen ook daalden. Onder de microscoop werden deze verbindingen korter of wijder, wat wijst op een verzwakte barrière. Belangrijk is dat de algehele architectuur niet instortte; in plaats daarvan toonde de darm een meer insidieus patroon van verminderde vernieuwing en bescherming, wat hem kwetsbaarder kan maken voor irritatie en infectie. 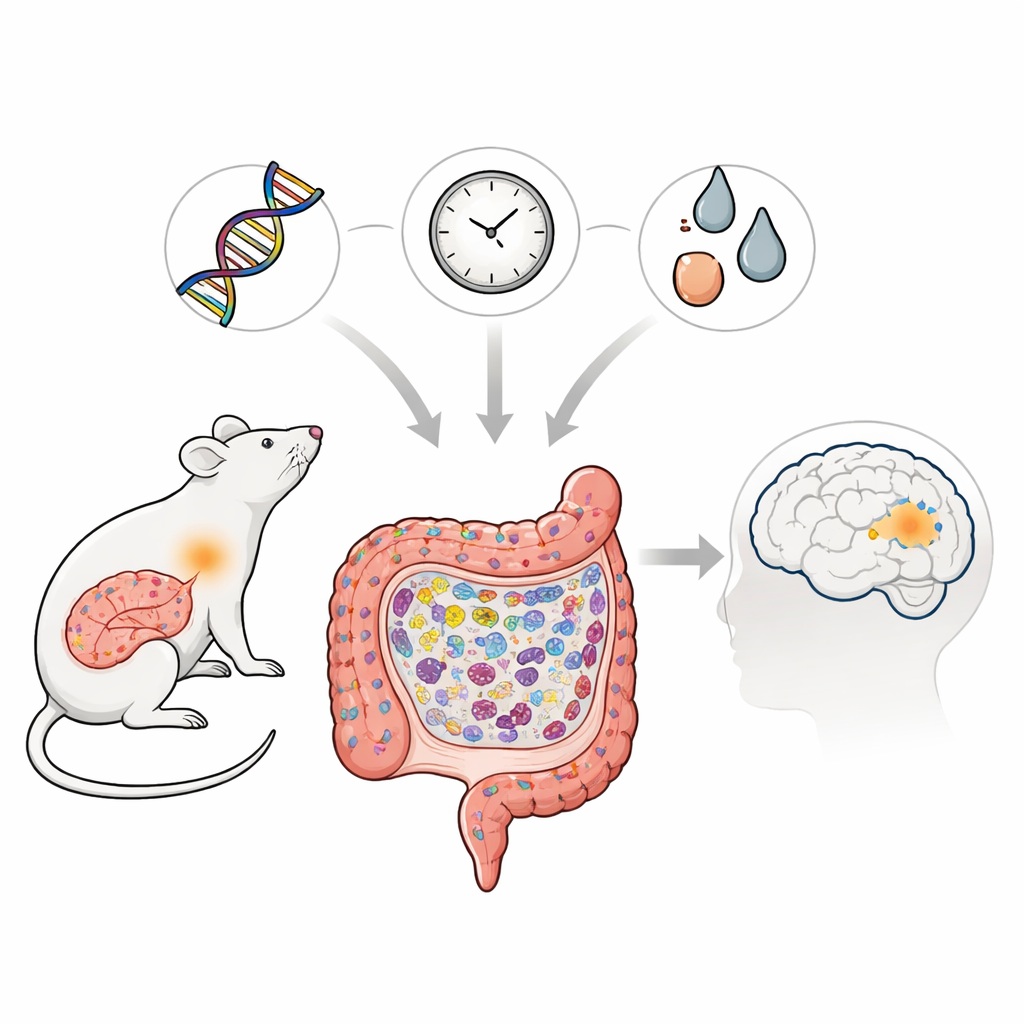
Immuunsysteem op scherp
Om te begrijpen waarom de darm uit balans raakte, onderzochten de onderzoekers genexpressie en immuuncellen in de darmwand. Ze vonden dat routes gekoppeld aan de sensor TLR4 en haar partner NF-κB overactief waren in oudere mutantenratten. Deze sensoren helpen normaal gesproken bij het detecteren van schadelijke microben, maar hier leidden ze tot een ophoping van ‘vecht-eerst’-immuuncellen, bekend als M1-macrofagen. Deze cellen produceerden ontstekingsmoleculen, waardoor de darm een chronisch geïrriteerde omgeving werd. Opvallend genoeg begon het met Parkinson geassocieerde eiwit α-synucleïne, in zijn ziekte-geassocieerde gefosforyleerde vorm, zich op te hopen niet in darmneuronen maar binnen deze geactiveerde macrofagen in de dunne darm, vooral bij oudere dieren.
Extra gevoelig voor omgevingsinslagen
De genetische mutatie alleen vertelde niet het hele verhaal. Toen jonge ratten kort werden blootgesteld aan bacteriële toxinen (LPS), die TLR4 stimuleren, ontwikkelden dieren met de LRRK2-mutatie veel ernstigere darmontsteking dan hun normale soortgenoten. Hun darmslijmvlies verloor meer cellen, barrière-eiwitten daalden verder en pro-inflammatoire macrofagen namen sterk toe, waarbij opnieuw abnormale α-synucleïne zich ophoopte. Dit suggereert dat mensen met vergelijkbare mutaties bijzonder gevoelig kunnen zijn voor omgevingsfactoren die de darm verstoren, zoals bepaalde infecties of toxines, wat hun langdurige risico kan versterken.
Het alarmsignaal dempen
Aangezien TLR4 centraal stond in deze ontstekingscascade, testte het team een middel, TAK-242, dat specifiek TLR4-signaalgeving dempt. Toegediend over meerdere maanden aan middelbare leeftijdsratten, herstelde de remmer grotendeels de lengte van de dunne darm, de grootte van villi en crypten, het aantal slijmproducerende cellen en de barrière-eiwitten. Het verminderde overactieve macrofagen, verlaagde ontstekingsmoleculen en sneed de ophoping van abnormale α-synucleïne in de darm sterk terug. Tegelijkertijd corrigeerde het een verstoorde microbegemeenschap: diversiteit nam toe, een overgroei van Lactobacillus nam af en verschillende gunstige bacteriegroepen herstelden zich, terwijl voorspelde microbiële functiesverschuifden weg van ziekte-geassocieerde patronen. 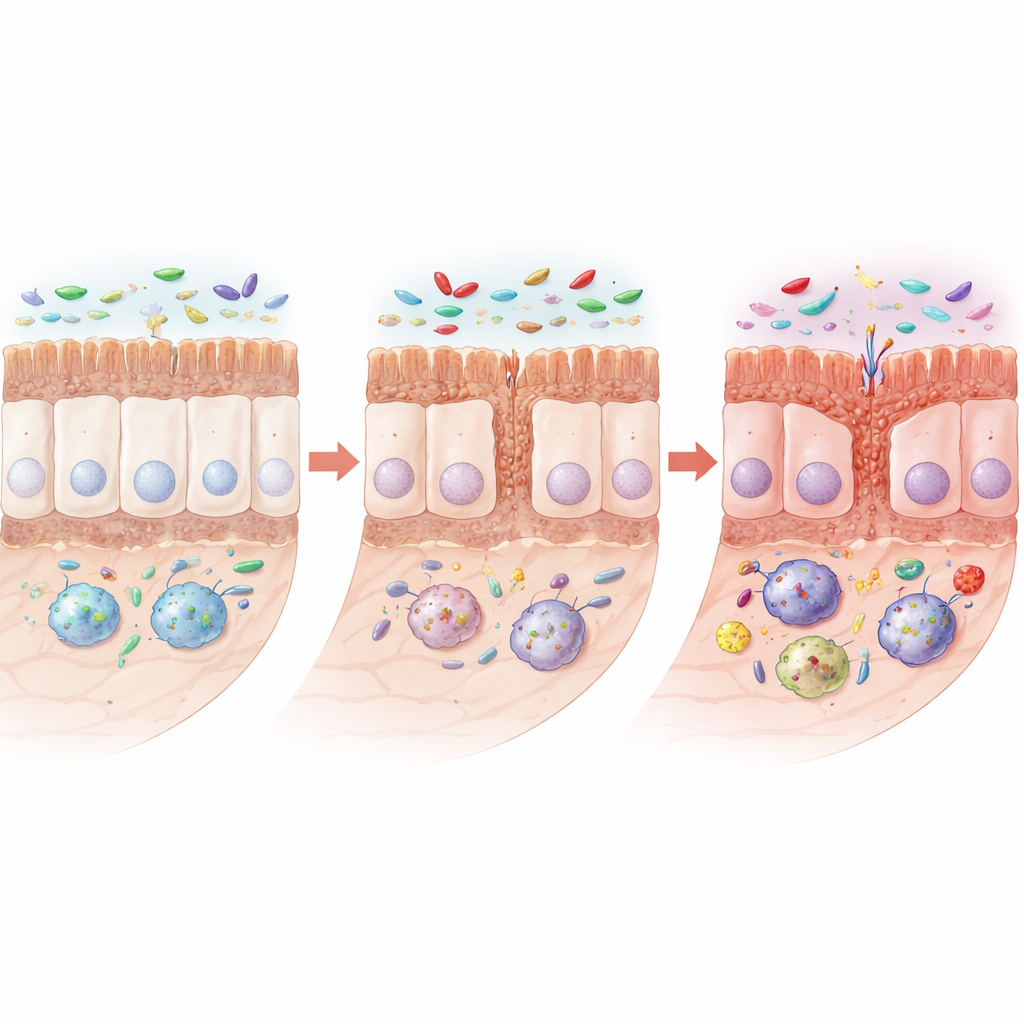
Wat dit betekent voor het Parkinsonrisico
Voor niet-specialisten is de kernboodschap dat een ‘Parkinson-gen’ de immuunverdediging van de darm in de loop van de tijd subtiel kan herschikken, vooral in combinatie met veroudering en omgevingsstress. Bij deze ratten resulteert dat in een chronische, laaggradige ontsteking die de intestinale barrière verzwakt, de residentiële microbiota verstoort en Parkinson-geassocieerd eiwit doet ophopen in immuuncellen — nog geen volledige Parkinson, maar een biologische context die later voor hersenziekte gunstig kan zijn. Door aan te tonen dat het blokkeren van één darmimmuunroute veel van deze veranderingen kan terugdraaien, benadrukt de studie de darm als een praktisch vroeg doelwit: het beschermen van darmgezondheid en het beteugelen van darmontsteking kan helpen het ontstaan van Parkinson uit te stellen of te voorkomen bij mensen met genetisch risico.
Bronvermelding: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
Trefwoorden: Ziekte van Parkinson, darmontsteking, LRRK2-mutatie, microbioom, aangeboren immuniteit