Clear Sky Science · nl
Systematische evaluatie van regulatoren van mitochondriale morfologie voor verbetering van neuronale α-synucleinopathie
Waarom kleine energiecentrales ertoe doen bij hersenziekten
Mitochondriën, de „energiecentrales” van de cel, zijn cruciaal om neuronen in leven te houden en hun verbindingen te laten functioneren. Bij hersenaandoeningen zoals de ziekte van Parkinson zien deze kleine structuren er vaak beschadigd of versnipperd uit, maar het is lastig geweest vast te stellen welke veranderingen schadelijk zijn en welke schakelaars we veilig kunnen omzetten om ze te beschermen. Deze studie test systematisch belangrijke mitochondriale „vormregelaars” in een laboratoriummodel van Parkinson‑achtige eiwitophoping, met behulp van een kunstmatige‑intelligentie‑tool om mitochondriale vormen in verschillende delen van neuronen te meten. Het werk wijst op één specifieke regulator, Fis1, als een veelbelovend doelwit om mitochondriën — en synapsen — gezond te houden zonder nieuwe bijwerkingen te veroorzaken.
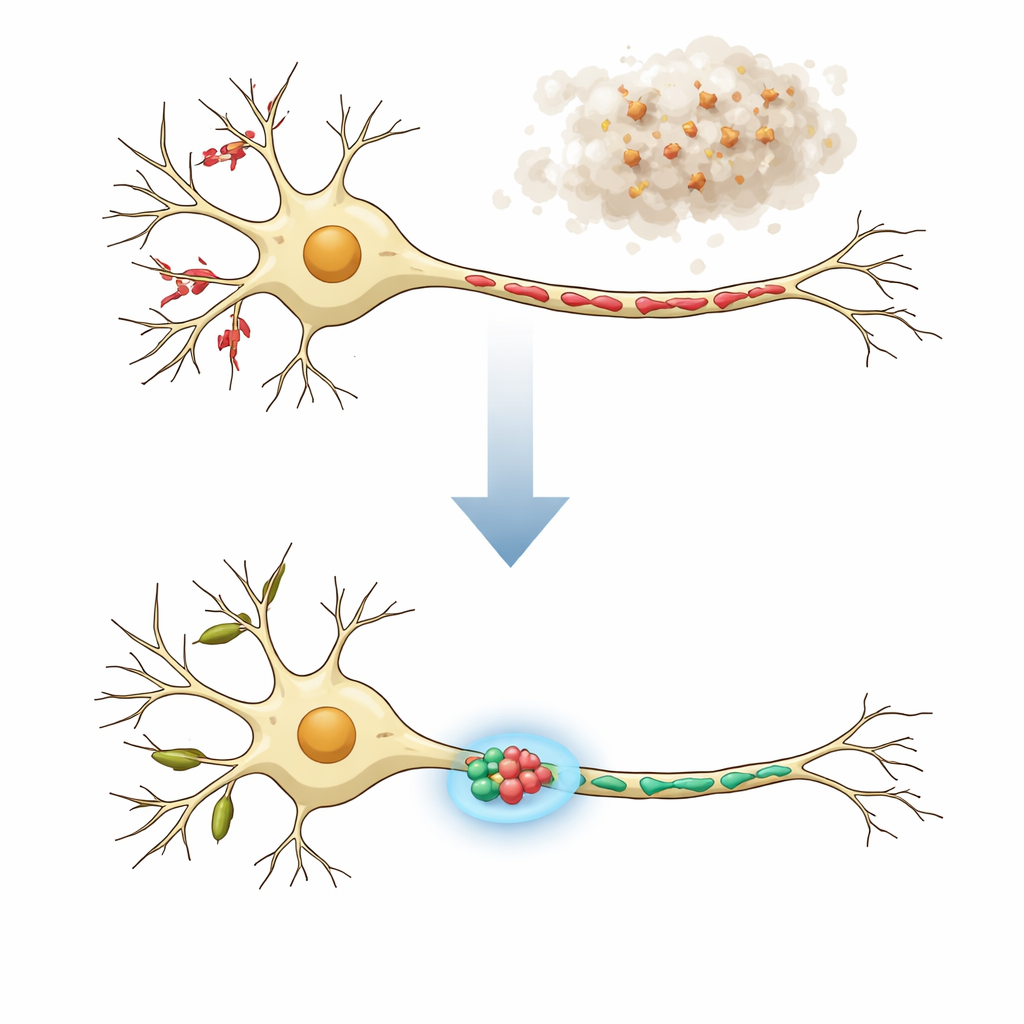
De twee buurten van een zenuwcel
Neuronen zijn niet uniform: hun boomachtige vertakkingen (dendrieten) en lange kabels (axon) hebben verschillende taken en herbergen mitochondriën met sterk verschillende vormen. In gezonde zenuwcellen bevatten dendrieten doorgaans lange, buisvormige mitochondriën die lokale eiwitsynthese en flexibele communicatie bij ontvangende sites, de dendritische spines, ondersteunen. Axonen, die signalen verzenden, bevatten juist veel korte mitochondriën die energie leveren en helpen calciumniveaus te reguleren bij presynaptische terminals. Bij neurodegeneratieve ziekten kunnen zowel de functie als de structuur van deze mitochondriën verstoord raken, wat zich uit als fragmenten, gezwollen vormen of kralenachtige reeksen. De auteurs redeneerden dat echt effectieve behandelingen mitochondriën in zowel dendrieten als axonen moeten herstellen naar hun normale, compartimentspecifieke vormen.
Opzetten van een Parkinson‑achtige stresstest
Om een kernmerk van de ziekte van Parkinson en verwante aandoeningen na te bootsen, werden gekweekte muiscorticale neuronen blootgesteld aan vooraf gevormde fibrillen van alpha‑synucleïne, een eiwit dat kan samenklonteren tot schadelijke aggregaten. Binnen enkele dagen seedden deze fibrillen abnormale alpha‑synucleïne‑ophopingen in de cellen en leidden ze tot uitgesproken mitochondriale fragmentatie in zowel dendrieten als axonen. Met MitoVis, een deep‑learning beeldanalysetool, kon het team automatisch dendrieten van axonen scheiden in microscoopbeelden en de lengte, oppervlakte en vorm van honderden mitochondriën per beeld meten — ongeveer tien keer sneller dan handmatig traceren. Deze hoge‑doorvoermethode bevestigde dat de ziekte‑achtige conditie mitochondriën verkortte en ronder maakte, overeenkomend met bevindingen uit diermodellen en patiëntweefsel.
Testen van de schakelaars voor mitochondriale vorm
Vervolgens vroegen de onderzoekers of het bijsturen van specifieke fusie‑ en splitsingsproteïnen deze schade kon voorkomen. Het verhogen van twee fusieproteïnen (Mfn1 en Mfn2) of het onderdrukken van een splitsingsproteïne (Mff) beschermde dendritische mitochondriën tegen door alpha‑synucleïne veroorzaakte verkorting en behield ook dendritische spines. Dezezelfde manipulaties maakten axonale mitochondriën echter te lang, iets wat eerder werk koppelde aan problemen met signaalafgifte en axonale vertakking. In contrast herstelde het terugschakelen van een ander splitsingsproteïne, Fis1, de mitochondriale lengte in zowel dendrieten als axonen tot bijna normale waarden zonder overmatige verlenging. Belangrijk is dat in dit opzet Fis1‑reductie geen neuronen deed afsterven en, net als de andere interventies, de dichtheid van dendritische spines behield die onder alpha‑synucleïne‑stress anders zou afnemen.
Calcium in balans houden
Aangezien mitochondriën in axonen helpen calcium te bufferen tijdens elektrische activiteit, onderzochten de onderzoekers of het veranderen van hun vorm dit fijne evenwicht beïnvloedde. Ze gebruikten een fluorescerende calciumsensor gericht op mitochondriën in presynaptische boutons en stimuleerden axonen met korte reeksen actiepotentialen. In de alpha‑synucleïne‑conditie leek de calciumhuishouding in licht verkorte axonale mitochondriën vergelijkbaar met normaal. Maar wanneer axonale mitochondriën te lang werden door overexpressie van Mfn1 of door knockdown van Mff, namen ze na stimulatie meer calcium op dan gebruikelijk. Deze verhoogde opname kan de presynaptische functie verstoren. Daarentegen behield Fis1‑knockdown, dat de mitochondriale lengte normaliseerde maar niet overschoot, mitochondriale calciumpatronen die sterk overeenkwamen met gezonde controles, wat duidt op minder verborgen compromissen.
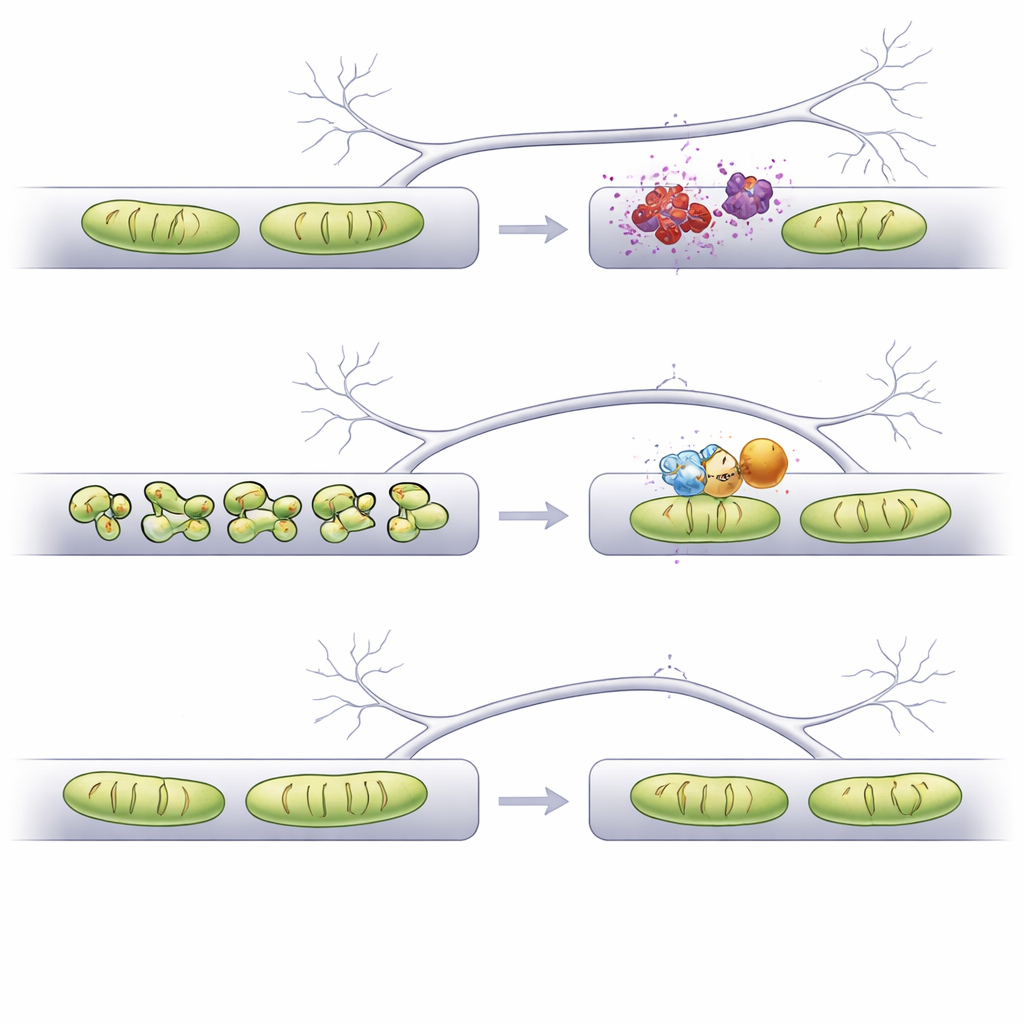
Wat dit kan betekenen voor toekomstige behandelingen
Alles bij elkaar laat de studie zien dat het simpelweg langer maken van mitochondriën niet voldoende is — het herstellen van hun vorm naar de juiste omvang in het juiste compartiment is beslissend. Met een AI‑ondersteunde beeldverwerkingsworkflow identificeren de auteurs Fis1 als een bijzonder aantrekkelijk doelwit: het omlaag brengen van Fis1 houdt mitochondriën structureel stabiel in zowel dendrieten als axonen, voorkomt verlies van dendritische spines en vermijdt abnormale calciumhuishouding in presynaptische terminals. Deze bevindingen ondersteunen het idee dat het zorgvuldig bijsturen van mitochondriale vorm, mogelijk met geneesmiddelen of antisense‑moleculen gericht op Fis1, kwetsbare synapsen kan helpen beschermen bij Parkinson‑gerelateerde alpha‑synucleinopathie en mogelijk andere hersenziekten waarin mitochondriën ontsporen.
Bronvermelding: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
Trefwoorden: Ziekte van Parkinson, mitochondriën, alpha-synucleïne, synaaptische disfunctie, neurodegeneratie