Clear Sky Science · nl
Klinische bruikbaarheid van geevokeerde potentialen voor het programmeren van subthalamische diepe hersenstimulatie bij de ziekte van Parkinson
Waarom dit verhaal over een hersenpacemaker ertoe doet
Voor veel mensen met de ziekte van Parkinson werken medicijnen uiteindelijk niet meer vloeiend. Ze kunnen wisselen tussen stijfheid en oncontroleerbare bewegingen, en het finetunen van de behandeling wordt een frustrerende cyclus van poliklinische bezoeken. Dit overzichtsartikel onderzoekt hoe artsen de elektrische echo’s van de hersenen—geëvokeerde potentialen genoemd—kunnen gebruiken om diepe hersenstimulatie (DBS) sneller en objectiever te programmeren. In wezen vraagt het of we DBS kunnen veranderen van zorgvuldig giswerk naar een meer datagestuurde, gepersonaliseerde hersenpacemaker.
Van vallen op je snufferd naar gerichte afstemming
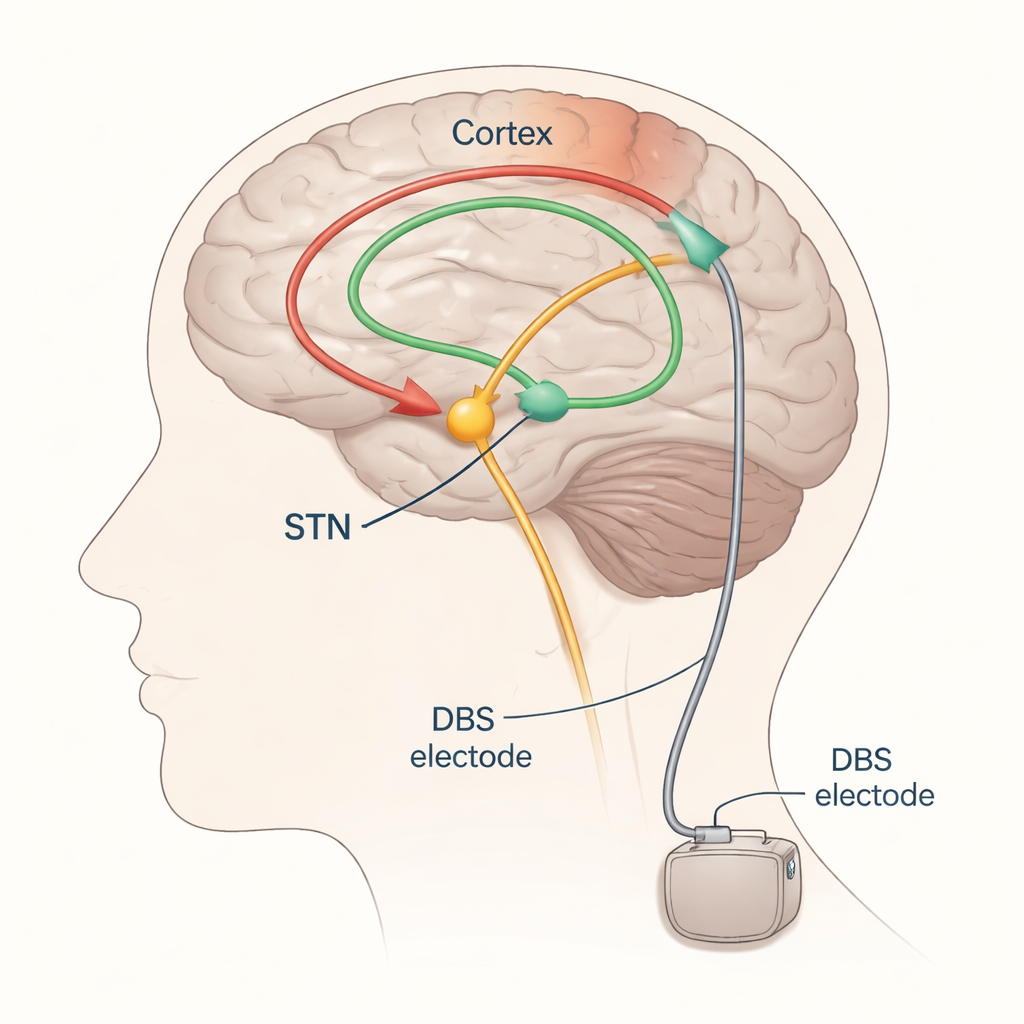
DBS bij Parkinson richt zich meestal op een kleine structuur diep in de hersenen die de nucleus subthalamicus (STN) heet. Elektroden worden daar geïmplanteerd en verbonden met een pulsgenerator onder de huid in de borst. Goed afgesteld kan STN‑DBS tremor, traagheid en stijfheid verminderen, maar als het elektrische veld te ver uitwaaiert kan het per ongeluk nabijgelegen banen stimuleren die spieren of gevoel aansturen, wat bijwerkingen zoals spiertrekking of tintelingen veroorzaakt. Tegenwoordig stellen neurologen DBS gewoonlijk bij door instellingen langzaam te veranderen en de bewegingen en bijwerkingen van de patiënt te observeren—een aanpak die tijdrovend is, afhangt van hoe de patiënt zich die dag voelt en vaak meerdere vervolgafspraken vereist.
Luisteren naar de elektrische echo’s van de hersenen
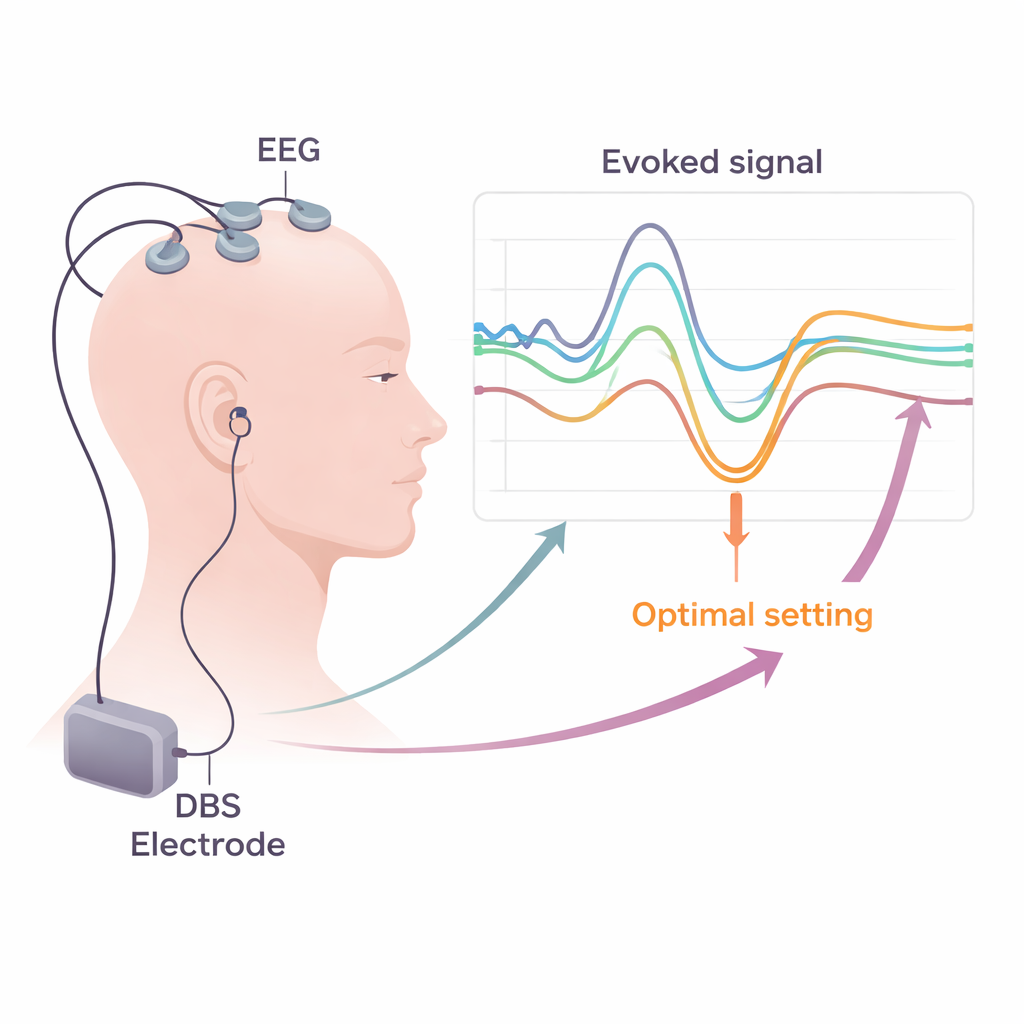
De auteurs richten zich op geëvokeerde potentialen—kleine, tijdsgelimiteerde elektrische reacties in de hersenen of spieren na een stimulus—als potentiële borden voor goede en slechte DBS‑instellingen. Wanneer de STN wordt gestimuleerd, reizen activiteitsgolven langs zenuwbanen en zijn ze op de schedel met EEG, in spieractiviteit met EMG, of soms met opnamebanen direct op het hersenoppervlak op te vangen. Door herhaaldelijk met lage frequenties te stimuleren en de reacties te middelen, kunnen onderzoekers betrouwbaar onderscheidende golven zien die na elke puls op verschillende vertragingen (milliseconden) verschijnen. Vroege golven, binnen ongeveer twee duizendsten van een seconde, weerspiegelen vooral activatie van snelle motorische banen dicht bij de elektrode. Iets latere golven, rond drie milliseconden (vaak de “P3”‑component genoemd), worden verondersteld voort te komen uit een directe verbinding tussen de frontale cortex en de STN, bekend als het hyperdirecte pad. Nog latere golven reizen waarschijnlijk via langere, meer circulerende circuits die de thalamus en andere diepe kernen omvatten.
Het sweet spot vinden en problemen vermijden
Over veel studies heen ontstaat een consistent beeld: contacten op de DBS‑leiding die een sterke, kort‑latente P3 veroorzaken blijken vaak te liggen in het meest hulpzame deel van de STN en worden geassocieerd met betere verbetering van Parkinson‑motorische symptomen en een ruimere “therapeutische marge” voordat bijwerkingen optreden. Daarentegen duiden zeer vroege golven die verband houden met motorische banen en bepaalde 8–10 milliseconde reacties er vaak op dat de stimulatie zich verspreidt naar aangrenzende structuren, waardoor het risico op spiercontracties of andere ongewenste effecten toeneemt. Aparte metingen van motorische geëvokeerde potentialen (EMG‑reacties in gezicht‑ en ledemaatspieren) en somatosensorische geëvokeerde potentialen (EEG‑patronen gerelateerd aan tastbanen) kunnen subtiele activatie van de interne capsule of het mediale lemniscus blootleggen—vezelbundels die motorische commando’s en sensorische informatie geleiden. Het vroeg detecteren van deze veranderingen stelt clinici in staat de stroom weg te sturen van risicovolle gebieden door andere contacten te kiezen of pulsvorm en polariteit aan te passen.
De labinstrumenten praktisch toepasbaar maken in de kliniek
Het omzetten van deze inzichten naar routinezorg vereist praktische oplossingen. Het overzicht legt uit hoe standaard ziekenhuis‑EEG‑ en EMG‑systemen al het grootste deel van de benodigde signalen kunnen opnemen, mits ze hoge bemonsteringsfrequenties gebruiken en zorgvuldige methoden hanteren om elektrische "ruis" van de DBS‑pulsen te verwijderen. De auteurs bespreken strategieën om artefacten te verminderen, zoals slimme her‑referenties, sjabloon‑substractie en geavanceerde computeralgoritmen die ware hersenactiviteit scheiden van stimulatie‑resten. Ze bepleiten dat korte, gestructureerde testsessies—die korte periodes van lage frequentie DBS, scalp‑opnames en spiermonitoring tijdens rust en lichte contractie combineren—kunnen worden ingepast in de gebruikelijke programmeerweek na chirurgie. Geëvokeerde‑potentiaalkaarten van elk contact kunnen dan gecombineerd worden met beeldvorming en andere biomarkers om te sturen welke contacten en instellingen op lange termijn te gebruiken.
Wat dit betekent voor mensen met Parkinson
Het artikel besluit dat geëvokeerde potentialen veelbelovende kandidaten zijn om DBS‑programmering preciezer, efficiënter en voorspelbaarder te maken. In het bijzonder lijkt de kort‑latente P3‑golf een sterk merkteken dat stimulatie het juiste circuit raakt om Parkinsonse motorische symptomen te verlichten, terwijl motorische en sensorische geëvokeerde reacties kunnen waarschuwen wanneer stroom lekt naar banen die bijwerkingen veroorzaken. Hoewel meer werk nodig is om technieken te standaardiseren en voordelen in de dagelijkse praktijk te bewijzen, streeft deze benadering naar een toekomst waarin artsen tijdens het programmeren naar de hersenen kunnen "luisteren", snel het sweet spot van elke patiënt kunnen vinden en de trial‑en‑error‑last voor mensen die met de ziekte van Parkinson leven kunnen verminderen.
Bronvermelding: Hale, B., Latorre, A., Rocchi, L. et al. Clinical utility of evoked potentials for programming subthalamic deep brain stimulation in Parkinsons disease. npj Parkinsons Dis. 12, 54 (2026). https://doi.org/10.1038/s41531-026-01274-2
Trefwoorden: Ziekte van Parkinson, diepe hersenstimulatie, geëvokeerde potentialen, hersenmapping, neurofysiologie