Clear Sky Science · nl
UQCRC1-tekort verstoort mitofagie via PINK1-afhankelijke mechanismen bij de ziekte van Parkinson
Waarom dit onderzoek ertoe doet voor gewone mensen
De ziekte van Parkinson staat vooral bekend om bewegingsproblemen—tremor, stijfheid en traagheid—but achter die symptomen worstelen hersencellen met het produceren en opruimen van energie. Deze studie onderzoekt hoe een weinig bekend eiwit, UQCRC1, hersencellen helpt hun “energiecentrales” gezond te houden, en hoe het falen ervan de deur naar Parkinson kan openen. Inzicht in deze verborgen machinerie kan richting geven aan behandelingen die de ziekte vertragen of zelfs voorkomen, in plaats van alleen de symptomen te verzachten.
Een energieprobleem binnen hersencellen
Onze hersencellen zijn afhankelijk van mitochondriën, kleine structuren vaak omschreven als cellulaire energiecentrales, om de energie te produceren die ze nodig hebben. UQCRC1 is een essentieel onderdeel van een van de mitochondriale motoren die dit werk verrichten. Eerder werk toonde dat zeldzame erfelijke mutaties in UQCRC1 een Parkinson-achtig beeld kunnen veroorzaken door deze motoren te belasten. In deze studie stelden de auteurs een bredere vraag: speelt verminderde UQCRC1 ook een rol in de veel voorkomende, niet-erfelijke (“idiopathische”) vormen van Parkinson?
Een gemeenschappelijk signaal vinden in patiëntengegevens
Om dit te beantwoorden, voegden de onderzoekers 19 openbaar beschikbare datasets samen van hersenweefsel van mensen die wel of niet aan Parkinson waren overleden. Ze concentreerden zich op de substantia nigra, het diepe hersengebied waarvan de dopamine-producerende zenuwcellen bij Parkinson degenereren. Over 150 controlegevallen en 185 Parkinson- of verwante gevallen vonden ze consequent lagere niveaus van UQCRC1-genactiviteit in Parkinson-hersenen—ongeveer 20% reductie gemiddeld, met weinig aanwijzing dat het resultaat door toeval of publicatiebias verklaard kon worden. Ze bevestigden dit door UQCRC1-eiwit te meten in hersenmonsters uit twee onafhankelijke bronnen en in humane zenuwachtige cellen met een ziektegerelateerde UQCRC1-mutatie; in elk geval waren de UQCRC1-niveaus duidelijk lager bij de Parkinson-conditie. 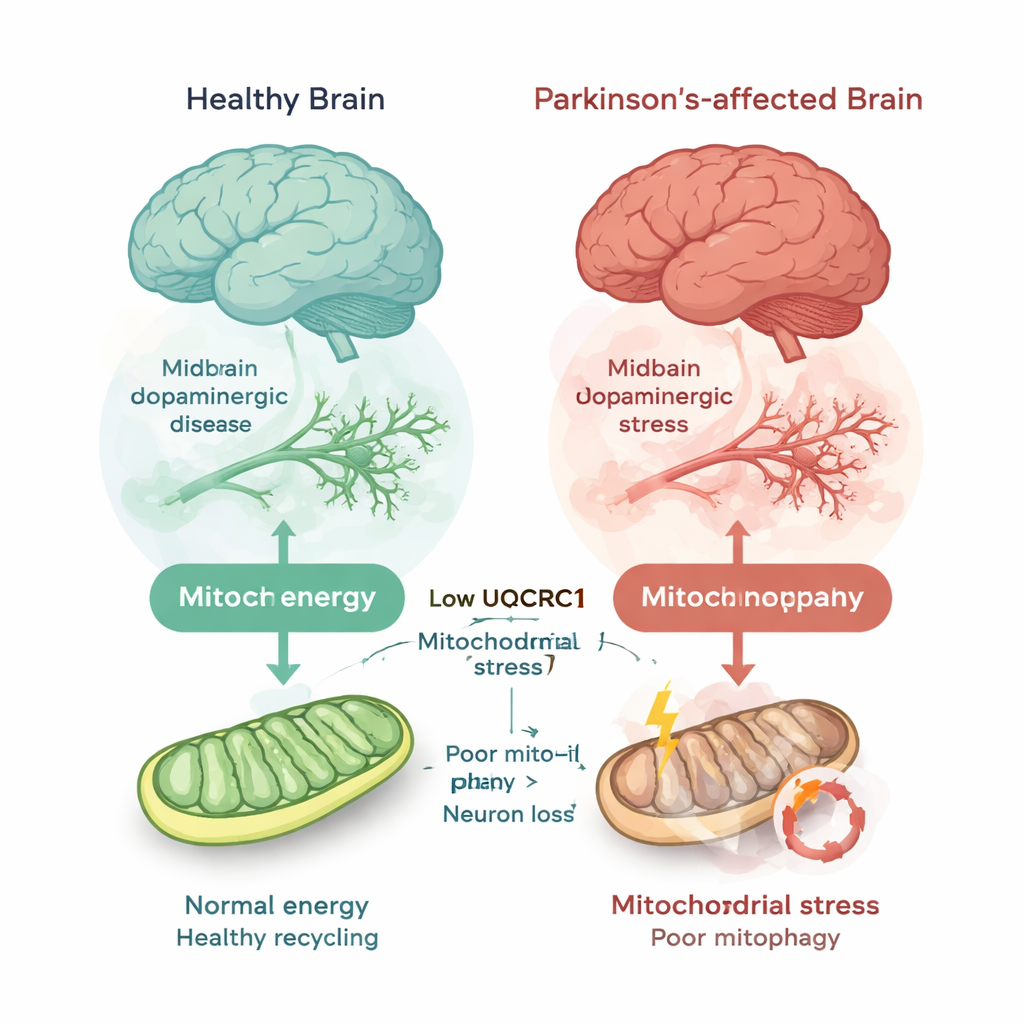
Wanneer opruimploegen falen
Mitochondriën maken niet alleen energie; ze hebben ook regelmatige inspectie en verwijdering nodig wanneer ze beschadigd raken. Cellen gebruiken een kwaliteitcontrolemecanisme genaamd mitofagie om versleten mitochondriën te markeren en naar een recyclecompartiment te sturen. Het team gebruikte fluorescerende reporters in menselijke cellen en fruitvliegen om dit proces in actie te volgen. Onder stress die normaal mitofagie activeert, maakten cellen met UQCRC1-mutaties of verlaagd UQCRC1 veel minder “mitolysosomen,” de structuren die succesvolle verwijdering van beschadigde mitochondriën aangeven. In dopaminecellen van fruitvliegen leidde vermindering van UQCRC1 eveneens tot minder gerecyclede mitochondriën, wat de defecten weerspiegelde die optreden wanneer een kern-gen voor autofagie werd geblokkeerd. Deze bevindingen tonen aan dat verlies van UQCRC1 niet alleen de energieproductie verzwakt—het verstoort ook het opruimen van defecte energiecentrales.
Een ontbrekende schakel en een veelbelovend doel
De onderzoekers richtten zich vervolgens op PINK1, een eiwit dat fungeert als sensor en schakelaar voor mitofagie. Wanneer mitochondriën onder stress staan, hoopt PINK1 zich op hun oppervlak op, werft het een ander eiwit genaamd Parkin en zet het het labelproces in gang dat naar recycling leidt. Meta-analyse van patiëntgegevens uit de hersenen toonde aan dat PINK1, maar niet Parkin, ook verlaagd was in de middenhersenen van Parkinsonpatiënten, met ongeveer 22%. In zowel menselijke cellen als vliegen met UQCRC1-problemen daalden de PINK1-niveaus, en vroege stappen van het PINK1–Parkin-pad—Parkin die naar mitochondriën verhuist en ze markeert—waren afgezwakt. Opvallend was dat het versterken van PINK1 in vliegen hun klimvaardigheid herstelde en de mitofagie normaliseerde, wat suggereert dat het terugdraaien van deze schakel kan compenseren voor UQCRC1-verlies. 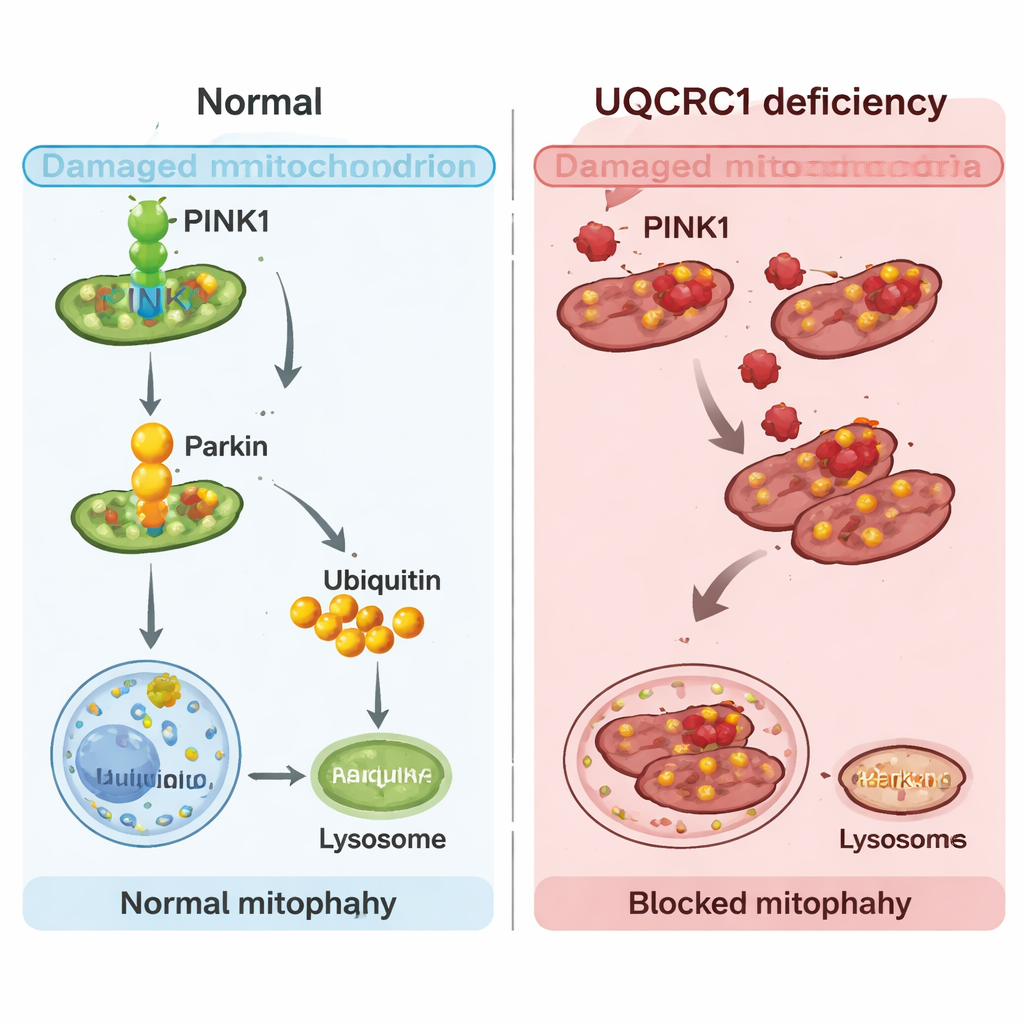
Testen van geneesmiddelachtige activatoren van het opruimpad
Aangezien het rechtstreeks toevoegen van PINK1 bij patiënten niet praktisch is, testte het team kleine moleculen waarvan bekend is dat ze PINK1-activiteit versterken: kinetin en MTK458. In fruitvliegen met UQCRC1-tekort verbeterde het voeren van deze verbindingen de beweging en beschermde ze kwetsbare dopaminecellen. In humane zenuwachtige cellen met verlaagd UQCRC1 verlengde MTK458 verschrompelde uitlopers en herstelde defecte mitofagie. Deze voordelen waren afhankelijk van PINK1, wat de gedachte ondersteunt dat gerichte activatie van dit pad cellen kan helpen omgaan met mitochondriale stress veroorzaakt door laag UQCRC1.
Wat dit kan betekenen voor toekomstige behandelingen van Parkinson
Al met al koppelt de studie een daling van UQCRC1 aan een kettingreactie: gestreste mitochondriën, zwakkere PINK1-gedreven opruiming en uiteindelijk verlies van dopaminerge neuronen. Voor een leek betekent dit dat sommige gevallen van Parkinson kunnen voortkomen uit energiecentrales die niet alleen slecht functioneren maar ook opstapelen als afval dat de cel niet kan opruimen. Hoewel meer onderzoek nodig is om elke stap in kaart te brengen en de veiligheid bij mensen te testen, benadrukken de resultaten PINK1-activatoren als potentiële precisiegeneesmiddelen voor patiënten van wie de Parkinson wordt gekenmerkt door mitochondriale defecten zoals UQCRC1-tekort. In plaats van alleen symptomen te maskeren, zouden zulke behandelingen erop gericht zijn het vermogen van de cel om haar energiecentrales te onderhouden en te vernieuwen te herstellen.
Bronvermelding: Li, JL., Huang, SY., Huang, PY. et al. UQCRC1 deficiency impairs mitophagy via PINK1-dependent mechanisms in Parkinson’s disease. npj Parkinsons Dis. 12, 48 (2026). https://doi.org/10.1038/s41531-026-01262-6
Trefwoorden: Ziekte van Parkinson, mitochondriën, mitofagie, PINK1, UQCRC1