Clear Sky Science · nl
Remming van putcorrosie in roestvrij staal door NaNO3: mechanistische inzichten in sulfideoplossing, depassivering en actieve oplossing
Waarom kleine roestplekjes ertoe doen
Van bruggen en wolkenkrabbers tot auto’s en chemische installaties: roestvrij staal wordt gekozen omdat het doorgaans bestand is tegen roest. Toch kan het onder bepaalde omstandigheden plotseling kleine, diepe gaatjes ontwikkelen die putten worden genoemd en uitgroeien tot gevaarlijke scheuren. Deze studie stelt een praktische vraag voor de industrie: kan een veelgebruikt, relatief veilig chemisch middel — natriumnitraat — voorkomen dat die putten ooit ontstaan, en zo ja, hoe werkt dat? Het antwoord kan helpen om kritieke infrastructuur langer veilig te houden met additieven die betaalbaar zijn en minder schadelijk voor het milieu. 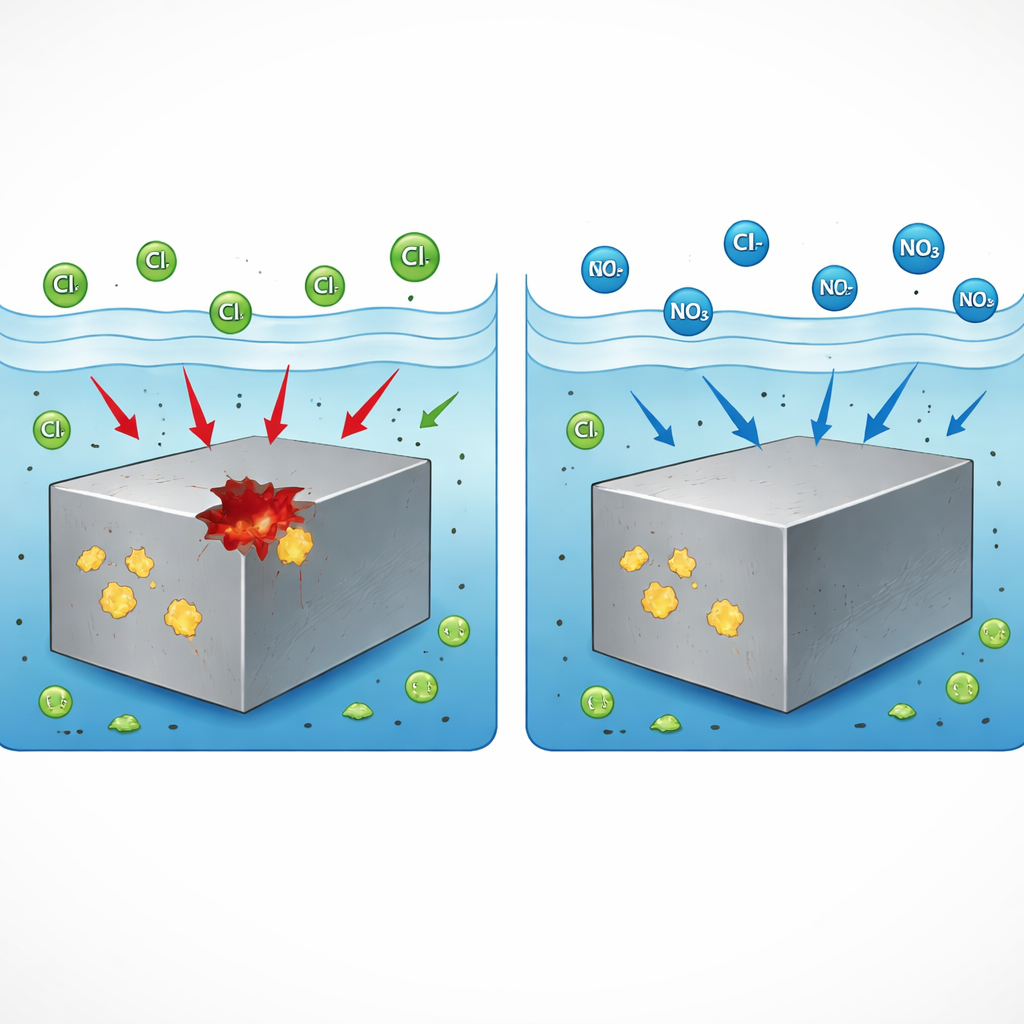
Verborgen zwakke plekken in roestvrij staal
Zelfs de beste roestvaste staalsoorten zijn niet volledig uniform. Verspreid binnenin bevinden zich microscopische deeltjes rijk aan zwavel, bekend als sulfideinsluitingen. Twee belangrijke typen zijn gebaseerd op mangaan (MnS) en calcium (CaS). Deze insluitingen functioneren als ingebouwde zwakke plekken waar putten bij voorkeur beginnen wanneer chloridehoudend water, zoals zoutnevel of koelwater, het metaal raakt. Eerder werk liet zien dat putvorming een consistent volgorde volgt: het sulfidedeeltje begint op te lossen, de beschermende film op het omliggende staal faalt en vervolgens begint het omringende metaal snel op te lossen en een put uit te graven. De huidige studie vergelijkt twee commerciële Type 304 roestvrijstalen — één gedomineerd door MnS‑insluitingen en één door CaS‑gebaseerde insluitingen — om te begrijpen of nitraat dit patroon bij een of beide types zwakke plekken kan doorbreken.
Testen van gangbare additieven in zout water
De onderzoekers dompelden de stalen onder in een eenvoudige zoutoplossing en dwongen het metaal geleidelijk naar meer corrosieve omstandigheden terwijl ze observeerden wanneer stabiele putten zich vormden. Ze vergeleken drie additieven in realistische concentraties: ammonium, nitriet en nitraat, telkens als natrium‑ of ammoniumzouten. Alleen nitraat had een opvallend effect. In zowel het MnS‑rijke als het CaS‑rijke staal voorkwam het toevoegen van een bescheiden hoeveelheid natriumnitraat volledig dat er stabiele putten ontstonden binnen het geteste bereik, terwijl de andere twee additieven geen verbetering lieten zien. Microscopie bevestigde dat zonder nitraat putten inderdaad begonnen bij sulfideinsluitingen, terwijl bij nitraat die insluitingen geen schadelijke gaten meer veroorzaakten. Dit toonde aan dat nitraat een breed effectief putremmend middel is voor verschillende sulfide‑typen, en geen bijzonder geval.
Nauw kijken naar wat nitraat wél en niet verandert
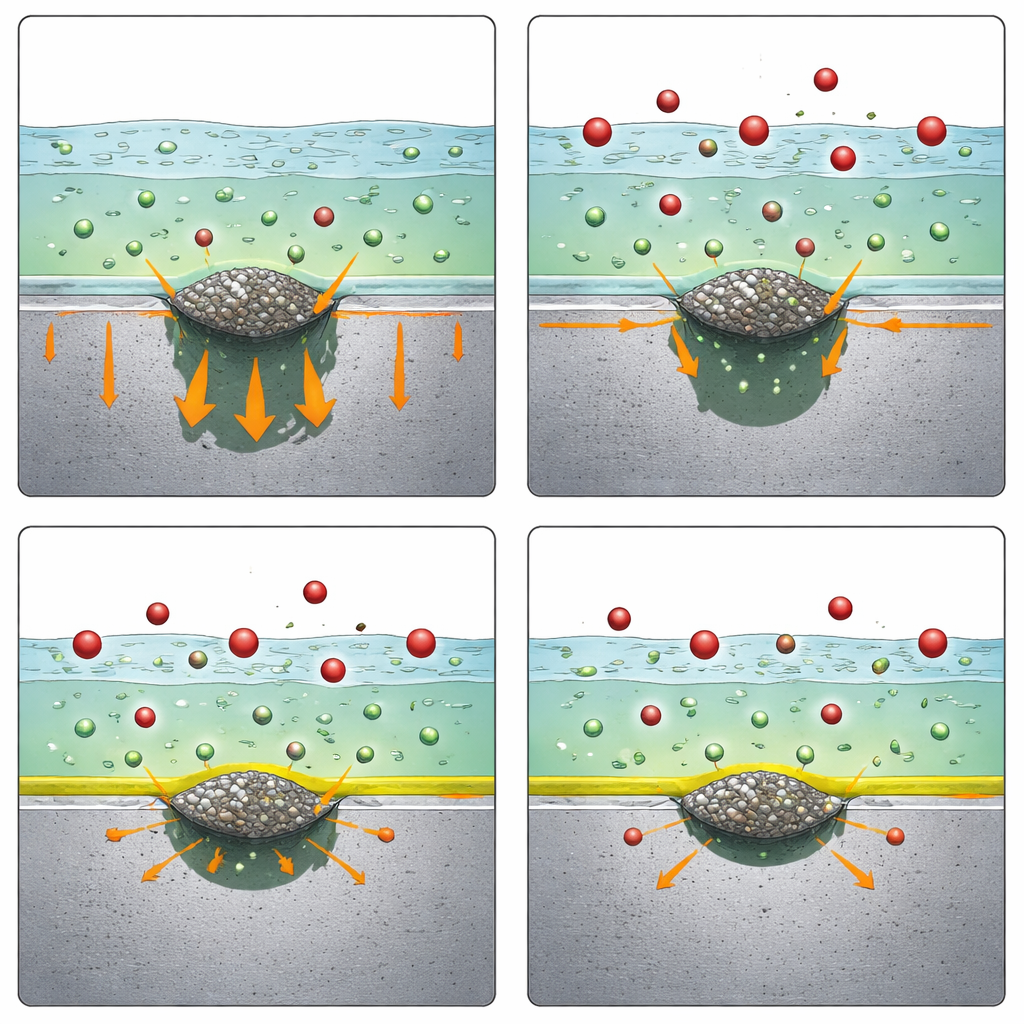
Om vast te stellen hoe nitraat werkt, zoomde het team in op de vroege stadia van putvorming rond individuele MnS‑deeltjes met behulp van kleine elektroden en hoog‑resolutie beeldvorming. Ze observeerden dat nitraat niet verhinderde dat de MnS‑deeltjes zelf oplosten, noch dat het de kleine sleuven veranderde die ontstaan waar de insluiting het omliggende staal raakt. Nitraat veranderde ook niet het zuurgraadniveau waarbij de beschermende film van het staal in chlorideoplossing faalt. Dit alles wees erop dat de eerste stappen van pitinitiëring — verzwakking en verstoring rond de insluiting — nog grotendeels op dezelfde manier verlopen in aanwezigheid van nitraat.
Het vertragen van de laatste uitbarsting van metaalverlies
Het cruciale verschil trad op wanneer de onderzoekers de zware omgeving binnen een eenmaal gevormde put nabootsten: zeer zuur en chloride‑rijk. Met sterke zure oplossingen die de chemie diep in putten nabootsen, vonden ze dat het staal normaal gesproken twee duidelijke pieken van snelle metaaloplossing laat zien wanneer de spanning wordt verhoogd. Het toevoegen van nitraat verminderde consequent de eerste piek in oplossing, zowel in simpele zuren als in zuren die ook zwavelhoudende soorten bevatten vergelijkbaar met die vrijkomen bij de oplossing van MnS. Oppervlaktewaarnemingen toonden een uniforme aantasting maar met een duidelijk lagere snelheid. Aanvullende tests, waarbij zuurgraad en chloridegehalte werden gevarieerd, suggereerden dat het effect van nitraat niet eenvoudigweg kon worden verklaard door verdunning van zuurtegraad, verdringing van chloride of stabilisatie van zoutkristallen. In plaats daarvan wezen de resultaten erop dat nitraat helpt dat chroom in de legering een stabiliserende oppervlaktelaag vormt, wat op zijn beurt de vroege, meest kritische fase van actief metaalverlies vertraagt.
Wat dit betekent voor stalen in de praktijk
Kort gezegd: nitraat voorkomt niet de eerste chemische aantastingen van kleine sulfidedeeltjes in roestvrij staal, maar het vertraagt wel de laatste, ongeremde fase waarin een onschadelijke imperfectie verandert in een gevaarlijke put. Door die uitbarsting van metaalverlies in zure, zoute micro‑omgevingen te dempen, houdt natriumnitraat het staal dichter bij een passieve, zichzelf beschermende toestand, zelfs wanneer sulfideinsluitingen en chloride‑ionen aanwezig zijn. Omdat nitraat relatief goedkoop is, minder toxisch dan veel alternatieven en al wordt gebruikt in industriële watersystemen, versterkt het begrip van dit mechanisme het argument voor het zorgvuldige gebruik ervan als additief voor corrosiebeheersing om de levensduur van roestvrijstalen constructies en apparatuur te verlengen.
Bronvermelding: Amatsuka, S., Nishimoto, M. & Muto, I. Pitting-corrosion inhibition in stainless steel by NaNO3: mechanistic insights on sulfide dissolution, depassivation, and active dissolution. npj Mater Degrad 10, 40 (2026). https://doi.org/10.1038/s41529-026-00753-4
Trefwoorden: corrosie van roestvrij staal, remming van putvorming, natriumnitraat, sulfideinsluitingen, chlorideoplossingen