Clear Sky Science · nl
Effect van elektrochemische waterbehandelingsprocessen op corrosie van koolstofstaal in stedelijke watervoorzieningssystemen
Waarom uw drinkwaterleidingen ertoe doen
Elektrochemische waterbehandelingssystemen worden in steden steeds vaker toegepast omdat ze efficiënt verontreinigingen verwijderen, water verzachten en micro-organismen doden. Maar dezelfde elektrische reacties die het water reinigen, kunnen ook onopgemerkt het metaal van de leidingen aantasten die dat water naar onze huizen vervoeren. Deze studie onderzoekt hoe zulke behandeling koolstofstaal — een veelgebruikt leidingmateriaal — beïnvloedt en legt uit waarom corrosie sterk kan versnellen wanneer elektrische processen en de normale samenstelling van kraanwater samenkomen.
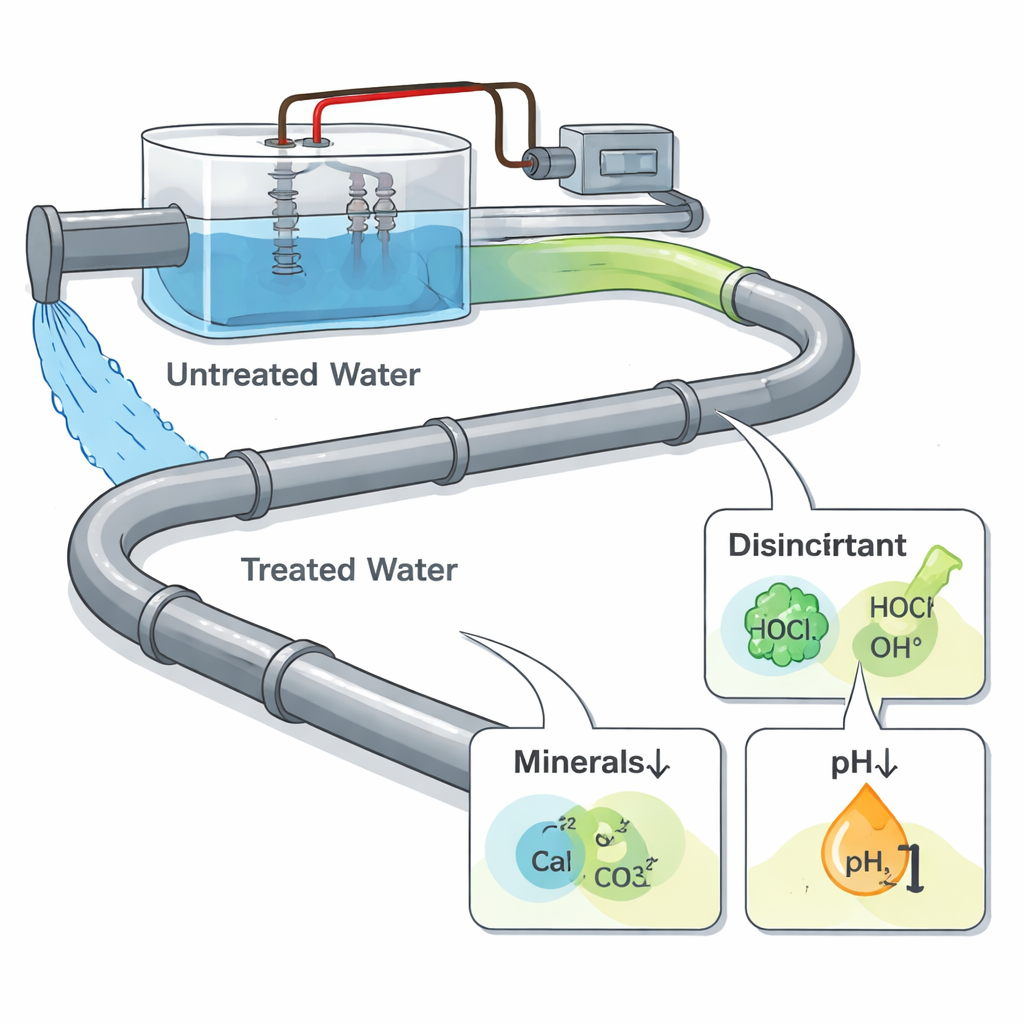
Water reinigen met elektriciteit
Bij elektrochemische waterbehandeling wordt een elektrische stroom door water geleid met behulp van metalen platen, elektroden genaamd. Dit kan ongewenste ionen verwijderen, organische vervuiling afbreken en desinfecterende stoffen genereren, waardoor het proces aantrekkelijk is voor stedelijke en industriële systemen. In tegenstelling tot traditionele behandelingen zijn de leidingen echter niet elektrisch aangesloten op het behandelingssysteem — ze krijgen alleen het water dat uit het apparaat komt. Dat betekent dat extra corrosie niet wordt veroorzaakt doordat elektriciteit direct de leiding raakt, maar door veranderingen in de waterchemie: nieuwe oxiderende chemicaliën voor desinfectie, verschuivingen in zuurgraad en verplaatsing van mineraalionen die normaal gesproken helpen beschermende lagen in leidingen te vormen.
Sneller metaalverlies en diepere verborgen schade
De onderzoekers voerden een experiment van 90 dagen uit met echt stadswater, waarbij koolstofstaalmonsters werden blootgesteld aan verschillende spanningen van 0 tot 9 volt, waarna gewichtsverlies, oppervlaktebeschadiging en elektochemisch gedrag werden gevolgd. Ze ontdekten dat al binnen de eerste drie dagen het inschakelen van elektrolyse de corrosie verergerde, en dat hogere spanning altijd meer schade betekende. Bij 9 volt steeg de algemene corrosiesnelheid meer dan 25 keer vergeleken met water dat niet door het elektrische proces was gegaan. Met 3D-oppervlakte-scans lieten ze ook zien dat kleine putjes in het metaal veel dieper werden naarmate de spanning toenam. Bij de hoogste spanning waren de diepste putten bijna vijf keer dieper dan in onbehandeld water, wat de verwachte levensduur van het staal scherp verkort, zelfs als het gemiddelde metaalverlies niet extreem leek.
Waarom beschermende lagen falen
In veel waterleidingen bouwen mineralen uit het water van nature een dunne, dichte laag op die helpt het metaal te beschermen. In onbehandeld water speelt calciumcarbonaat vaak die beschermende rol. In het elektrochemisch behandelde water verdwijnt die minerale bescherming echter grotendeels. Omdat de kathode in de behandelunit calcium- en carbonaationen aantrekt en aanzet tot afzetting daar, blijven er minder van deze ionen over om een stevige beschermlaag op de leidingwanden te vormen. Microscopie- en diffractieonderzoek toonde aan dat het staal in behandeld water in plaats van een dichte mineraalrijke barrière een losse, poreuze roestlaag met kleine, instabiele kristallen ontwikkelde. Deze zwakke bekleding liet corrosieve stoffen en elektronen gemakkelijk passeren, zodat corrosie snel bleef verlopen in plaats van in de loop van de tijd af te nemen.
Een sterkere chemische aanval in het water
Om te achterhalen wat de extra aanval veroorzaakte, scheidde het team verschillende factoren. Toen ze elektrolyse uitvoerden in een sulfaatoplossing zonder chloride, veranderden de bijproducten van het splitsen van water — zoals zuurstof, waterstof en kortlevende radicalen — de corrosiegedraging van het staal nauwelijks. Maar wanneer chloride aanwezig was, hetzelfde ion dat voorkomt in gewone zouten en in veel waterbronnen, veranderde het beeld. Elektrolyse zette een deel van het chloride om in hypochloriet, een reactiever desinfectiemiddel. Elektochemische tests toonden aan dat naarmate de stroom toenam, staal in chlorideoplossingen veel gemakkelijker te corrodereerde was. Computersimulaties bevestigden dit: hypochloriet verlaagde de energiebarrière voor ijzeratomen om het metaaloppervlak te verlaten, waardoor corrosie makkelijker verliep dan bij alleen chloride. Tegelijkertijd verbruikte de snelle vorming van roestproducten hydroxide-ionen, waardoor het water een lagere pH kreeg — meer zure omstandigheden — wat corrosie verder bevorderde.
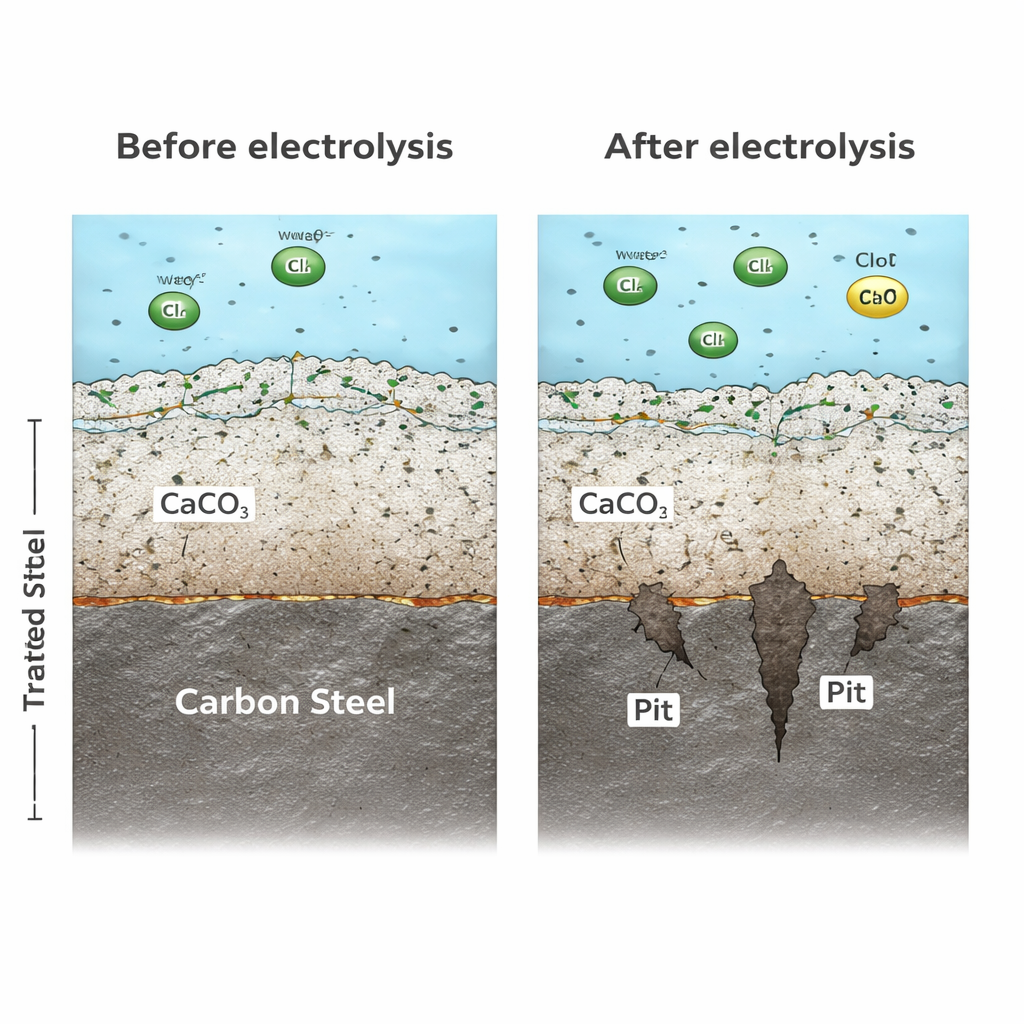
Wat dit betekent voor watersystemen
Voor niet-specialisten is de conclusie dat het reinigen en desinfecteren van water met elektriciteit niet automatisch mild is voor de leidingen die dat water transporteren. In systemen waar het water chloride bevat, kan elektrochemische behandeling een deel van dat chloride omzetten in een sterker, meer corrosief desinfectiemiddel en tegelijkertijd de minerale ingrediënten onttrekken die nodig zijn om natuurlijke bescherming op te bouwen. Het resultaat is snellere metaalafname en diepere putten die de levensduur van leidingen kunnen verkorten en het risico op lekken of besmetting kunnen vergroten. De auteurs adviseren ontwerpers en beheerders van dergelijke systemen om corrosie als een centraal ontwerpprobleem te beschouwen — door spanning te beperken, chloride vóór behandeling te verminderen, elektroden te kiezen die minder agressieve bijproducten vormen, en op lange termijn putvorming en waterchemie te monitoren — om ervoor te zorgen dat schoner water niet ten koste gaat van falende infrastructuur.
Bronvermelding: Zhao, S., Jing, Y., He, X. et al. Effect of electrochemical water treatment processes on carbon steel corrosion in urban water supply system. npj Mater Degrad 10, 23 (2026). https://doi.org/10.1038/s41529-026-00736-5
Trefwoorden: elektrochemische waterbehandeling, corrosie van koolstofstaal, stedelijke waterleidingen, chloride en hypochloriet, duurzaamheid van waterinfrastructuur