Clear Sky Science · nl
Flexibele ferro-elektrische biomaterialen voor herstel van huid-, zenuw- en bewegingsweefsel
Slimme materialen die het lichaam helpen zichzelf te genezen
Als we een bot breken, een pees scheuren, een zenuw beschadigen of een hardnekkige huidswond krijgen, kunnen artsen vaak de blessure stabiliseren — maar het volledig laten herbouwen van gezond weefsel blijft lastig. Dit artikel verkent een nieuwe klasse van "slimme" materialen die meebewegen met ons lichaam en alledaagse bewegingen omzetten in kleine elektrische signalen. Die signalen bootsen de eigen bio-elektrische taal van het lichaam na en kunnen cellen zachtjes aansporen om te groeien, zich te herschikken en beschadigd huid-, zenuw-, spier-, kraakbeen- en botweefsel te herstellen.
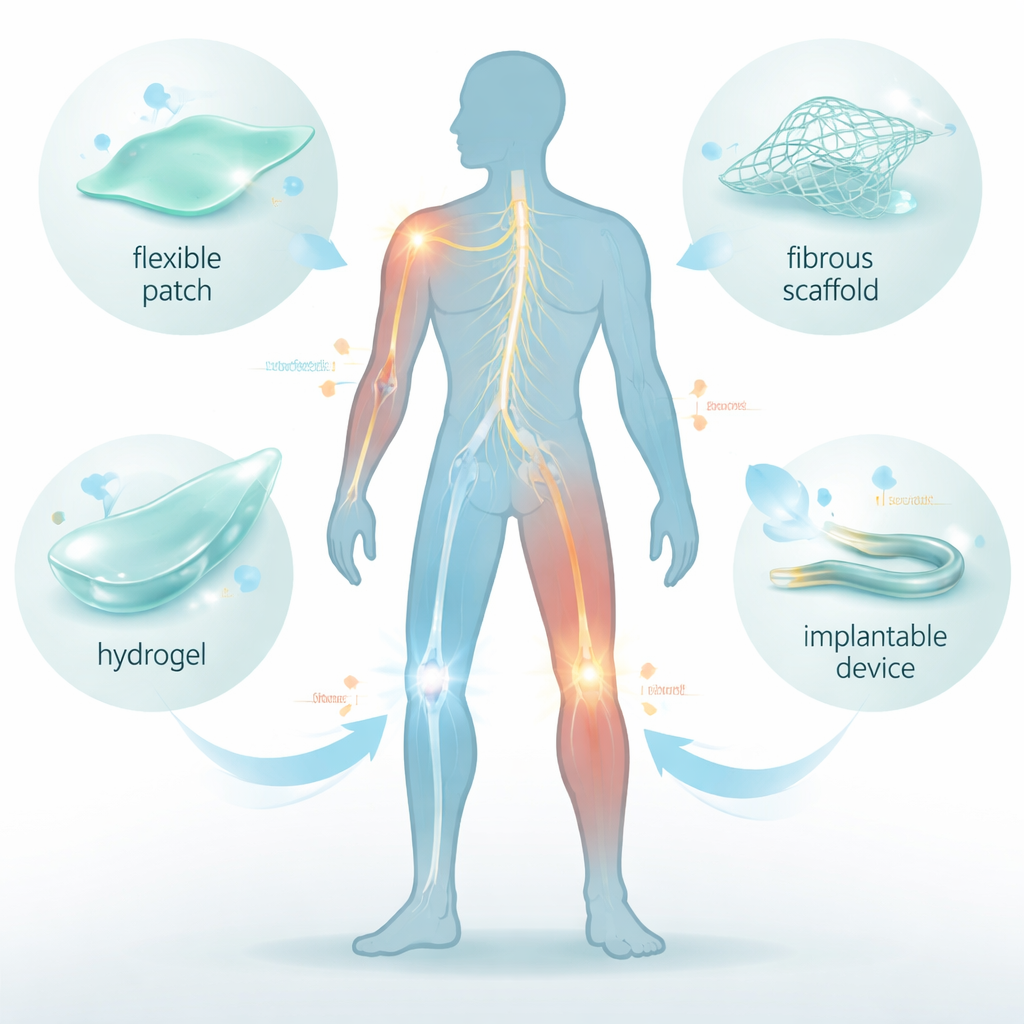
Waarom elektriciteit belangrijk is voor genezing
Elk levend weefsel draagt subtiele elektrische patronen. Zenuwen vuren spanningspulsen af, botten genereren kleine ladingen als we lopen, en de huid vormt natuurlijke elektrische velden rond wonden. Deze signalen sturen cellen — ze geven aan wanneer cellen moeten bewegen, delen en specialiseren. Verwonding of chronische ontsteking kan dit elektrische landschap verstoren, waardoor herstel vertraagt of verkeerd wordt geleid. De review verklaart hoe flexibele ferro-elektrische biomaterialen zijn ontworpen om deze signalen te herstellen of te versterken. Ze reageren op buigen, rekken of temperatuurveranderingen door kleine, gelokaliseerde spanningen te produceren en vertalen mechanische beweging in de elektrische "genezingsaanwijzingen" van het lichaam.
Waar deze slimme materialen van gemaakt zijn
De auteurs richten zich op verschillende families ferro-elektrische materialen die zacht en lichaamsvriendelijk gemaakt kunnen worden. Polymeren zoals PVDF, het copolymeer P(VDF-TrFE) en PLLA zijn kunststoffen die, mits correct verwerkt, werken als miniatuurgeneratoren: beweging veroorzaakt lading. Keramische deeltjes zoals bariumtitanaat (BaTiO₃), bismutferraat (BiFeO₃) en kalium-natriumniobaat (KNN) bieden sterke elektrische respons maar zijn op zichzelf bros, dus worden ze gemengd in flexibele polymeren. Door kristalstructuur, vezeluitlijning en porositeit te optimaliseren, kunnen onderzoekers dunne folies, nanovezelmatten, 3D-geprinte steigers en injecteerbare hydrogels maken die zich naar gebogen lichaamsoppervlakken vormen en daarbij biologisch relevante niveaus van elektrische stimulatie produceren.
Hoe bewegingsgedreven signalen met cellen communiceren
Wanneer deze materialen worden ingedrukt, uitgerekt of gepulseerd met ultrasone golven, leveren ze kleine elektrische pulsen aan nabijgelegen cellen. In het celmembraan bevinden zich ionkanalen die openen als reactie op elektrische of mechanische prikkels, waardoor calciumionen binnenstromen. Die korte calciumpiek fungeert als een hoofdschakelaar die netwerken activeert die celoverleving, migratie, groei en differentiatie in bot-, kraakbeen-, zenuw- of spiercellen regelen. Elektrische signalen herschikken ook oppervlaktereceptoren, beïnvloeden hoe cellen zich aan hun omgeving hechten, veranderen het energiegebruik in mitochondriën en sturen immuuncellen weg van aanhoudende ontsteking naar pro-herstellend gedrag. Op die manier kan een eenvoudige beweging — zoals lopen na een operatie — via deze materialen worden omgezet in betekenisvolle biologische instructies.
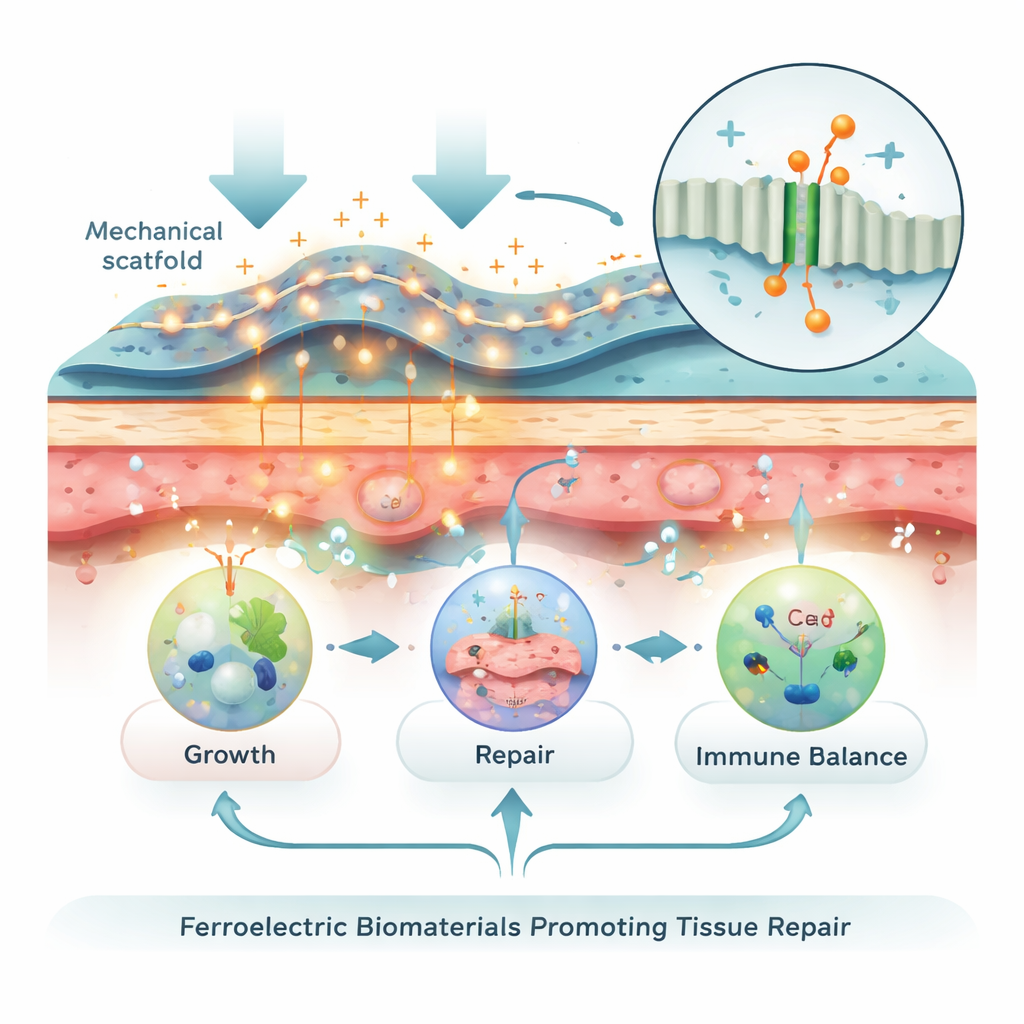
Toepassingen in bot, zenuwen, huid en meer
De review geeft een overzicht van snelle vooruitgang in veel weefsels. In bot en kraakbeen genereren ferro-elektrische steigers en hydrogels, aangebracht in defecten, kleine spanningen bij normale gewrichtsbeweging of gerichte ultrasone stimulatie, wat de activiteit van botvormende genen verhoogt en hoogwaardige kraakbeengroei stimuleert. In perifere zenuwen begeleiden flexibele kanalen gemaakt van piezo-elektrische vezels herinnende axonen en bieden ze, wanneer geactiveerd door beweging of geluidsgolven, zachte, continue stimulatie vergelijkbaar met zenuwsamentrekkingen. Voor de huid versterken zelfvoorzienende verbanden en 3D-geprinte pleisters de eigen wondstroom van het lichaam, versnellen ze sluiting, vaatgroei, infectiebestrijding en verminderen ze zelfs littekenvorming. Vergelijkbare strategieën helpen spiervezels uitlijnen en rijpen en ondersteunen sterkere aanhechting van pees aan bot na rotatorcuff- of ligamentblessures.
Van belofte in het lab naar dagelijkse therapieën
Ondanks de opwinding benadrukken de auteurs dat de meeste van deze technologieën nog in vroege dier- of laboratoriumstudies verkeren. Deze complexe, gelaagde materialen betrouwbaar op schaal produceren, ervoor zorgen dat ze sterilizatie en jaren in het lichaam overleven, en hun afbraak afstemmen op het tempo van weefselherstel, zijn open uitdagingen. Sommige veelgebruikte polymeren, zoals PVDF, breken vrijwel niet af in het lichaam, wat vragen oproept over hun langetermijnbestaan. Toekomstig werk zal betere regelsystemen vereisen — mogelijk met AI — om stimulatie in realtime aan te passen, evenals nieuwe ferro-elektrische materialen die zowel effectief als echt biologisch afbreekbaar zijn. Als deze obstakels overwonnen kunnen worden, zouden flexibele ferro-elektrische biomaterialen implantaten, verbanden en zachte elektronische "huiden" mogelijk maken die onze eigen bewegingen oogsten om precieze, gepersonaliseerde reparatie van huid, zenuwen, spieren en het hele bewegingsapparaat aan te sturen.
Bronvermelding: Sheng, N., Wang, Y., Luo, X. et al. Flexible ferroelectric biomaterials for skin, neural, and musculoskeletal tissue repair. npj Flex Electron 10, 29 (2026). https://doi.org/10.1038/s41528-026-00532-w
Trefwoorden: flexibele biomaterialen, elektrische stimulatie, weefselregeneratie, piezo-elektrische polymeren, wondgenezing