Clear Sky Science · nl
Varianten in MTNAP1 liggen ten grondslag aan een neurodegeneratieve aandoening door het verstoren van mitochondriale stabiliteit
Waarom dit verhaal ertoe doet voor de gezondheid van de hersenen
Veel families kennen het verdriet van het zien van een kind dat geleidelijk ontwikkelingsvaardigheden verliest zonder duidelijke diagnose. Deze studie onthult een nieuwe genetische oorzaak van een dergelijke aandoening, en volgt het pad vanaf een enkel fout gen tot beschadigde "energiecentrales" binnen hersencellen en uiteindelijk tot krimpende hersenweefsels. Inzicht in deze keten van gebeurtenissen biedt niet alleen antwoorden voor getroffen families, maar verscherpt ook ons bredere beeld van hoe kwetsbaar de energiesystemen van de hersenen werkelijk zijn.
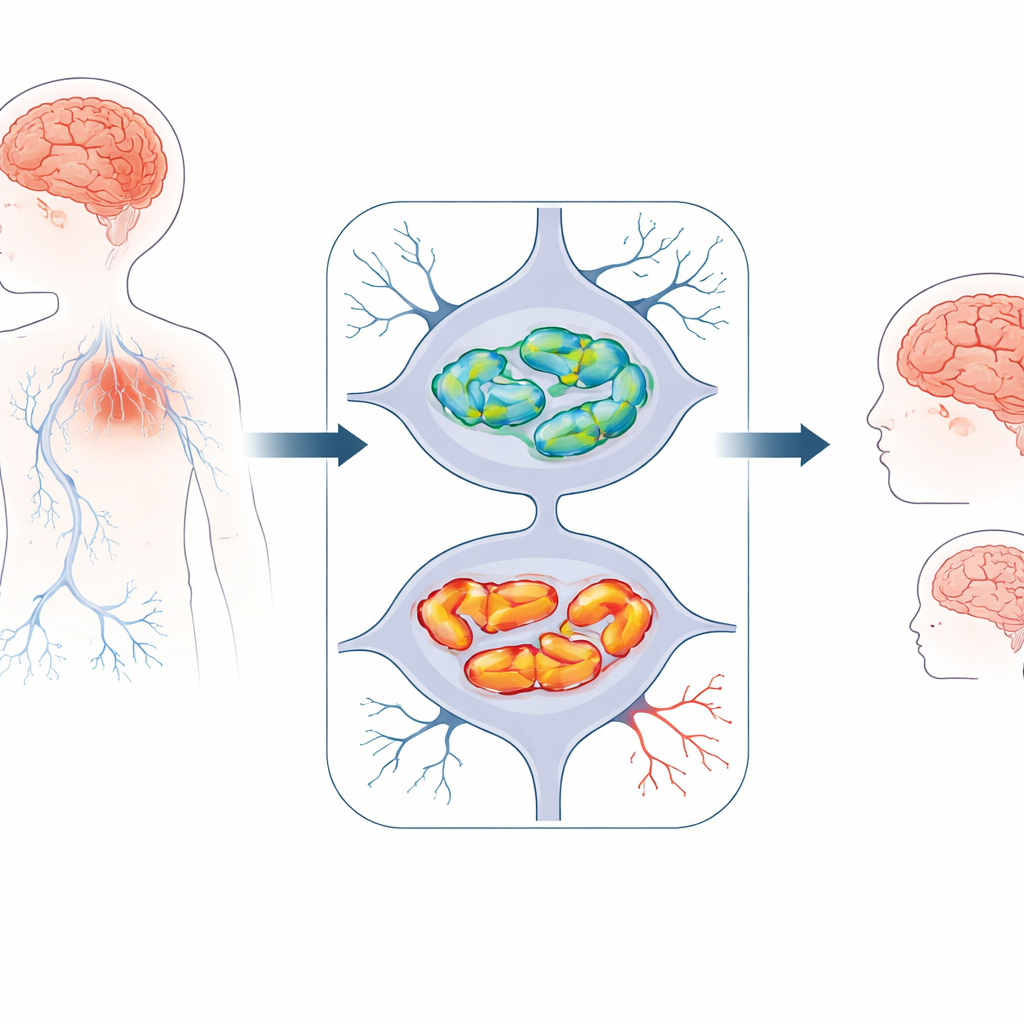
Een recent herkende kinderhersenaandoening
De onderzoekers bestudeerden drie kinderen uit twee niet-verwante families die allen vroegtijdige ontwikkelingsproblemen vertoonden. Ze waren klein voor hun leeftijd, leerden later zitten, lopen en praten dan verwacht, en verloren daarna geleidelijk sommige van deze vaardigheden. Allen ontwikkelden bewegingsproblemen zoals een onstabiele gang, spierstijfheid of lage spiertonus, en aanvallen. Hersenscans lieten een consistent beeld zien: zowel het weefsel van de grote hersenen (cerebrum) als dat van het achterste kleinere gedeelte (cerebellum) werd na verloop van tijd dunner, en een belangrijke verbindingsbrug van zenuwvezels, het corpus callosum, was ongewoon smal. Deze kenmerken wezen op een progressief verlies van zenuwcellen in plaats van een eenmalig letsel bij de geboorte.
Een klein gen met grote gevolgen
Om een erfelijke oorzaak te zoeken, volgde het team de sequentie van alle eiwitcoderende genen van de getroffen kinderen en hun ouders. Ze richtten zich op een gen dat MTNAP1 heet, dat helpt bij het ordenen van het DNA binnen mitochondriën, de energiefabrieken van de cel. Elk kind droeg twee foutieve kopieën van MTNAP1, één van elke gezonde dragerouder. Bij twee broers/zussen verwisselde een enkele "letter" in het gen één bouwsteen van het eiwit voor een andere, waardoor de vorm subtiel werd vervormd. Bij het derde kind veroorzaakte een vroege stopcodon waarschijnlijk dat het eiwit helemaal niet werd aangemaakt. Deze veranderingen werden niet gezien in grote bevolkingsdatabases, wat het argument versterkt dat het zeldzame schadelijke varianten zijn in plaats van onschuldige verschillen.
Energiecentrales onder stress
Vervolgens onderzochten de wetenschappers huidcellen van de kinderen en vergeleken die met cellen van gezonde personen. Onder de microscoop toonden normale cellen lange, draadachtige mitochondriën die een verbonden netwerk vormden, terwijl de cellen van de kinderen korte, gebroken en klonterige mitochondriën bevatten. Toen de onderzoekers experimenteel MTNAP1-niveaus verminderden in een mensachtige zenuwcel-lijn, zagen ze hetzelfde uiteenvallen van het mitochondriale netwerk, wat bevestigt dat het verlies van dit eiwit op zichzelf hun structuur kan verstoren. Metingen van mitochondriale activiteit toonden aan dat sleutelstappen in de energieproductie verzwakt waren en dat de cellen overtollige reactieve zuurstofsoorten produceerden — schadelijke zuurstofafbraakproducten die als moleculair roest werken. De gestreste cellen stopten met correct delen, bleven in een rustfase hangen en schakelden merkers van voortijdige veroudering aan.
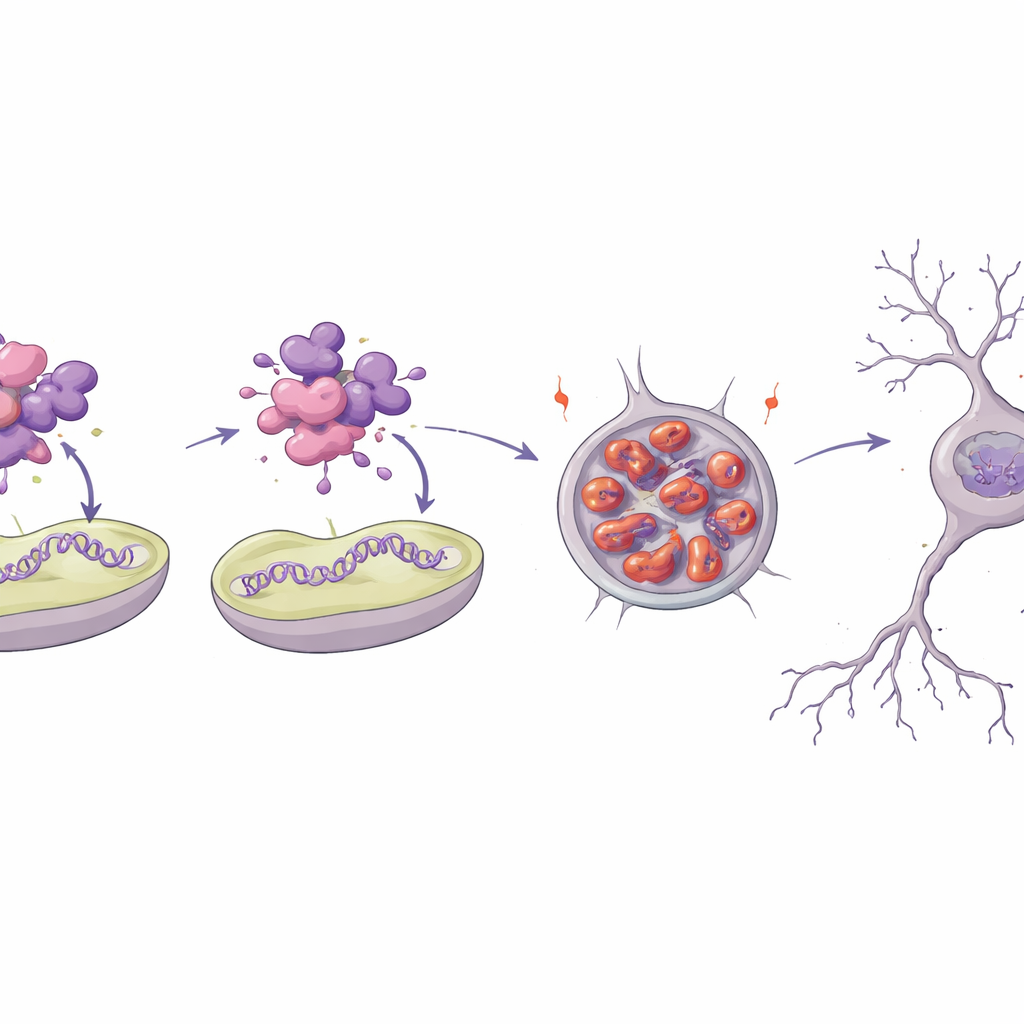
Hoe één wijziging een vitaal eiwit doet ontvouwen
Om te begrijpen waarom één van de varianten zo ontwrichtend is, modelleerde het team de 3D-structuur van het MTNAP1-eiwit en maakte het in het laboratorium na. De vervangen bouwsteen bevindt zich in een dicht verpakte helixregio die normaal helpt het eiwit te laten interageren met mitochondriaal DNA en het binnenmembraan. Computersimulaties en biofysische tests toonden aan dat het mutant-eiwit minder stabiel is, veel van zijn geordende structuur verliest en gemakkelijk klontert. In proefbuisexperimenten bond het normale eiwit sterk aan korte stukjes mitochondriaal DNA en aan kunstmatige membraanoppervlakken, terwijl het mutant nauwelijks interactie aanging en in plaats daarvan amyloïde-achtige aggregaten vormde. Wanneer het in zenuwachtige cellen werd ingebracht, hoopt het mutant zich in de loop van de tijd op in grote perinucleaire klonten, een teken dat de eiwitkwaliteitscontrolesystemen overweldigd raken.
Van beschadigde mitochondriën naar een falende hersenen
Door de stukjes te verbinden schetst de studie een stapsgewijs model: defect MTNAP1 verzwakt het raamwerk dat helpt mitochondriaal DNA te organiseren en het aan het binnenmembraan te verankeren; dit destabiliseert mitochondriën, waardoor ze fragmenteren en hun vermogen om efficiënt energie te produceren verliezen; toenemende oxidatieve stress en cellulair "vroegtijdig verouderen" maken zenuwcellen extra kwetsbaar, omdat zij een hoge en constante energiebehoefte hebben en beperkte capaciteit om zichzelf te vernieuwen. In de ontwikkelende hersenen vertaalt deze langzame, voortdurende energiecrisis zich in stilstaande ontwikkelingsmijlpalen, verlies van aangeleerde vaardigheden en geleidelijke krimp van belangrijke hersengebieden. Hoewel meer patiënten en dierstudies nodig zijn om het syndroom volledig in kaart te brengen, plaatst dit werk MTNAP1 stevig als een cruciale bewaker van mitochondriale stabiliteit en benadrukt het de organisatie van mitochondriaal DNA als een centrale pijler van gezonde hersenontwikkeling.
Bronvermelding: Kumar, A., Saha, S., Nasir, N. et al. Variants in MTNAP1 underlie a neurodegenerative disorder by impairing mitochondrial stability. npj Genom. Med. 11, 19 (2026). https://doi.org/10.1038/s41525-026-00554-3
Trefwoorden: mitochondriën, neurodegeneratie, pediatrische genetica, mitochondriaal DNA, eiwitmisvouwing