Clear Sky Science · nl
Transcriptomische analyse om het mechanisme van radiosensitisatie van AR-positieve triple-negatieve borstkankers met AR-remming te achterhalen
Waarom deze studie ertoe doet voor mensen met borstkanker
Bestralingstherapie is een pijler van de behandeling voor veel mensen met agressieve borstkankers, maar sommige tumoren zijn van nature moeilijker met bestraling te doden dan andere. Deze studie stelt een praktische vraag met reële klinische belangen: kunnen een klasse geneesmiddelen die mannelijke hormoonsignalen blokkeren, al gebruikt bij prostaatkanker, een subgroep van triple-negatieve borstkankers kwetsbaarder maken voor bestraling — en waarom werkt dit in sommige gevallen wel en in andere niet?
Een moeilijk te behandelen vorm van borstkanker
Triple-negatieve borstkankers missen drie veelvoorkomende moleculaire doelwitten — oestrogeenreceptoren, progesteronreceptoren en HER2 — zodat patiënten vaak afhankelijk zijn van chirurgie, chemotherapie en bestraling alleen. Een deel van deze tumoren draagt echter wel de androgeenreceptor, een eiwit dat reageert op hormonen vergelijkbaar met testosteron en tumorgroei kan stimuleren. Eerder onderzoek toonde aan dat het blokkeren van deze receptor deze kankers kan vertragen en mogelijk de effecten van bestraling kan versterken, maar de details van hoe dat gebeurt en welke geneesmiddelen en tumoren het meest profiteren, waren onduidelijk.
Testen van moderne hormoonblokkers met bestraling
De onderzoekers bestudeerden verschillende laboratoriummodellen van triple-negatieve borstkankercellen die vooral verschilden in hoeveel androgeenreceptor ze bevatten. Ze concentreerden zich op twee nieuwere anti-androgene middelen, apalutamide en darolutamide, en combineerden korte blootstellingen aan deze geneesmiddelen met standaarddoses röntgenbestraling. In cellen met hoge niveaus van androgeenreceptor verhoogde apalutamide duidelijk de stralingsschade, waardoor minder cellen in staat waren nieuwe kolonies te vormen. Darolutamide daarentegen had weinig of geen invloed op de stralingsgevoeligheid in dezelfde cellen, en geen van beide geneesmiddelen hielp in cellen die zeer weinig androgeenreceptor tot expressie brachten. Deze bevindingen suggereren dat niet alle androgeenblokkers op dezelfde manier werken bij borstkanker en dat tumoren sterk van deze receptor moeten afhankelijk zijn om baat te hebben van de combinatie.
Het volgen van een sleuteleiwit binnen de cel
Om te begrijpen wat er binnen kankercellen gebeurt na hormoonsignalen of bestraling, volgde het team waar de androgeenreceptor zelf zich bevond. Wanneer cellen werden blootgesteld aan een synthetisch androgeen, verplaatste de receptor zich naar de kern, het controlecentrum waar genen aan- en uitgezet worden. Bestraling alleen dreef de receptor niet uit de kern; hij bleef juist in de kern aanwezig na behandeling, klaar om genactiviteit te beïnvloeden. Toen cellen echter het anti-androgeen middel enzalutamide kregen vóór bestraling, daalden de nucleaire niveaus van de receptor en bleef meer ervan in het cytoplasma van de cel. Dit ondersteunt het idee dat het blokkeren van de kerninvoer van de receptor zijn vermogen om een beschermend genprogramma na bestraling te activeren, verstoort.
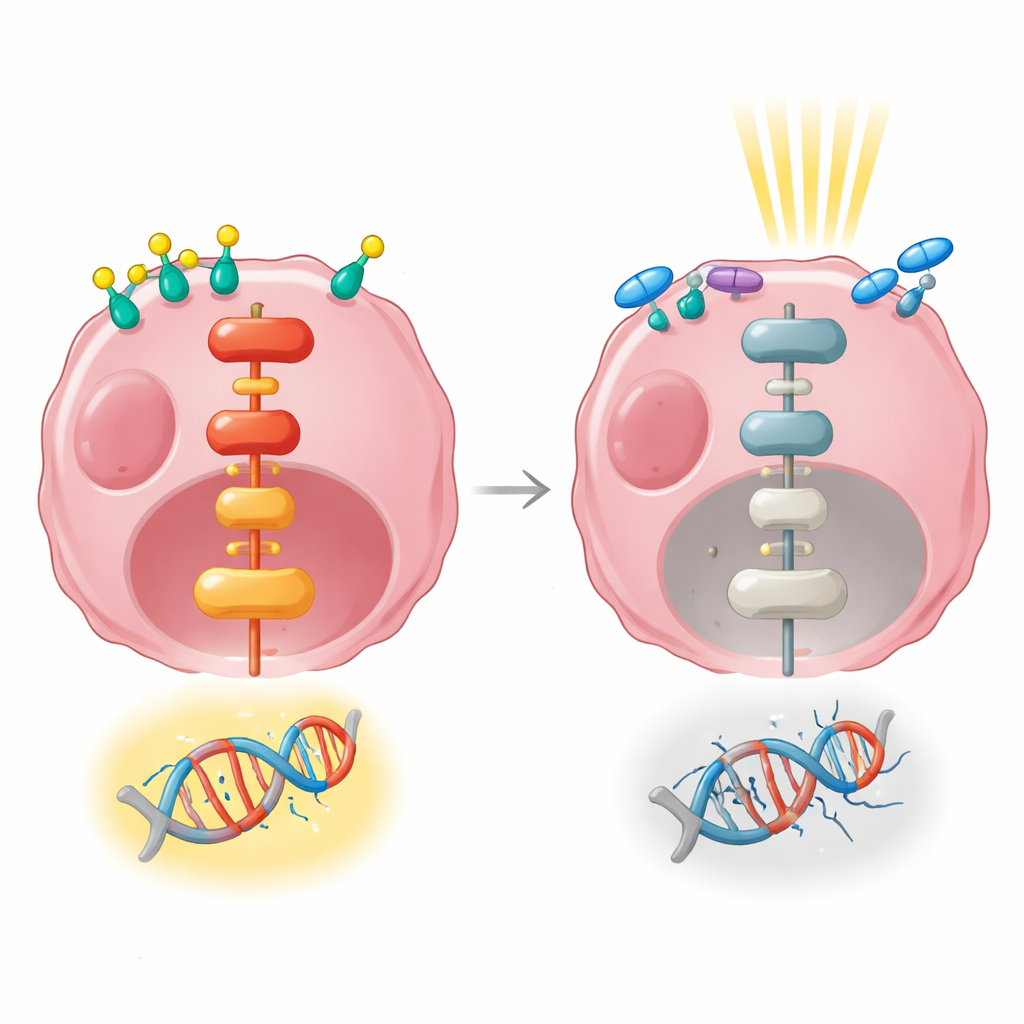
Gensignalen die hormonen met resistentie verbinden
Vervolgens gebruikten de onderzoekers RNA-sequencing om een breed overzicht te krijgen van welke genen omhoog- of omlaaggereguleerd werden na hormoonstimulatie, bestraling of beide. Alleen hormoonbehandeling veranderde de activiteit van honderden genen en beïnvloedde sterk paden die celgroei, hechting en communicatie met de omgeving regelen. Bestraling op zichzelf veranderde, op een vroeg tijdstip, veel minder genen. Toen hormoonstimulatie en bestraling werden gecombineerd, werden veel van dezelfde groeigerelateerde paden geactiveerd, waaronder een belangrijk signaaltraject dat bekendstaat als MAPK/ERK, dat signalen van het celoppervlak naar de kern doorgeeft. Dit pad is bekend om cellen te helpen overleven en DNA-schade te repareren.
Onderzoeken van een overlevingspad dat DNA afschermt
Aangezien MAPK/ERK-signaaltransductie steeds terugkeerde in hun analyses, testten de onderzoekers of het versterken van dit pad het voordeel van androgeenblokkade tijdens bestraling ongedaan kon maken. Ze manipuleerden kankercellen zodat ze een voortdurend actieve variant van ERK overproduceren, een sleutelcomponent van het pad, en herhaalden vervolgens de bestraling plus apalutamide-behandeling. In deze situatie maakte apalutamide de cellen niet langer gevoeliger voor bestraling: het versterkte ERK-signaal leek hen te beschermen. Samen met eiwitmetingen wijzen deze resultaten op MAPK/ERK-signaaltransductie als een cruciale schakel tussen androgeenreceptoractiviteit en het vermogen van de cel om door bestraling veroorzaakte DNA-breuken te herstellen.
Wat dit betekent voor toekomstige borstkankerzorg
Concreet suggereert dit werk dat sommige triple-negatieve borstkankers bestraling overleven door androgeen-gerelateerde signalen te gebruiken om een intern overlevingscircuit aan te zetten dat hen helpt beschadigd DNA te herstellen. Geneesmiddelen zoals apalutamide en enzalutamide kunnen dit circuit onderbreken in tumoren die sterk afhankelijk zijn van de androgeenreceptor, waardoor bestraling effectiever wordt, terwijl tumoren met lage receptorlevels of alternatieve overlevingsroutes mogelijk geen baat hebben. Door de betrokken genpaden in kaart te brengen — vooral het MAPK/ERK-traject — legt deze studie de basis voor meer precieze combinaties van hormoonblokkers, padremmers en bestraling die de uitkomsten voor patiënten met deze moeilijk te behandelen vorm van borstkanker kunnen verbeteren.
Bronvermelding: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
Trefwoorden: triple-negatieve borstkanker, androgeenreceptor, bestralingstherapie, radiosensitisatie, MAPK ERK-signaaltransductie