Clear Sky Science · nl
Programmeerbare lokale immunochemotherapie voor triple-negatieve borstkanker via spatiotemporaal gecontroleerde afgifte van CpG-oligodeoxynucleotiden, gemcitabine en paclitaxel
Een hardnekkige borstkanker veranderd in een lokaal doelwit
Triple-negatieve borstkanker is een van de moeilijkste vormen van borstkanker om te behandelen omdat het de gebruikelijke moleculaire schakelaars mist waaraan veel moderne geneesmiddelen zich hechten. Patiënten zijn vaak aangewezen op krachtige chemotherapie die zich door het hele lichaam verspreidt, met ernstige bijwerkingen en te vaak teleurstellende langdurige beheersing tot gevolg. Deze studie onderzoekt een heel ander idee: in plaats van het lichaam met geneesmiddelen te overspoelen, kunnen we een klein programmeerbaar medicijndepot naast de tumor plaatsen dat chemo- en immuunstimulerende middelen in een zorgvuldig getimede volgorde afgeeft, precies waar ze het meest nodig zijn?
Een klein depot met grote ambities
De onderzoekers ontwikkelden wat ze een Programmeerbare Lokale Immunochemotherapie-platform noemen, of PLICT. Zie het als een zachte, injecteerbare parel die naast een borstkankertumor zit en gedurende weken langzaam behandeling afgeeft. De parel combineert een hydrofiele gel die snel een immuunstimulerend middel en één chemotherapeuticum, gemcitabine, vrijgeeft, met microscopische plastic bolletjes die langzaam een tweede geneesmiddel, paclitaxel, afgeven. De immuunstimulator, een korte DNA-reeks genaamd CpG, is ontworpen om lokale immuuncellen wakker te maken, terwijl de gecombineerde chemotherapieën tumorcellen rechtstreeks aanvallen en de tumoromgeving hervormen zodat immuuncellen naar binnen kunnen trekken en hun werk kunnen doen.
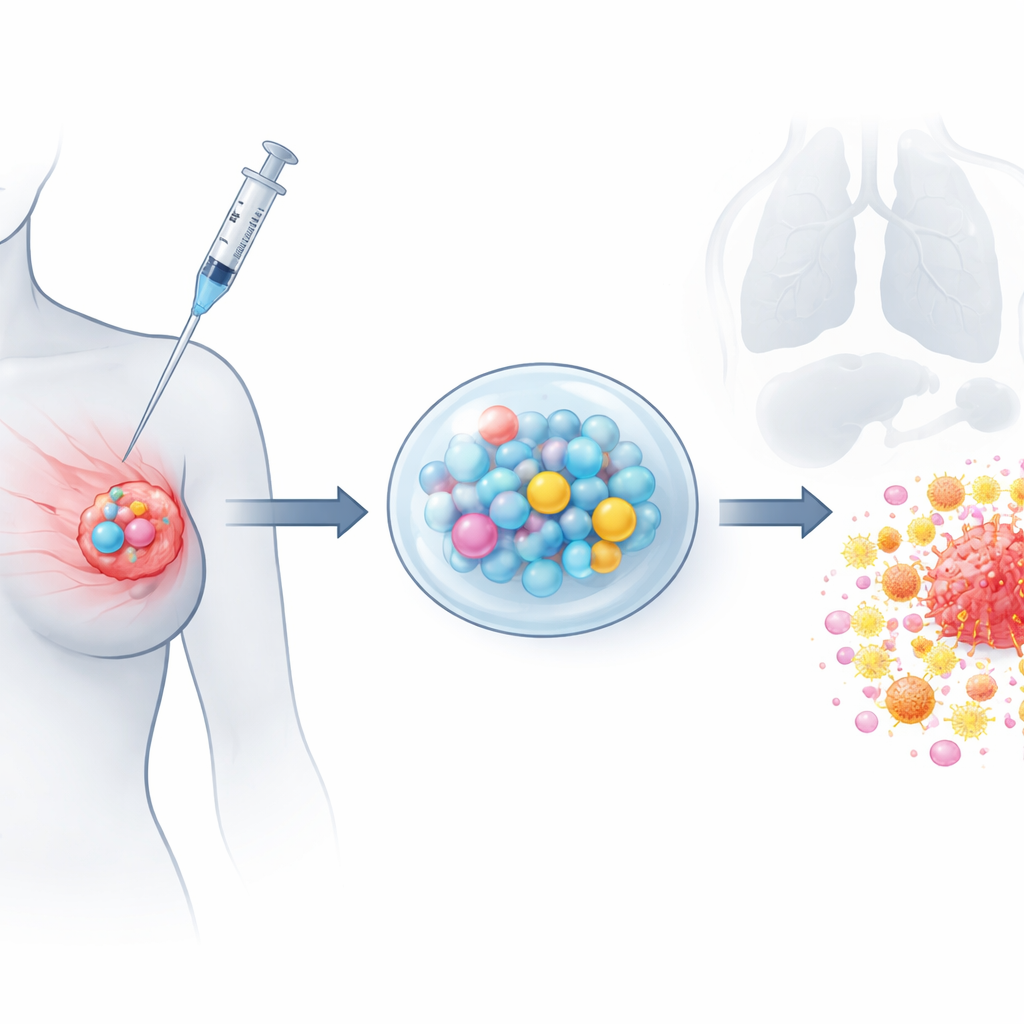
Het ontwerpen van een getimede aanval met gecontroleerde afgifte
Om dit systeem te bouwen, gebruikte het team een hoge-spanning “electrospray”-methode om uniforme, met paclitaxel geladen microsferen te vormen uit een biologisch afbreekbaar polymeer. Beelden toonden gladde, bolvormige deeltjes van ongeveer één tiende van de breedte van een mensenhaar, en laboratoriumtests bevestigden dat paclitaxel gedurende minstens een maand gestaag vrijkwam zonder een vroege uitbarsting. Separaat embedden ze gemcitabine en CpG in een temperatuursensitieve gel die vloeibaar is bij koeling en semi-vaste wordt bij lichaamstemperatuur. Chemische fingerprinting verifieerde dat beide geneesmiddelen intact bleven in hun dragers. Gecombineerd levert de gel een snelle, vroege dosis gemcitabine en CpG, terwijl de microsferen een langdurige druppel paclitaxel bieden, wat de voordelen van langdurige, lage-dosis chemotherapie nabootst vanuit één lokale toepassing.
De lokale strategie testen in muizen
Het team testte vervolgens PLICT in een muismodel van triple-negatieve borstkanker. Muizen ontwikkelden eerst kleine borstumoren en kregen daarna ofwel standaardinjecties met alleen paclitaxel, paclitaxel plus gemcitabine, of een enkele lokale PLICT-implantaat nabij de tumor. Over vier weken groeiden tumoren in de controlegroep snel, die met standaardchemotherapie groeiden langzamer, maar de met PLICT behandelde tumoren waren dramatisch kleiner in zowel omvang als gewicht. Beeldvorming van het hele dier en van verwijderde organen toonde dat PLICT ook de uitzaaiing naar verre locaties, vooral de longen, effectiever terugdrong dan conventionele geneesmiddelinjecties. Metingen van geneesmiddelconcentraties verklaarden waarom: paclitaxel was sterk geconcentreerd in PLICT-behandelde tumoren maar laag in vetweefsel op afstand en vergelijkbaar in de bloedbaan, wat wijst op sterke lokale vasthouding met minder off-target blootstelling.
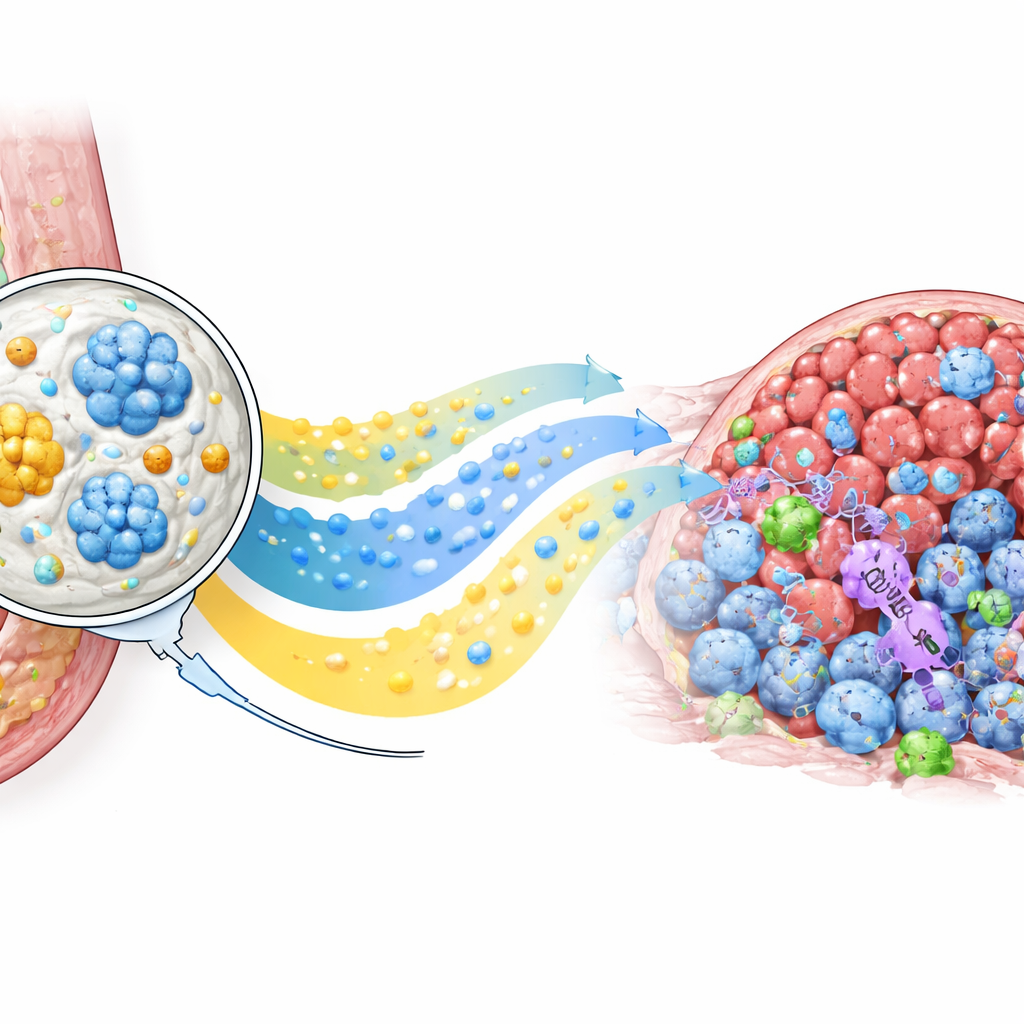
Het lichaam’s eigen verdedigers rekruteren
Naast het verkleinen van tumoren veranderde PLICT het immuunlandschap binnenin. Gedetailleerde celanalyses lieten een sterke toename zien van kanker-dodende CD8-T-cellen in PLICT-behandelde tumoren vergeleken met alle andere groepen, samen met een afname van bepaalde regulerende T-cellen die normaal immuunaanvallen temperen. Weefselkleuring voor CD69, een marker van recent geactiveerde T-cellen, bevestigde dat veel van deze infiltrerende cellen geactiveerd en klaar om te handelen waren. Tegelijkertijd veroorzaakte standaardchemotherapie merkbare schade aan leverweefsel, terwijl organen van PLICT-behandelde muizen er onder de microscoop vrijwel normaal uitzagen. Samen wijzen deze bevindingen erop dat het lokale depot niet alleen de directe geneesmiddelinexpositie in de tumor versterkt, maar ook een gunstiger, minder onderdrukt immuunantwoord ontsteekt zonder extra belasting van vitale organen.
Wat dit zou kunnen betekenen voor toekomstige kankerzorg
Voor niet-specialisten is de boodschap duidelijk: door chemotherapie en immuunstimulatie te veranderen in een langzaam, nauwkeurig gelaagd druppelsysteem dat direct naast de tumor wordt toegediend, behaalde deze benadering in proefdieren sterkere tumorkontrole en minder bijwerkingen over het hele lichaam dan standaard injecties. Het werk bevindt zich nog in de preklinische fase en er blijven vragen over hoe goed zo’n systeem bij mensen of in andere behandelingsinstellingen zou presteren. Maar het concept van een injecteerbaar, programmeerbaar “medicijndepot” dat meerdere middelen achtereenvolgens stil afgeeft, kan nieuwe wegen openen om agressieve kankers zoals triple-negatieve borstkanker te behandelen—de strijd richten waar het het meest telt en tegelijkertijd de rest van het lichaam te sparen.
Bronvermelding: Hsieh, CH., Hsu, MY., Lin, CF. et al. Programmable local immunochemotherapy for triple-negative breast cancer via spatiotemporally controlled release of CpG oligodeoxynucleotides, gemcitabine, and paclitaxel. npj Breast Cancer 12, 45 (2026). https://doi.org/10.1038/s41523-026-00910-7
Trefwoorden: triple-negatieve borstkanker, lokale medicijnafgifte, immunotherapie, gecontroleerde afgifte, hydrogel-microsferen