Clear Sky Science · nl
Expressie van doelwitgenen van oestrogeenreceptor β onthult nieuwe repressieve functies bij agressieve borstkanker
Waarom dit onderzoek ertoe doet
Inflammatoire borstkanker is een van de meest agressieve en dodelijke vormen van borstkanker; het verspreidt zich vaak snel en laat patiënten met weinig gerichte behandelingsopties achter. Deze studie onderzoekt een minder bekende hormoonsensor in borstcellen, oestrogeenreceptor beta, en laat zien hoe deze kan fungeren als een natuurlijke rem op tumorspread. Inzicht in hoe deze ingebouwde rem werkt kan de deur openen naar nieuwe medicijnen die metastase vertragen of voorkomen bij patiënten die momenteel zeer beperkte keuzes hebben.
Een ander gezicht van inflammatoire borstkanker
In tegenstelling tot veel borstkankers die afhankelijk zijn van de klassieke oestrogeenreceptor alfa, ontbreekt deze molecule meestal bij inflammatoire borstkanker en reageert deze dus niet goed op standaard hormoontherapieën. De auteurs richten zich daarom op een tweede oestrogeenreceptor, oestrogeenreceptor beta (ERβ), die zij eerder in verband brachten met minder metastasen bij zowel patiënten als muismodellen. Eerder werk suggereerde dat ERβ het interne steunskelet en het bewegingsapparaat van de cel vertraagt. In deze studie wilde het team genome-breed in kaart brengen hoe ERβ de genactiviteit verandert en welke downstreammoleculen haar beschermende, anti-metastatische rol zouden kunnen verklaren.
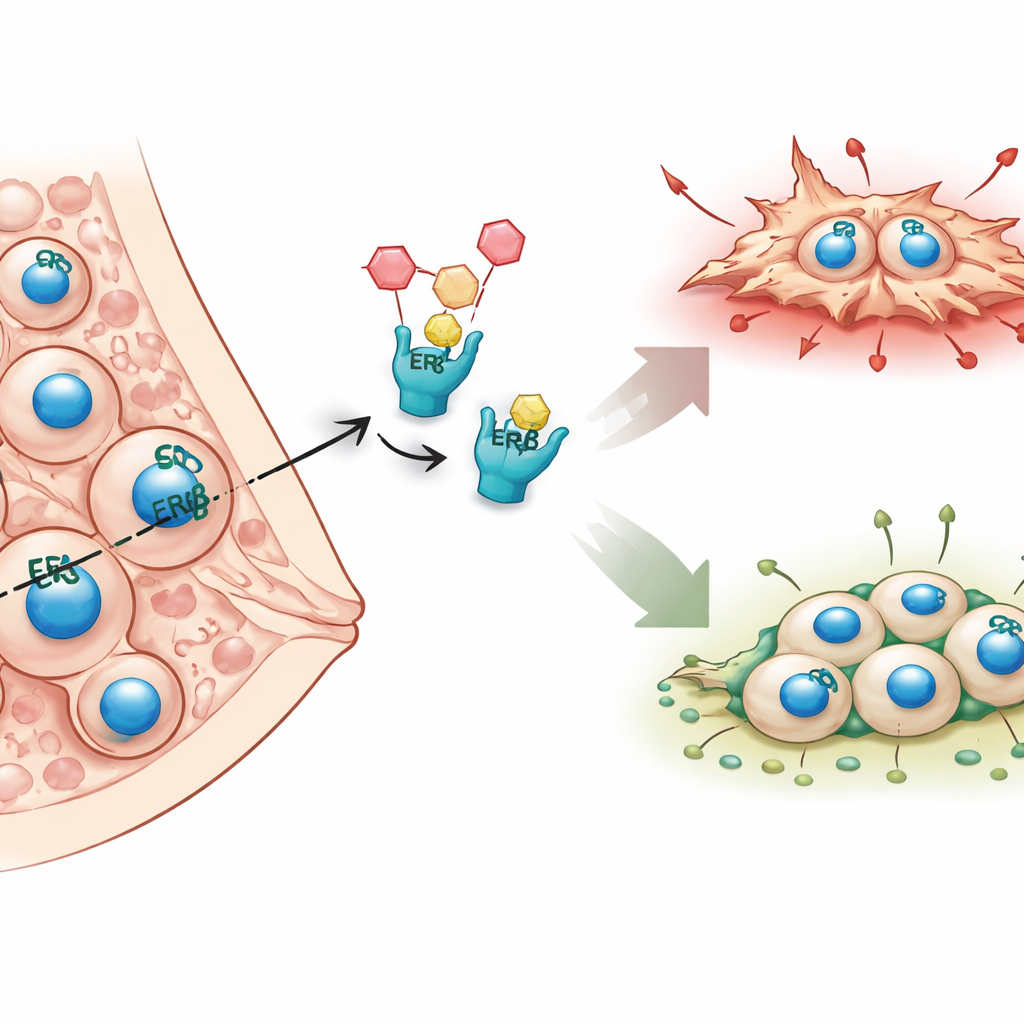
Het instructieboek van de kankercel lezen
Om de invloed van ERβ te ontdekken, gebruikten de onderzoekers twee krachtige sequencingbenaderingen op cellijnen van inflammatoire borstkanker. De ene methode, ChIP-seq, geeft precies aan waar ERβ op het DNA bindt, alsof je specifieke pagina’s en regels in het instructieboek van de cel markeert. De andere methode, RNA-seq, meet welke genen omhoog- of omlaaggeregeld worden wanneer ERβ aanwezig is, afwezig is of geactiveerd wordt door een selectief middel. Door deze datasets te vergelijken, vonden ze duizenden DNA-locaties gebonden door ERβ, waarvan de meeste niet alleen bij klassieke genaan/uit-schakelaars zitten maar diep binnenin of tussen genen, wat wijst op een breed bereik van regulatie. Ze ontdekten ook dat ERβ vaak samenwerkt met families van andere transcriptiefactoren, en complexe vormt die gezamenlijk beslissen welke genen worden stilgelegd of geactiveerd.
Groeien, bewegen en metabolisme herschakelen
De geïntegreerde analyse toonde aan dat ERβ de neiging heeft genen te dempen die celbeweging, morfologische veranderingen en invasie bevorderen, vooral die gekoppeld aan het actine-cytoskelet en Rho GTPase-signaleringsroutes — pathways die bekend staan om het stimuleren van metastase. Tegelijkertijd ondersteunt ERβ genprogramma’s die verband houden met weefselontwikkeling en celdifferentiatie, waardoor kankercellen meer naar een sessielere, minder agressieve staat worden gestuurd. De studie onthulde ook een verrassende rol voor ERβ bij het aanpassen van metabole routes, met name die welke vetzuren en fosfolipiden betreffen — sleutelbrandstof en bouwstenen voor snelgroeiende tumoren. Belangrijk is dat deze effecten werden gezien niet alleen in cellen die zodanig waren gemanipuleerd dat ze ERβ overproduceren, maar ook in cellen met natuurlijke receptorlevels, wat het real-world belang versterkt.
Kleine RNA-boodschappers en klinische impact
Naast proteïnencoderende genen onderzochten de onderzoekers microRNA’s — kleine RNA-moleculen die genexpressie fijn afstemmen. Ze vonden tientallen microRNA’s waarvan de niveaus veranderden wanneer ERβ werd verwijderd of hersteld, waarvan er veel in verband zijn gebracht met tumorremming bij borstkanker. Door deze microRNA’s te koppelen aan hun doelsgenen toonden de auteurs aan dat ERβ sommige kankeraanjagers indirect reguleert via een gelaagd regulatoir netwerk. Vervolgens bekeken ze patiëntgegevens en onderzochten tumoren van individuen met inflammatoire en niet-inflammatoire borstkanker. Verschillende door ERβ gecontroleerde genen waren sterk gerelateerd aan overleving: hoge niveaus van sommige (zoals SERPINA1 en HSPB8) voorspelden betere uitkomsten, terwijl hoge niveaus van andere (zoals PITX1 en HOMER3) gekoppeld waren aan slechtere overleving. Dit plaatst deze downstreammoleculen als potentiële markers voor prognose en als toekomstige medicijndoelen.
Van moleculaire rem naar toekomstige therapieën
Al met al schetst de studie ERβ als een centrale rem op het invasieve gedrag van cellen van inflammatoire borstkanker. Door aan DNA te binden, samen te werken met andere regulatoren en zowel gen- als microRNA-netwerken te vormen, dempt ERβ programma’s die celmigratie en metastase aansturen, terwijl het stabielere, gedifferentieerde toestanden bevordert en het kankermetabolisme herschakelt. Voor patiënten suggereert dit dat middelen die ERβ activeren of de belangrijke downstreamdoelen van ERβ remmen — vooral die betrokken bij celbeweging en vetzuurgebruik — de basis zouden kunnen vormen voor nieuwe, meer precieze behandelingen voor deze moeilijk te behandelen ziekte.
Bronvermelding: Tastsoglou, S., Karagounis, I.V., Miliotis, M. et al. Estrogen receptor β target gene expression reveals novel repressive functions in aggressive breast cancer. npj Breast Cancer 12, 38 (2026). https://doi.org/10.1038/s41523-026-00905-4
Trefwoorden: inflammatoire borstkanker, oestrogeenreceptor beta, metastase, genregulatie, kankermetabolisme