Clear Sky Science · nl
De CXCL10/CXCR3-as is essentieel om immunologische rusttoestand te behouden bij triple-negatieve borstkanker
Waarom sommige kankers slapen in plaats van zich verspreiden
Borstkanker kan zich soms gedragen als een sluimerende agent. Na de eerste behandeling kunnen een paar kankercellen jarenlang in het lichaam verborgen blijven, niet voldoende groeiend om op scans te worden gezien — maar nog steeds in staat later wakker te worden en levensbedreigende uitzaaiingen te veroorzaken. Dit artikel onderzoekt waarom die "slaap"toestand, dormantie genoemd, voorkomt bij een bijzonder agressieve vorm van de ziekte, triple-negatieve borstkanker, en onthult een chemisch signaal dat het immuunsysteem helpt deze cellen onder controle te houden.
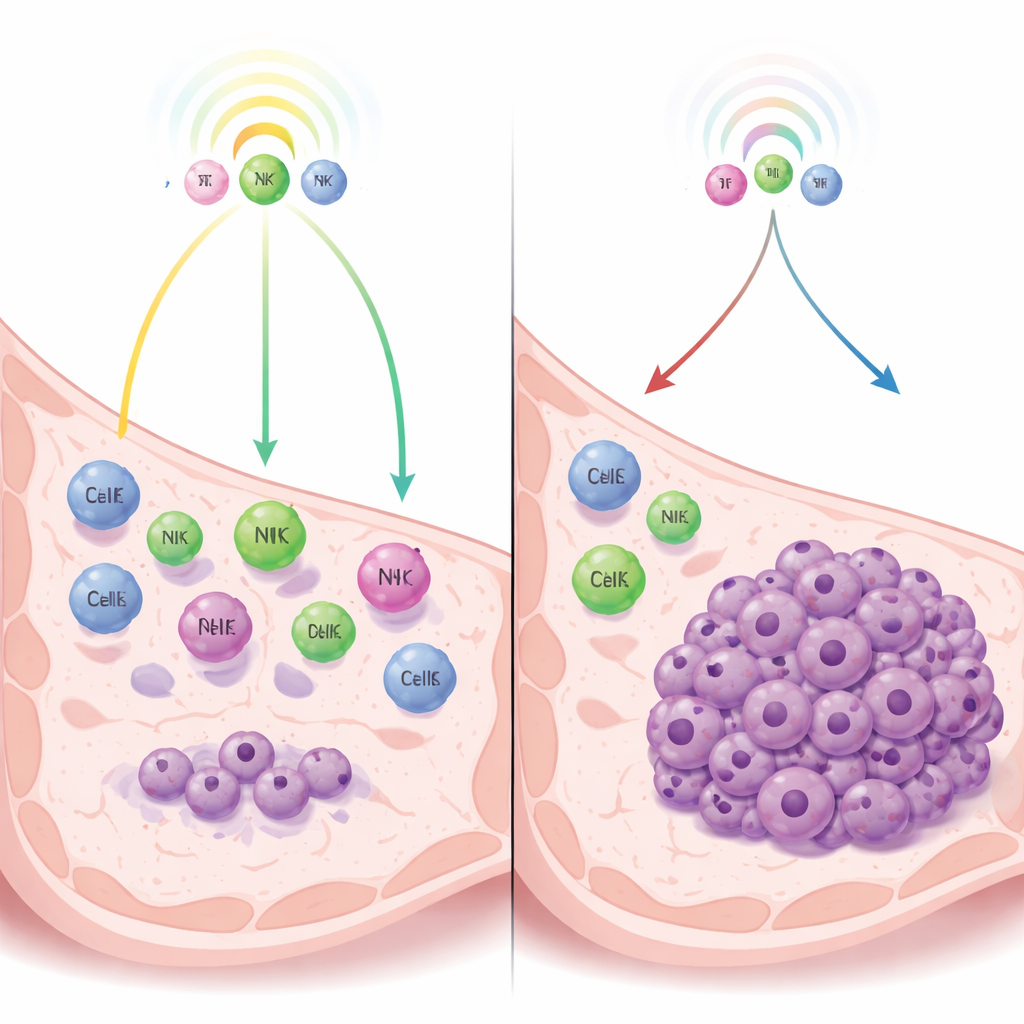
Een touwtrekken tussen kanker en het immuunsysteem
De auteurs richten zich op een vorm van dormantie die niet wordt geregeld door gebrek aan bloedtoevoer of interne remmen van de cel, maar door immuunbewaking — het constante toezicht van immuuncellen dat tumoren op afstand kan houden zonder ze volledig uit te roeien. Met behulp van muismodellen van triple-negatieve borstkanker vergelijken ze tumorcellen die van nature dormante blijven met nauw verwante cellen die snelgroeiende tumoren vormen. Door te onderzoeken welke genen zijn ingeschakeld, vinden ze dat dormante cellen sterk interferonroutes activeren — immuunalarmwegen die de afgifte van signaalstoffen stimuleren die immuuncellen naar het tumorgebied aantrekken.
Een sleutelmolecuul dat tumoren stilhoudt
Onder de vele moleculen die in dormante cellen worden geactiveerd, springt er één uit: CXCL10, een klein eiwit dat fungeert als baken voor immuuncellen die de bijpassende receptor CXCR3 dragen. Dormante kankercellen produceren veel meer CXCL10 dan hun agressieve tegenhangers. Wanneer de onderzoekers CXCL10 doelbewust uitschakelen in dormante cellen en deze in muizen met een intact immuunsysteem implanteren, vormen de eens stille cellen snel tumoren. Het blokkeren van de CXCR3-receptor met een antilichaam heeft een vergelijkbaar effect. In beide gevallen ontsnappen kankercellen aan de immuunpatstelling en beginnen te groeien, wat laat zien dat de CXCL10/CXCR3-as niet alleen geassocieerd is met dormantie — maar vereist is om die te behouden.
Hoe verandering van de lokale omgeving het evenwicht doet kantelen
Het terugschakelen van CXCL10 doet meer dan een enkele route veranderen; het herschikt het hele lokale immuunnlandschap. In tumoren die CXCL10 hebben verloren, nemen nuttige CD4- en CD8-T-cellen af, terwijl bepaalde myeloïde cellen die immuunreacties kunnen onderdrukken juist in aantal toenemen. Natural killer-cellen en dendritische cellen verschuiven ook in aantal. Dit patroon blijkt zowel in primaire tumoren als in de longen, waar kankercellen heen kunnen reizen en onderduiken. Zelfs wanneer longmetastasen te klein zijn om onder de microscoop te zien, tonen moleculaire markers aan dat meer kankercellen er in slagen zich in de longen te vestigen wanneer CXCL10 afwezig is, en dat minder T-cellen die weefsels infiltreren. Toch maakt het verwijderen van CXCL10 geen verschil in muizen die helemaal geen werkend immuunsysteem hebben — dormante cellen groeien ongeacht — wat benadrukt dat dit signaal via immuuncontrole werkt in plaats van een directe rem op de kankercelgroei.
Waarom meer signaal helpt maar geen magische schakelaar is
Het team test ook het omgekeerde: kan het verhogen van CXCL10 een agressieve tumor in een dormante veranderen? Wanneer ze snelgroeiende kankercellen zodanig aanpassen dat ze extra CXCL10 produceren, groeien tumoren langzamer en doen ze er langer over om te verschijnen, en sommige immuunceltypes in het bloed nemen toe. Volledige dormantie treedt echter niet op; uiteindelijk ontwikkelen alle muizen nog steeds tumoren. Dit suggereert dat hoewel CXCL10 essentieel is voor het behouden van dormantie wanneer de rest van de immuunmachine aanwezig is, het op zichzelf die complexe toestand niet uit het niets kan opbouwen. Andere routes moeten samenwerken om een langdurig evenwicht tussen immuunaanval en overleving van kankercellen te creëren.
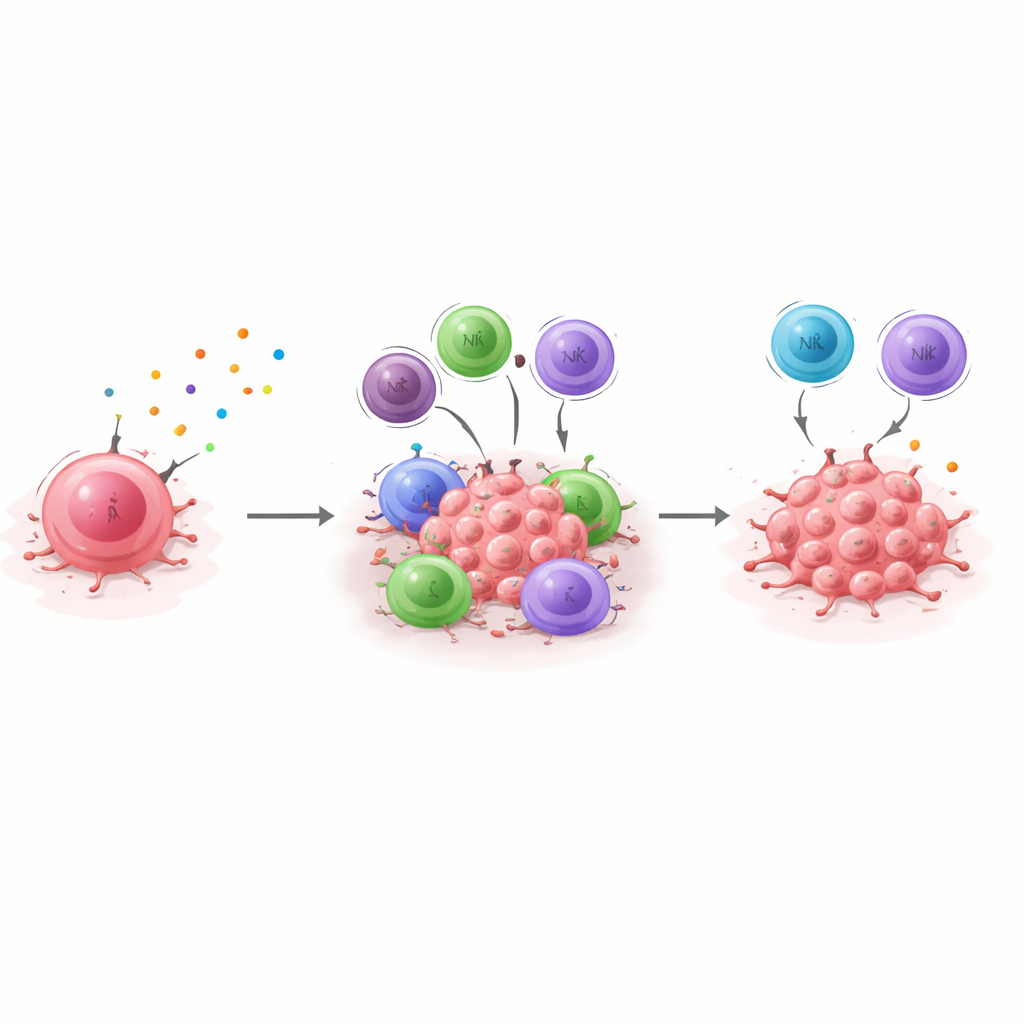
Van muisexperimenten naar patiëntenvooruitzicht
Om hun bevindingen met menselijke ziekte te verbinden, leiden de onderzoekers een "dormantiesignatuur" af — een set genen die consequent hoger is in dormante cellen en daalt wanneer CXCL10 wordt uitgeschakeld. Ze bekijken vervolgens grote datasets van borstkankerpatiënten en vragen hoe deze signatuur samenhangt met overleving. Bij triple-negatieve borstkanker leven patiënten van wie de tumoren deze dormantiesignatuur hoger tot uiting brengen gemiddeld langer en blijven ze langer vrij van terugkeer, wat overeenkomt met een immuun-gecontroleerde dormante staat die terugkeer uitstelt. Het effect is niet op dezelfde manier zichtbaar bij hormoonpositieve tumoren, wat biologische verschillen tussen borstkankersubtypen benadrukt. Gezamenlijk suggereren de resultaten dat de CXCL10/CXCR3-as een centraal pijler is van immuun-gemedieerde dormantie bij triple-negatieve borstkanker, en dat het meten van deze dormantiesignatuur kan helpen patiënten te identificeren die waarschijnlijk profiteren van therapieën die immuuncontrole versterken — of omgekeerd, degenen die mogelijk langduriger nauwlettend gevolgd moeten worden omdat hun kanker minder goed onder controle wordt gehouden.
Bronvermelding: Yilmaz, A., Haerri, L., Granda, M.E. et al. The CXCL10/CXCR3 axis is essential for sustaining immunological dormancy in triple-negative breast cancer. npj Breast Cancer 12, 36 (2026). https://doi.org/10.1038/s41523-026-00903-6
Trefwoorden: triple-negatieve borstkanker, tumor-dormantie, immuunbewaking, chemokinesignalering, CXCL10 CXCR3-as