Clear Sky Science · nl
Ruimtelijke genexpressie-analyse onthult drijfveren van extreem vroege lymfekliermetastase bij borstkanker
Waarom kleine rondreizende kankercellen ertoe doen
Wanneer borstkanker zich buiten de borst verspreidt, stopt ze vaak eerst in nabijgelegen lymfeklieren — kleine filters die helpen bij het bestrijden van infecties. Artsen weten dat het aantreffen van kanker in deze knopen doorgaans wijst op een hoger risico op terugkeer van de ziekte. Maar wat er precies gebeurt in de allereerste momenten wanneer slechts een handjevol cellen een lymfeklier bereikt, was bij echte patiënten bijna onmogelijk te zien. Deze studie gebruikte een nieuw soort microscopische “kaart” van genactiviteit om die vroegste stappen met ongekende detailwaarneming te volgen, en onthulde welke cellen slagen, welke falen en waarom dat belangrijk is voor de uitkomst van patiënten.
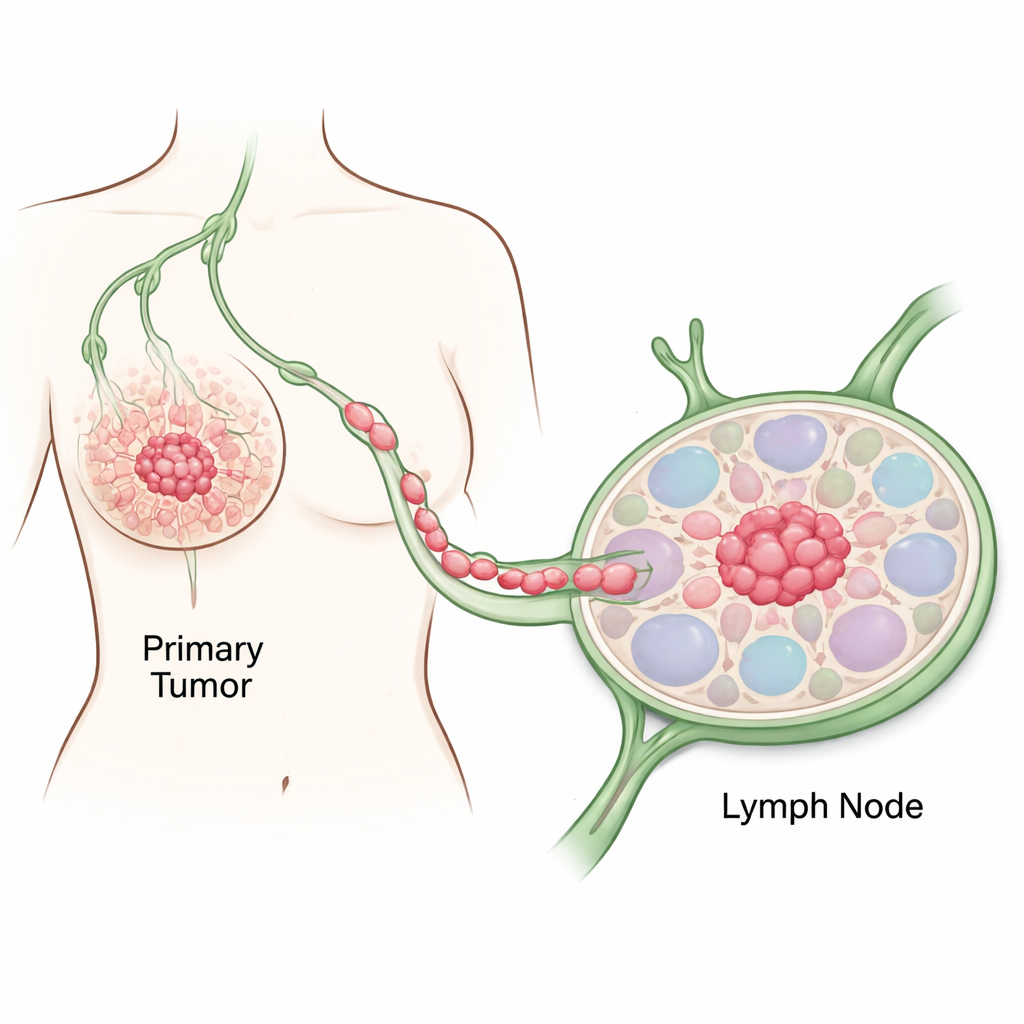
De eerste stappen van kanker volgen
De onderzoekers concentreerden zich op weefsel van een 80-jarige vrouw met een agressieve HER2-positieve borstkanker. Ze namen zowel monsters van normaal ogende borstgebieden als van nabijgelegen tumorregio’s, en gebruikten vervolgens meerdere DNA- en RNA-tests om te reconstrueren hoe gewone cellen kankerachtig werden. In vergelijking met gezond weefsel vertoonden tumorregio’s klassieke kenmerken van kanker: verstoorde celadhesie, hyperactieve celdeling, grootschalige veranderingen in DNA-methylering en belangrijke mutaties in genen die groei en genomische stabiliteit regelen. Deze moleculaire veranderingen stemden overeen met wat pathologen onder de microscoop zagen, en bevestigden een stapsgewijze overgang van normale borstcellen naar volledig kwaadaardige cellen.
Vormveranderende cellen in beweging
Om te begrijpen hoe tumorcellen beginnen te reizen, gebruikte het team een hoogresolutie techniek die genactiviteit leest in individuele cellen terwijl hun exacte positie in het weefsel behouden blijft. Dit stelde hen in staat te reconstrueren hoe kankercellen van identiteit veranderden toen ze normale borststructuren verliet en richting metastase trokken. Ze ontdekten dat de kanker leek voort te komen uit één bepaald type rijpe borstcel, dat vervolgens geleidelijk kenmerken overnam van een proces dat epitheliale–mesenchymale overgang genoemd wordt — een soort vormverandering die cellen helpt losser te worden, te bewegen en omliggend weefsel binnen te dringen. In plaats van een eenvoudige aan/uit-schakelaar, bezetten cellen een spectrum van gemengde toestanden, waarin “epitheliale” eigenschappen (ordelijk, aan elkaar vastzittend) samengaan met “mesenchymale” eigenschappen (bewegelijk, invasief). Sommige van deze hybride cellen verspreidden zich door de tumor, terwijl andere zich bundelden in meer gevorderde kankergroepen die klaar leken om zich naar lymfeklieren te verspreiden.
Het eerste verre bruggenhoofd in een lymfeklier
In een lymfeklier die bij standaard klinische testen als metastasevrij werd beschouwd, zagen de wetenschappers iets opmerkelijks: slechts 30 verdwaalde tumorcellen, die een gebied van ongeveer 200 micrometer bedekten — ruwweg twee keer zo breed als een mensenhaar. Deze geïsoleerde tumorcellen kwamen uit verschillende hybride toestanden, elk met een eigen patroon van genactiviteit. Door verwante kankercellen te groeperen, definieerde het team zes subtypes met verschillende rollen. Eén subtype, sterk mesenchymaal, leek bijzonder goed bestand tegen celdood en het ontsnappen aan immuunaanvallen. Een ander subtype, dat meer epitheliale kenmerken herwon, toonde een opvallende verschuiving in zijn energiegebruik, met een voorkeur voor vetzuurmetabolisme. Alleen deze metabool-herschikte, meer epitheliaal-achtige groep slaagde erin kleine kolonies in lymfeklieren te vormen, wat suggereert dat de keuze van brandstof — niet alleen invasiviteit — mede bepaalt of vroege aankomsten zich kunnen vestigen.
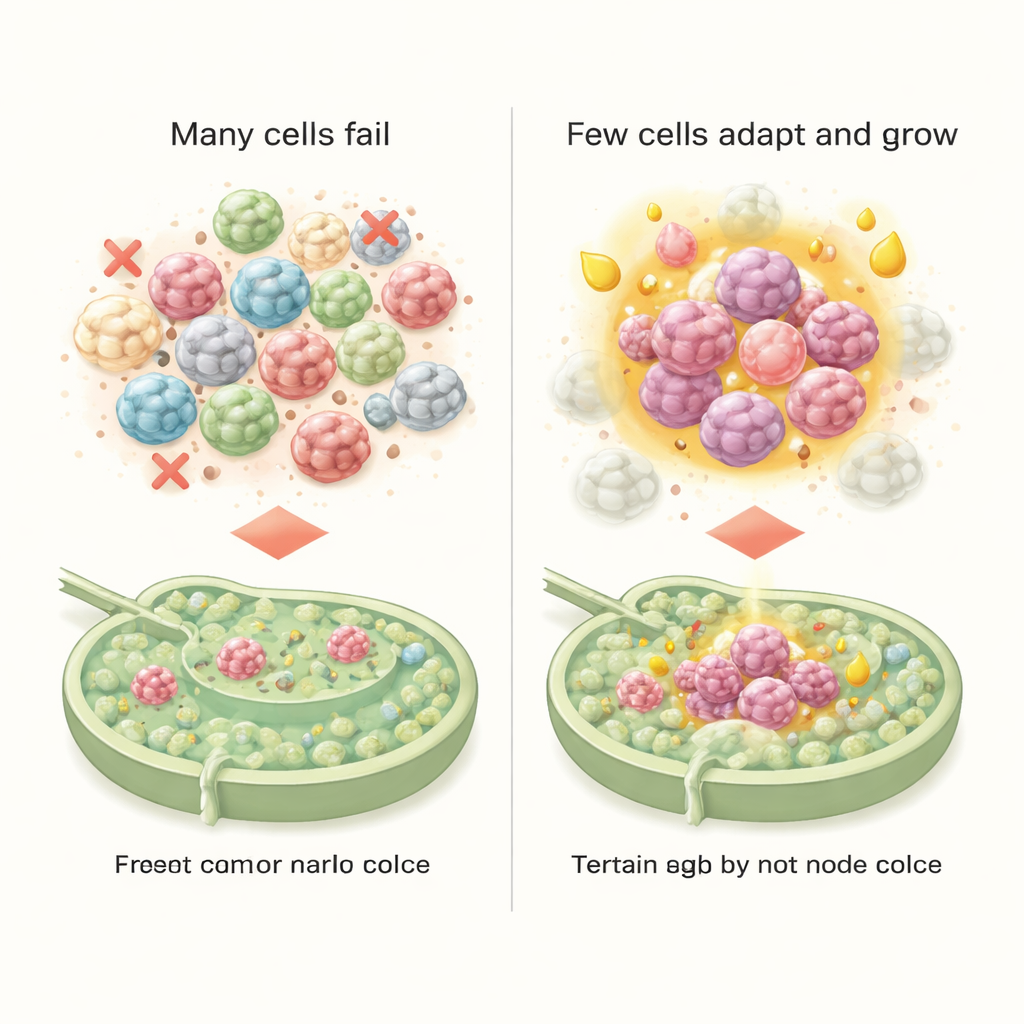
Een lymfeklier die de kanker stilletjes helpt
De studie onderzocht ook hoe de lymfeklieromgeving reageerde op deze indringers. Zelfs voordat een zichtbare metastase was gevormd, zonden immuuncellen, bloedvatcellen en bindweefsel al signalen uit die immuunreacties afzwakten en tumoroverleving ondersteunden. Bepaalde receptor–ligandparen tussen immuuncellen wezen op vroege immuuntolerantie, terwijl andere nieuwe bloedvatgroei en herstructurering van het weefselskelet aanmoedigden. Gezamenlijk bouwden deze veranderingen een niche die verrassend gastvrij was voor de metabool aangepaste kankercellen, en hielpen ze die cellen overleven, groeien en mogelijk toekomstige verspreiding zaad te leggen.
Wat dit betekent voor patiënten
Door hun bevindingen te vergelijken met grote, bestaande patiëntendatasets, deden de onderzoekers een contra-intuïtieve ontdekking. De cellen die het beste vroege lymfeklierkolonies vormden, en zelfs die met de sterkste mesenchymale kenmerken, kwamen niet overeen met de slechtste klinische uitkomsten. In plaats daarvan hadden patiënten het slechtst wanneer hun tumoren bepaalde agressieve hybride celtypen bevatten die gekenmerkt werden door hoge celcyclusactiviteit en suikerverbranding (glycolyse) programma’s aangedreven door genen zoals MYC. Met andere woorden: verschillende vormveranderde celtoestanden lijken zich te specialiseren: sommige zijn experts in het stilletjes koloniseren van nieuwe locaties, terwijl andere snelle groei en terugkeer aansturen. Het begrijpen en gericht aanpakken van deze verschillende celtoestanden en hun metabolische voorkeuren kan leiden tot preciezere behandelingen — behandelingen die niet alleen de vroegste verspreiding betrouwbaarder detecteren, maar ook de tumorceltypen kunnen wegknippen die het meest waarschijnlijk dodelijke terugvallen veroorzaken.
Bronvermelding: Nagasawa, S., Kajiya, K., Ishikawa, E. et al. Spatial gene expression analysis reveals drivers of extremely early lymph node metastasis in breast cancer. npj Breast Cancer 12, 28 (2026). https://doi.org/10.1038/s41523-026-00897-1
Trefwoorden: borstkankermetastase, lymfeklier, epitheliale-mesenchymale overgang, ruimtelijke transcriptomica, kankermetabolisme