Clear Sky Science · nl
Gezamenlijke levering van chemokine CXCL9 en costimulatorische ligand TNFSF9 door mesenchymale stamcellen herprogrammeert het immuunmicro‑milieu bij triple‑negatieve borstkanker
Waarom deze nieuwe benadering bij borstkanker belangrijk is
Triple‑negatieve borstkanker behoort tot de gevaarlijkste vormen van borstkanker omdat ze snel groeit, vroeg uitzaait en de veelvoorkomende hormonale doelwitten mist waarop veel geneesmiddelen vertrouwen. Immunotherapie heeft hoop gewekt, maar bij veel patiënten dringen de afweercellen simpelweg niet in voldoende aantallen het tumorweefsel binnen om effect te sorteren. Deze studie onderzoekt een vindingrijke strategie: levende dragercellen gebruiken als gerichte “leveringswagens” die immuunstimulerende signalen rechtstreeks in moeilijk behandelbare tumoren brengen, waardoor mogelijk meer patiënten in aanmerking komen voor krachtige immuungerichte behandelingen.
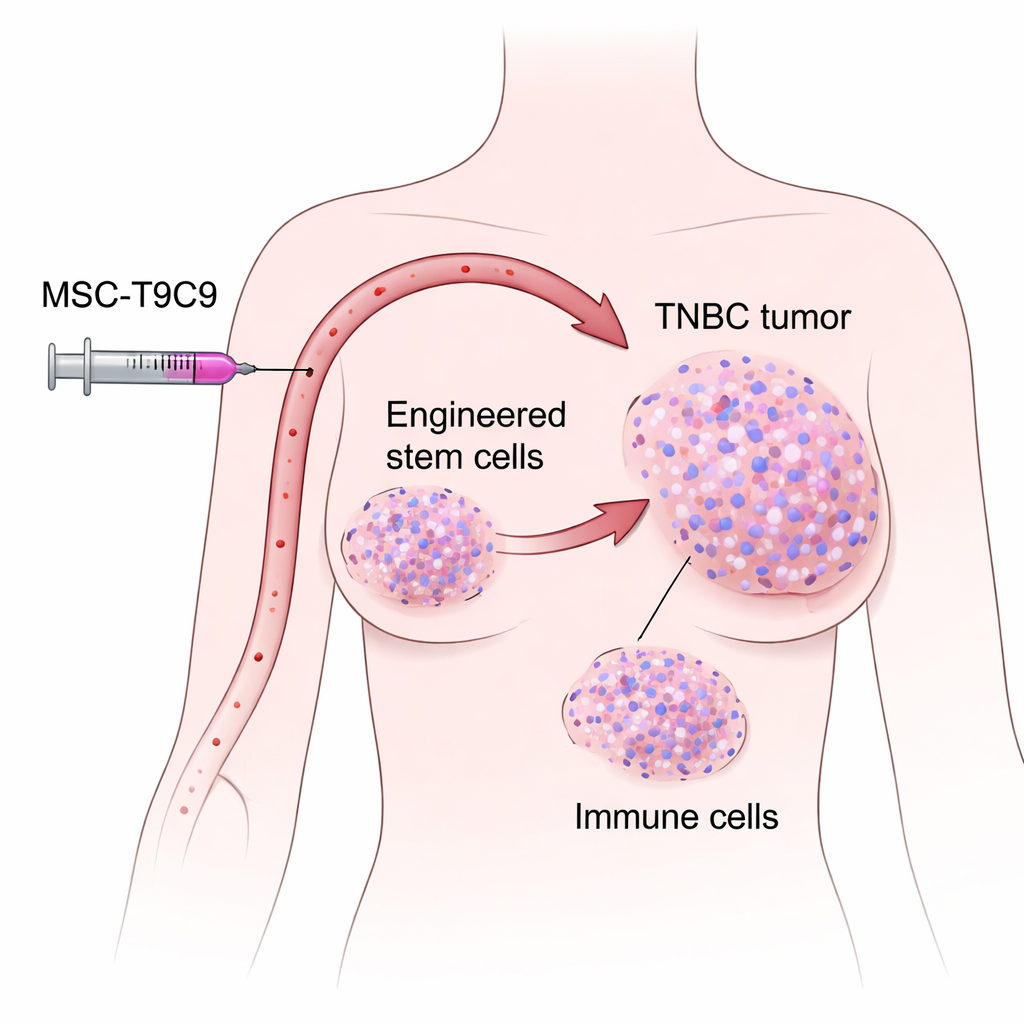
Een hardnekkige kanker met te weinig immuunhulp
Standaardbehandelingen voor triple‑negatieve borstkanker — chirurgie, chemotherapie en bestraling — voorkomen vaak geen terugkeer, en de gemiddelde overleving bij gevorderde ziekte blijft onder de twee jaar. Een belangrijke reden is dat veel van deze tumoren “koud” zijn: ze bevatten weinig kankerbestrijdende immuuncellen. Grote patiëntendatabanken lieten zien dat mensen waarvan de tumoren van nature hogere hoeveelheden van twee immuun‑gerelateerde moleculen, CXCL9 en TNFSF9, produceren, doorgaans langer leven en meer T‑cellen en natural killer (NK)‑cellen in hun tumoren hebben. CXCL9 is een chemisch signaal dat immuuncellen naar het weefsel roept, terwijl TNFSF9 fungeert als een extra ‘gas’‑schakelaar die die cellen helpt krachtiger aan te vallen. Het patroon suggereerde dat het verhogen van beide signalen rechtstreeks in tumoren het voordeel naar het immuunsysteem kan doen verschuiven.
Stamcellen omvormen tot slimme leveringswagens
De onderzoekers richtten zich op mesenchymale stamcellen afkomstig van gedoneerde menselijke navelstrengen. Deze cellen hebben een nuttige eigenschap: wanneer ze in de bloedbaan van muizen met borsttumoren worden geïnjecteerd, trekken ze van nature naar tumorlokaties en blijven daar dagenlang aanwezig, terwijl ze normale organen grotendeels vermijden. Het team bracht genetische wijzigingen aan in deze stamcellen zodat ze CXCL9 afgeven en TNFSF9 op hun oppervlak tonen, waarmee ze een dubbeldoelige celtherapie creëerden die ze MSC‑T9C9 noemen. Laboratoriumtesten toonden aan dat de gewijzigde cellen hoge niveaus van CXCL9 uitscheiden en muis‑T‑cellen en NK‑cellen sterk activeren, zonder hun eigen groeigedrag te veranderen of zelf tumoren te veroorzaken. Dit maakte ze veelbelovend als gerichte immuunversterkers.
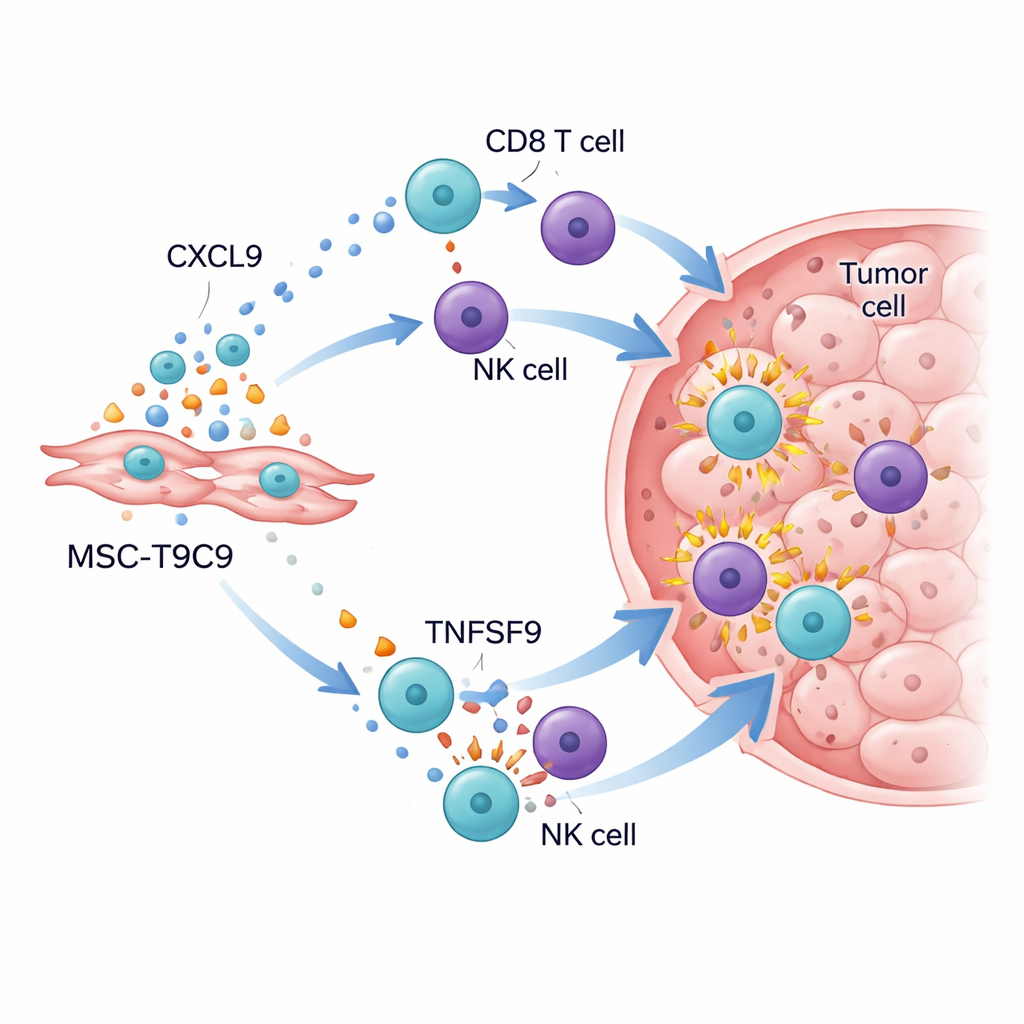
Het immuun‑slagveld van de tumor wakker maken
Wanneer de gemodificeerde cellen werden toegediend aan muizen met triple‑negatieve borsttumoren, waren de resultaten opvallend. Bij muizen met een werkend immuunsysteem remden herhaalde injecties van MSC‑T9C9 de tumorgroei sterk en verhoogden ze de kankerceldood, terwijl controle‑stamcellen weinig effect hadden. Gedetailleerde analyse van de tumoren toonde een dramatische toename van het aantal CD8‑‘killercellen’ en NK‑cellen, samen met hogere niveaus van krachtige aanvalsmoleculen zoals granzyme B, interferon‑γ, tumor necrose factor‑α en interleukine‑2. Tegelijkertijd verschoof de tumoromgeving weg van een onderdrukkende toestand: behulpzame ontstekingsmacrofagen namen toe, en hoewel regulerende T‑cellen nog aanwezig waren, werden ze overvleugeld door de nieuwe golf van strijders. In immuun‑deficiënte muizen, waar T‑ en NK‑cellen ontbreken, vertraagde MSC‑T9C9 de tumorgroei niet, wat bevestigt dat het voordeel afhankelijk is van het mobiliseren van de eigen afweer van het lichaam.
Tumoren klaarmaken voor checkpoint‑therapie
Moderne immunotherapiegeneesmiddelen zoals anti‑PD‑1‑antilichamen halen moleculaire ‘remmen’ van T‑cellen, maar ze werken het best wanneer er al voldoende T‑cellen in de tumor aanwezig zijn. De studie vond dat MSC‑T9C9 niet alleen meer CD8‑T‑cellen naar tumoren trok, maar ze ook in een zeer actieve, doch rem‑gevoelige staat duwde, gekenmerkt door de PD‑1‑receptor. In een muismodel leverde de combinatie van MSC‑T9C9 met een anti‑PD‑1‑middel de sterkste tumorkrimp en de langste overleving op vergeleken met een van beide behandelingen alleen. Analyses van menselijke kankerdata ondersteunden dit idee: patiënten met hogere gecombineerde niveaus van TNFSF9 en CXCL9 hadden meer kans te profiteren van checkpoint‑blokkerende therapieën, wat suggereert dat dezelfde biologische principes ook bij mensen kunnen gelden.
Veiligheid en toekomstige belofte
Elke behandeling die de immuniteit verhoogt, wekt zorgen over gevaarlijke bijwerkingen zoals wijdverbreide ontsteking of orgaanschade. Bemoedigend was dat muizen die MSC‑T9C9 ontvingen een normaal gewicht en gedrag behielden, geen duidelijke schade aan belangrijke organen toonden en normale bloed‑ en lever‑nierwaarden hadden. Belangrijk is dat de opleving in immuunactiviteit grotendeels beperkt bleef tot de tumor zelf en dat ontstekingssignalen in de bloedbaan niet stegen. Hoewel er meer werk nodig is voordat er menselijke proeven kunnen beginnen — inclusief testen in meer realistische modellen en zorgvuldige dosisbepaling — suggereert deze studie dat het gericht naar tumoren geleiden van gemodificeerde stamcellen om immuuncellen op te roepen en te activeren, een gerichte en mogelijk veiligere manier kan bieden om ‘koude’ triple‑negatieve borstkankers ‘heet’ te maken en beter reageerbaar op immunotherapie.
Bronvermelding: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Trefwoorden: triple‑negatieve borstkanker, immunotherapie, mesenchymale stamcellen, tumor micro‑milieu, checkpoint‑blokkade