Clear Sky Science · nl
Interleukine‑1α van de gastheer veroorzaakt tumorimmunosuppressie door tumorgeassocieerde myeloïde cellen te herprogrammeren
Waarom dit onderzoek belangrijk is voor kankerpatiënten
Immunotherapie heeft de behandeling van bepaalde kankers veranderd, maar veel borstumoren ontkomen nog steeds aan het immuunsysteem. Dit artikel onderzoekt een minder bekende dader: een signaalmolecuul genaamd interleukine‑1 alfa (IL‑1α) dat niet door de kankercellen zelf wordt geproduceerd, maar door normale cellen van het lichaam. De auteurs tonen aan dat door de gastheer geproduceerde IL‑1α immuuncellen stilletjes in bondgenoten van de tumor kan veranderen, en dat het blokkeren van dit signaal bij muizen kan leiden tot krimping of verdwijning van borsttumoren. Inzicht in deze omschakeling kan artsen helpen behandelingen te ontwerpen die immunotherapie bij borstkanker effectiever maken.
Een verborgen beïnvloeder in de tumoromgeving
Kankers groeien niet geïsoleerd; ze leven in een drukke “buurt” van immuuncellen, bloedvaten en bindweefsel die bekendstaat als de tumormicro-omgeving. Tot de belangrijkste bewoners behoren myeloïde cellen, vooral macrofagen, die tumoren kunnen aanvallen of juist beschermen. Klassieke leerboeken delen macrofagen in M1 (tumorbestrijdend) en M2 (tumorondersteunend), maar in echte tumoren komen veel tussenvormen voor. De auteurs richtten zich op IL‑1α, een molecuul dat normaal door niet-kankertissue wordt gemaakt, om te onderzoeken of dit gastheer‑signaal binnenkomende myeloïde cellen stuurt naar behulpzame of schadelijke rollen in borstumoren.
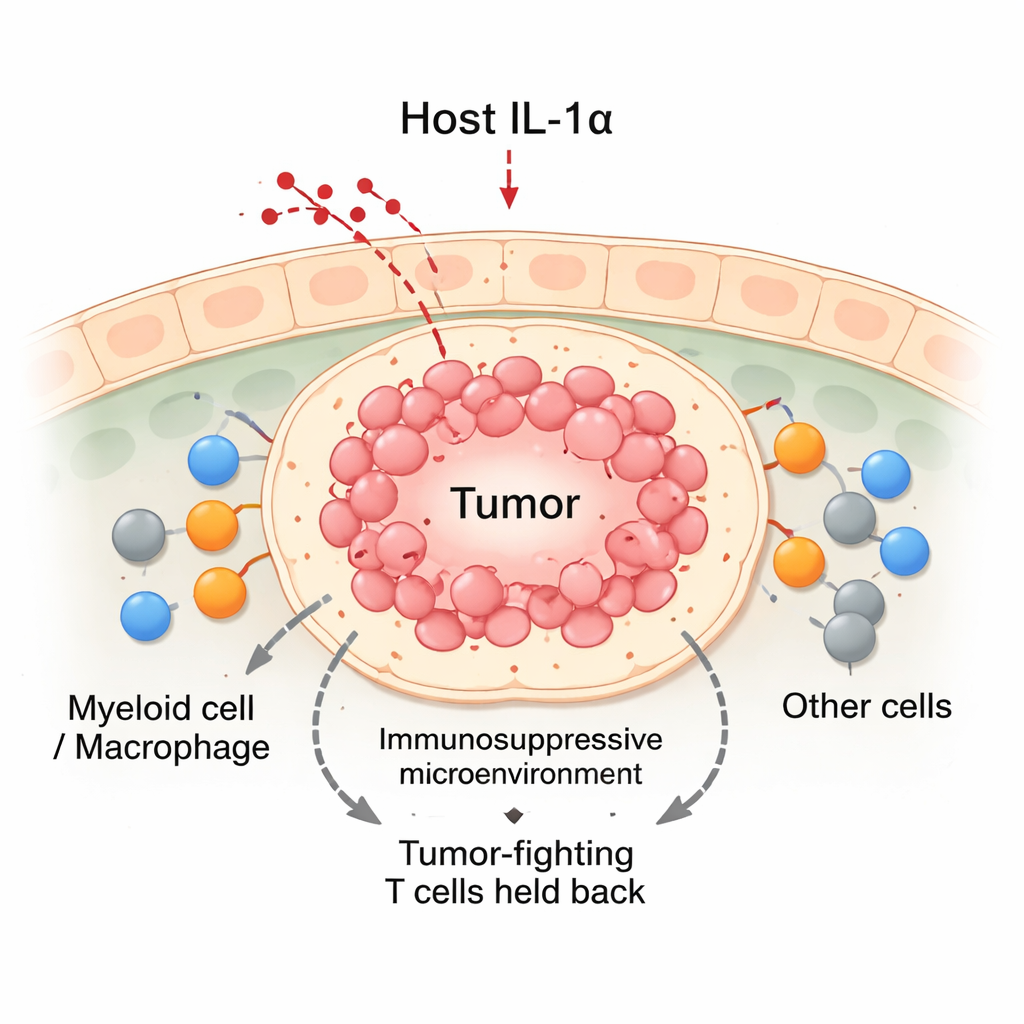
Het uitschakelen van IL‑1α kantelt de balans tegen tumoren
Met muismodellen van borstkanker vergeleek het team normale dieren met dieren die genetisch zo gemodificeerd waren dat ze geen IL‑1α konden produceren. Wanneer borstkankercellen in de melkklieren werden getransplanteerd, groeiden tumoren in normale muizen gestaag. Daarentegen groeiden tumoren in IL‑1α‑deficiënte muizen aanvankelijk ongeveer twee weken en trokken zich daarna vaak terug. Deze regressieve tumoren bevatten in totaal meer immuuncellen, waaronder een toename van CD8 “killer” T‑cellen en myeloïde cellen. Hoewel IL‑1α‑deficiënte muizen minder witte bloedcellen in de circulatie hadden, stapelden ze veel meer immuuncellen op in de tumorplaats. Gedetailleerde analyses lieten zien dat de infiltrerende CD8 T‑cellen in IL‑1α‑deficiënte tumoren actiever waren, hogere niveaus van tumordodende moleculen produceerden en minder tekenen van uitputting vertoonden.
Hoe IL‑1α tumorgeassocieerde myeloïde cellen hervormt
Om te begrijpen wat IL‑1α op cellulair niveau deed, gebruikten de onderzoekers single‑cell RNA‑sequencing om duizenden individuele cellen uit tumoren te onderzoeken. Ze ontdekten dat slechts een kleine subset van tumorgeassocieerde macrofagen — die gemarkeerd zijn door een receptor genaamd CX3CR1 — IL‑1α produceerde. In normale muizen rijpten veel binnenkomende monocyten uit tot deze CX3CR1‑positieve macrofagen, die werden geassocieerd met immuunsuppressief gedrag. In muizen zonder IL‑1α werd deze rijpingsroute verstoord. In plaats daarvan werden myeloïde cellen vaker iNOS‑positieve inflammatoire macrofagen, een profiel dat samenhangt met antitumorale activiteit. Functioneel waren myeloïde cellen uit IL‑1α‑deficiënte tumoren minder goed in staat om remmen zoals PD‑1 en CTLA‑4 op T‑cellen te induceren en toonden ze een zwakkere capaciteit om T‑celproliferatie te dempen.
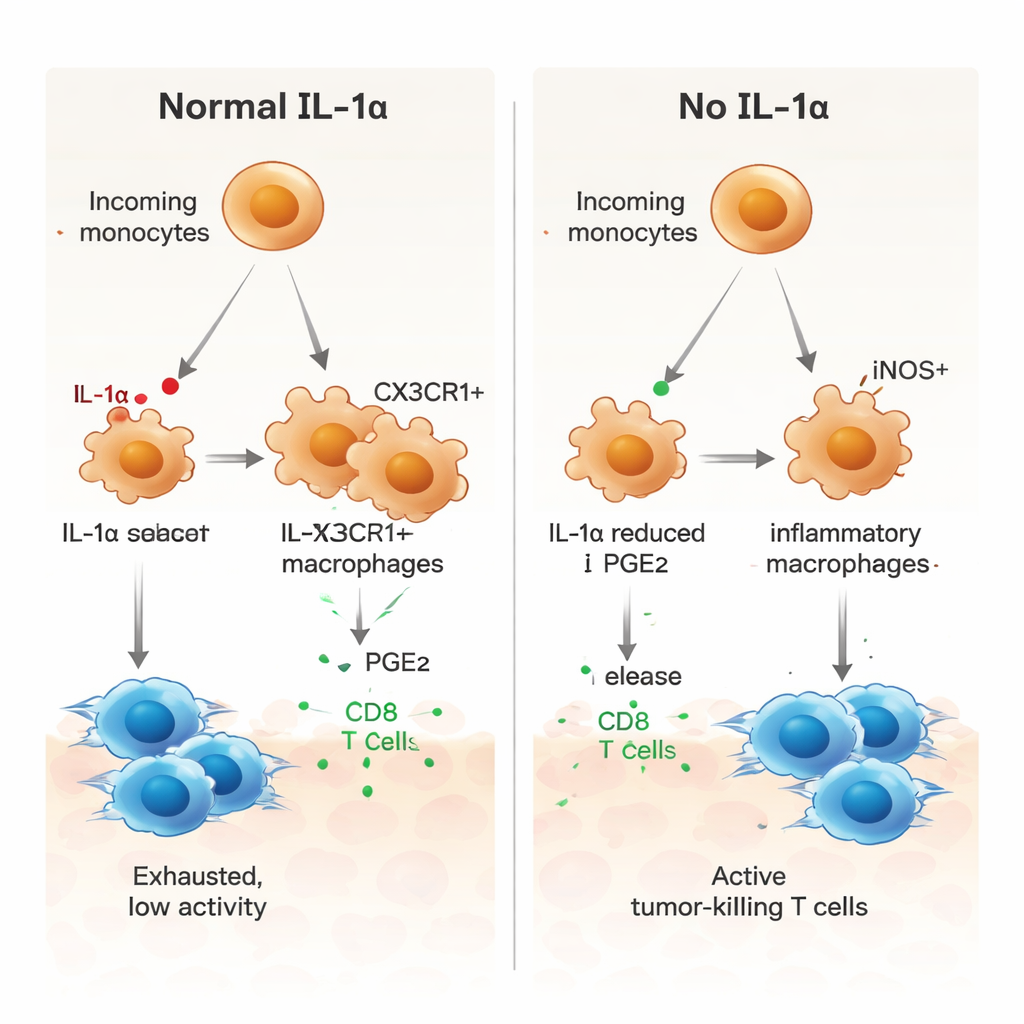
Een sleutelrol voor een lipide‑boodschapper, PGE2
De auteurs onderzochten vervolgens hoe IL‑1α myeloïde cellen richting een tumorondersteunende staat stuurt. Communicatieanalyse van de single‑cell data wees op verschillende signaalroutes, waaronder een pathway met prostaglandine E2 (PGE2), een lipidemediater die bekendstaat om immuunsuppressie te bevorderen. In tumoren zonder IL‑1α bleken macrofagen lagere niveaus van receptoren voor macrofaaggroeifactor (M‑CSF), TGF‑β receptoren en een PGE2‑receptor te uiten, en nabijgelegen stroma‑cellen maakten minder van de enzymen die PGE2 produceren. In kweektoestanden vertoonden uit beenmerg afgeleide macrofagen van IL‑1α‑deficiënte muizen een meer inflammatoir profiel, met hogere iNOS en lagere CX3CR1. Het toevoegen van PGE2 keerde deze verschuiving om en herstelde een meer onderdrukkend patroon, terwijl het blokkeren van PGE2 in normale macrofagen hen naar een pro‑inflammatoire staat dreef. Macrofagen zonder IL‑1α stimuleerden ook sterker de tumor‑specifieke proliferatie van CD8 T‑cellen, een effect dat werd afgezwakt wanneer PGE2 weer werd toegevoegd.
De verbinding tussen muisbevindingen en menselijke immuniteit
Om te bepalen of hun muisgegevens overeenkomen met menselijke biologie, vergeleek het team gen‑handtekeningen van de verschillende muismacrofagen‑subsets met een groot panel van menselijke myeloïde cellen die in het laboratorium richting verschillende staten waren gedreven. Macrofagenclusters uit tumoren van normale muizen leken op menselijke cellen die door moleculen zoals IL‑10, IL‑4 en glucocorticoïden naar M2‑achtige, immuundempende toestanden werden geduwd. Daarentegen kwamen dezelfde clusters uit IL‑1α‑deficiënte tumoren overeen met menselijke cellen in meer inflammatoire, minder onderdrukkende omstandigheden. Opvallend waren genpatronen gekoppeld aan PGE2‑signalering verrijkt in IL‑1α‑afhankelijke macrofagen maar afwezig wanneer IL‑1α ontbrak, wat het idee versterkt dat IL‑1α en PGE2 samenwerken om een immunosuppressief micro‑niche te creëren.
Wat dit zou kunnen betekenen voor toekomstige borstkankertherapie
Kort gezegd suggereert deze studie dat een door de gastheer geproduceerd molecuul, IL‑1α, bepaalde macrofagen stilletjes kan instrueren om de tumor te beschermen en killer T‑cellen in toom te houden, deels via PGE2‑signalering. Wanneer IL‑1α bij muizen wordt verwijderd, verschuiven macrofagen naar een meer inflammatoir, tumoraanvallend profiel, worden CD8 T‑cellen actiever en worden getransplanteerde borstumoren vaak verworpen. Omdat huidige immunotherapieën al gericht zijn op het heractiveren van uitgeputte T‑cellen, zou het combineren hiervan met benaderingen die IL‑1α of de downstream PGE2‑route blokkeren de tumormicro‑omgeving nog meer in het voordeel van het immuunsysteem van de patiënt kunnen kantelen. Hoewel meer onderzoek nodig is om veiligheid en werkzaamheid bij mensen te testen, benadrukken deze bevindingen IL‑1α als een veelbelovend nieuw doel om borstkanker gevoeliger te maken voor immuunaanvallen.
Bronvermelding: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Trefwoorden: immunotherapie bij borstkanker, tumormicro-omgeving, macrofagen, interleukine-1 alfa, prostaglandine E2