Clear Sky Science · nl
Geselecteerde uitroeiing van Staphylococcus aureus-mastitisinfecties met synthetische fage-gebaseerde CRISPR-Cas afleveringssystemen
Strijden tegen een kostbare zuivelinfectie
Melk van koeien en andere landbouwdieren kan worden aangetast door een pijnlijke uierinfectie die mastitis heet, vaak veroorzaakt door de bacterie Staphylococcus aureus. De behandeling van deze infecties vereist doorgaans langdurige kuren met antibiotica, wat duur is, stressvol voor de dieren en bijdraagt aan het groeiende probleem van antibioticaresistentie. Deze studie verkent een radicaal andere benadering: het ombouwen van een natuurlijk virusachtig parasiet van bacteriën tot een precisiewapen dat het DNA van de bacterie selectief kan doorsnijden en infecties kan opruimen zonder resistentiegenen te verspreiden.
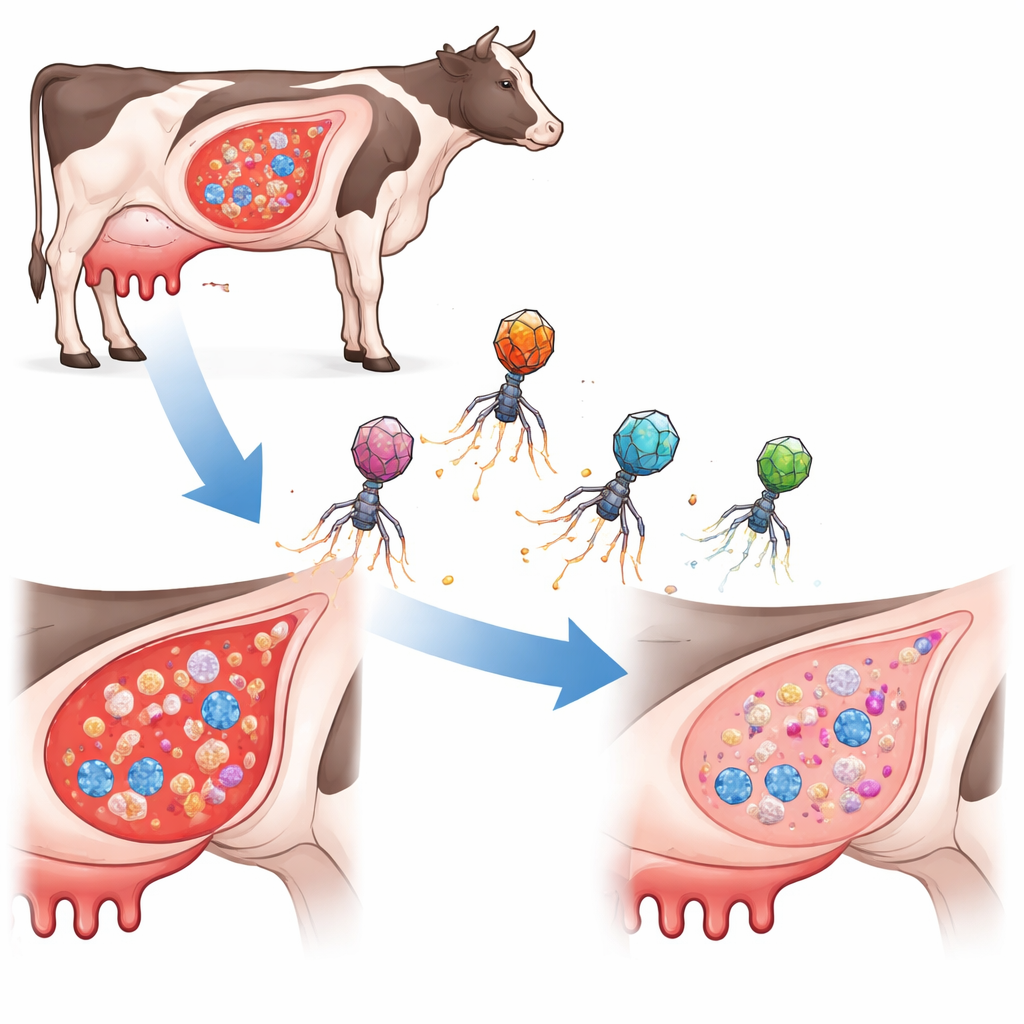
Een nieuw soort gerichte bacteriejager
In plaats van traditionele antibiotica of gewone bacteriofagen (virussen die bacteriën infecteren) te gebruiken, ontwierpen de onderzoekers kleine DNA-dragende elementen die bekendstaan als phage-induceerbare chromosomale eilanden. In de natuur meerijden deze eilanden in fageschillen om tussen bacteriële cellen te springen. Hier bouwde het team ze opnieuw als “ePICIs” die de genbewerkingstool CRISPR-Cas9 dragen plus korte gidssequenties gericht op drie kleine maar belangrijke regulerende RNA’s in S. aureus. Wanneer een ePICI een doelcel binnendringt, wordt Cas9 geproduceerd en knipt het in het chromosoom van de bacterie op de gekozen plaats, waardoor de cel van binnenuit wordt gedood. Cruciaal is dat deze gemodificeerde deeltjes zich niet zelfstandig vermenigvuldigen, wat hun verspreiding beperkt en het risico op het per ongeluk verplaatsen van schadelijke genen verlaagt.
Hoe het bacteriële schild de strijd verandert
S. aureus overleeft behandelingen vaak door biofilms te vormen—plakkerige gemeenschappen waarin cellen zijn ingebed in een zelfgemaakte matrix. Het team vergeleek twee veelvoorkomende typen matrix: één opgebouwd uit een eiwit genaamd Bap en een andere gemaakt van een suikerpolymeer dat bekendstaat als PIA/PNAG. In laboratoriumtesten beschermden Bap-rijke biofilms de bacteriën sterk tegen de ePICIs en tegen een standaard helperfage, en fungeerden ze als een dicht pantser dat infectie blokkeerde. Daarentegen maakten biofilms op basis van het suikerpolymeer de bacteriën makkelijker te doden, waarschijnlijk omdat enzymen op de virusomhulsels deze suikers kunnen afbreken en zo de deeltjes helpen hun doelen te bereiken.
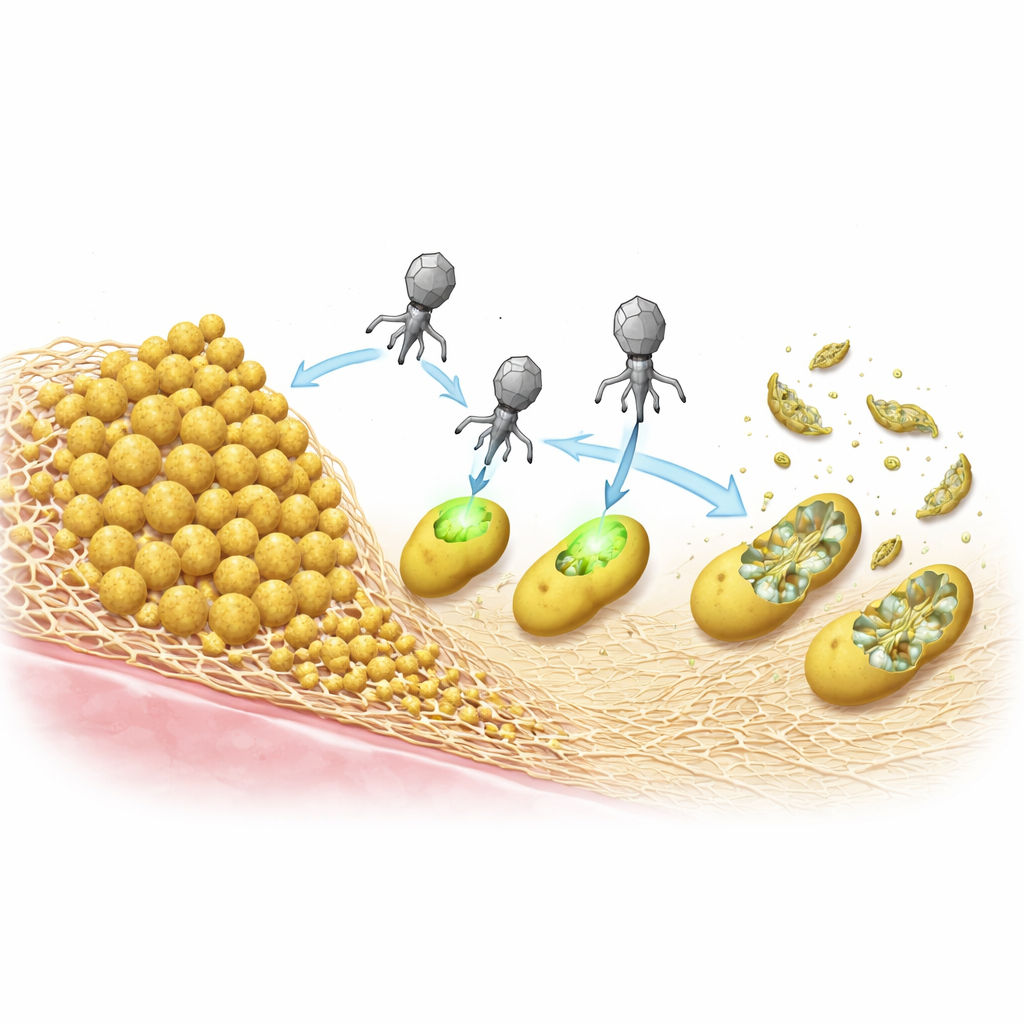
Bacteriën doden zonder hun DNA te fuseren
Eens binnen een cel kunnen ePICIs in het bacteriële chromosoom integreren, maar de onderzoekers vroegen zich af of die stap echt nodig is voor doding. Ze maakten een versie die niet langer kon integreren en toonden aan dat, zolang het deeltje correct werd geproduceerd in de bronstam, het even dodelijk was voor S. aureus als het origineel. Dit betekent dat het CRISPR-systeem direct vanaf het inkomende circulaire DNA kan worden uitgedrukt, zijn werk kan doen en vervolgens verloren gaat als de cel sterft. Die integratievrije werking verkleint bovendien de kans op onbedoelde gentransfer en onderscheidt deze deeltjes van klassieke fagentherapie, die afhankelijk is van virale replicatie en celruptuur om zich te verspreiden.
Van petrischaal naar geïnfecteerde melkklieren
Aangezien Bap-producerende stammen veel voorkomen bij zuivelmastitis, testte het team hun best presterende construct, ePICIrsaE, in een muismodel dat uierinfectie nabootst. In melk en in laboratoriumculturen dempten Bap-rijke biofilms duidelijk de activiteit van ePICI. Toch verminderden herhaalde doses ePICIrsaE in de melkklier het aantal bacteriën sterk voor alle geteste stammen, inclusief diegenen die Bap produceerden. De prestatie was vergelijkbaar met vancomycine, een krachtig antibioticum als laatste redmiddel. De resultaten suggereren dat omstandigheden in levend weefsel—zoals lagere Bap-productie, de aanwezigheid van vrij zwevende bacteriën of hulpzame componenten in melk—de gemodificeerde deeltjes veel beter laten werken dan in statische lab-biofilms.
Wat dit kan betekenen voor boerderijen en verder
De studie toont aan dat niet-replicerende, fage-verpakte CRISPR-systemen S. aureus selectief kunnen elimineren bij een moeilijke, met biofilm verbonden infectie zonder zichzelf te verspreiden of grote aantallen cellen in één keer te laten barsten. Hoewel hoge deeltjesdoses nodig zijn en opschaling van muis naar koe uitdagend zal zijn, bieden deze deeltjes een veelbelovende, beheersbare alternatieve behandeling voor gelokaliseerde infecties zoals mastitis. Breder gezien benadrukt het werk dat behandelingen die in eenvoudige labtesten teleurstellend lijken, toch kunnen slagen in de complexe omgeving van een dier, en het opent de deur naar bibliotheken van op maat gemaakte ePICIs afgestemd op verschillende bacteriën, virale schillen en gidssequenties.
Bronvermelding: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Trefwoorden: rundermastitis, Staphylococcus aureus, CRISPR-therapie, fage-gebaseerde behandeling, biofilminfecties