Clear Sky Science · nl
Realtime, hoogresolutie metabolische karakterisering van levende bacteriën met labelvrije optische metabolische beeldvorming
Germs in realtime zien reageren
Bacteriën zitten overal op en in ons en beïnvloeden stilletjes onze gezondheid. Ze helpen bij de vertering, beschermen onze huid en veroorzaken soms hardnekkige infecties die bestand zijn tegen antibiotica. Deze studie introduceert een manier om levende bacteriën in realtime te observeren terwijl ze op stress en geneesmiddelen reageren, op het niveau van individuele cellen en zonder kleurstoffen of labels toe te voegen. Die mogelijkheid zou artsen op termijn kunnen helpen sneller de juiste behandeling te kiezen en wetenschappers beter kunnen laten begrijpen waarom sommige infecties zo moeilijk te genezen zijn.
Licht als venster op bacterieel leven
In plaats van vlekken of genetische labels toe te voegen, vertrouwen de onderzoekers op het feit dat bacteriën van nature een heel zwak gloeien tonen wanneer bepaalde moleculen in hen door laserlicht worden aangeslagen. Twee van deze moleculen, bekend als NAD(P)H en FAD, spelen een centrale rol in hoe cellen voedsel omzetten in energie. Met snelle, hoogresolutie lasermicroscopie kan het team zowel de helderheid als de kleine tijdvertraging van dit gloeien meten, wat onthult hoe actief de stofwisseling van een cel is. Omdat de methode labelvrij en niet-destructief is, kunnen dezelfde levende bacteriën gedurende seconden tot minuten gevolgd worden terwijl hun omgeving verandert. 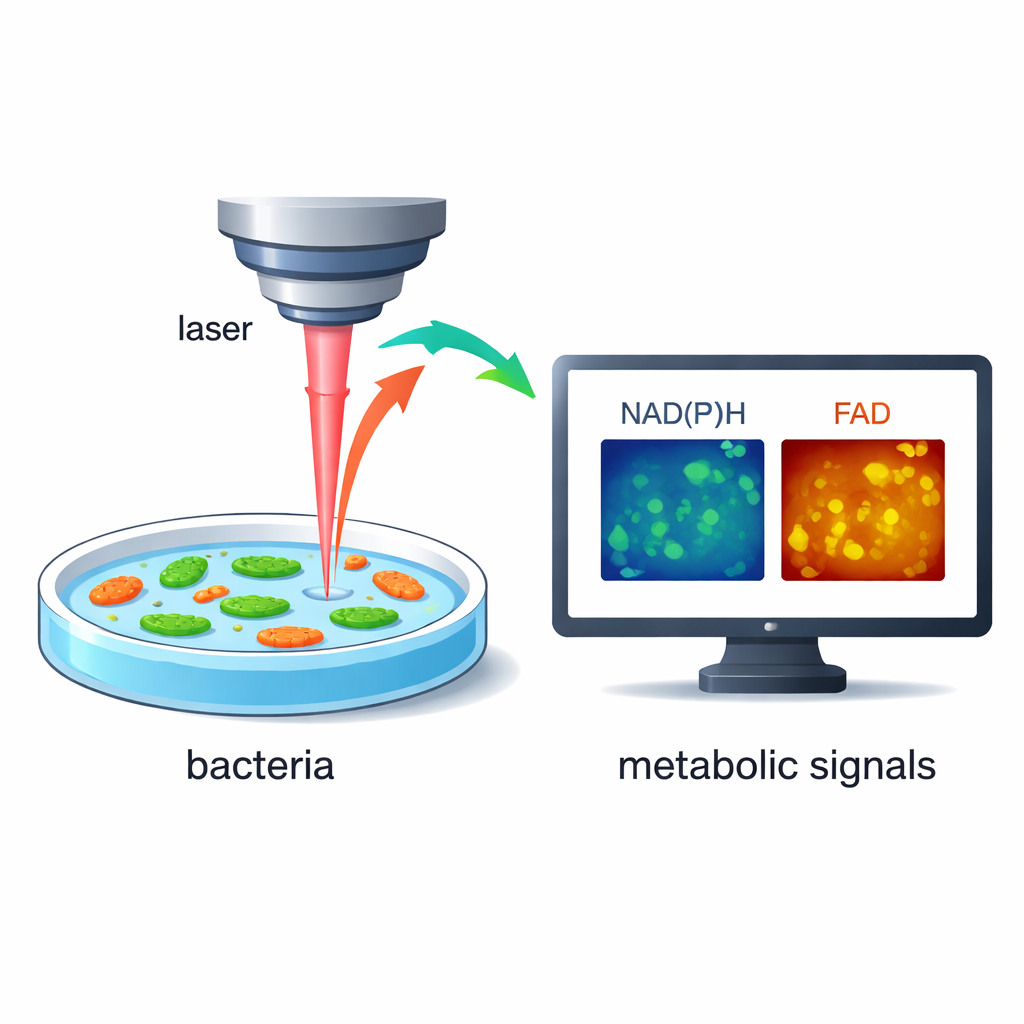
Verschillen tussen individuele bacteriën zien
De meeste standaard labtesten mengen miljoenen bacteriën en geven alleen een gemiddelde respons weer. Hier tonen de auteurs aan dat hun beeldvormingsmethode individuele Staphylococcus aureus‑cellen in vloeibare cultuur kan onderscheiden en elke cel apart kan analyseren, zelfs bij hoge celdichtheden. Toen ze twee kolonies S. aureus vergeleken die onder dezelfde omstandigheden waren gegroeid, verschilde één sleutelsignaal (van FAD) tussen de kolonies, en binnen elke kolonie was er ook een spreiding in waarden. Dit betekent dat zelfs genetisch vergelijkbare bacteriën in hetzelfde flesje in zeer verschillende metabolische staten kunnen verkeren — een verborgen diversiteit die standaard bulktesten kunnen missen maar die van belang kan zijn voor hoe infecties op behandeling reageren.
Antibiotica binnen seconden zien toeslaan
Het team volgde vervolgens individuele S. aureus‑cellen terwijl ze werden blootgesteld aan verschillende antibacteriële behandelingen, waaronder gangbare antibiotica en huishoudbleekmiddel. Met hun snelle beeldvormingsopstelling legden ze veranderingen vast vanaf het moment dat de geneesmiddeldruppel de cellen raakte tot de volgende 30 minuten. Sterke behandelingen veroorzaakten dat NAD(P)H‑signalen daalden en FAD‑signalen stegen, vaak binnen enkele seconden — een afspiegeling van stilgevallen energieproductie en een verschuiving naar een meer geoxideerde toestand in de cel. De precieze timing en het patroon van deze veranderingen hingen af van het type en de dosis van het middel: bijvoorbeeld, eiwitremmende en celwandgerichte antibiotica veroorzaakten een korte dip gevolgd door gedeeltelijk herstel, terwijl bleekmiddel een scherpe, aanhoudende verschuiving teweegbracht. Deze onderscheidende “lichtsignaturen” suggereren dat de techniek niet alleen kan detecteren of cellen onder stress staan of afsterven, maar ook op welke manier ze beschadigd worden. 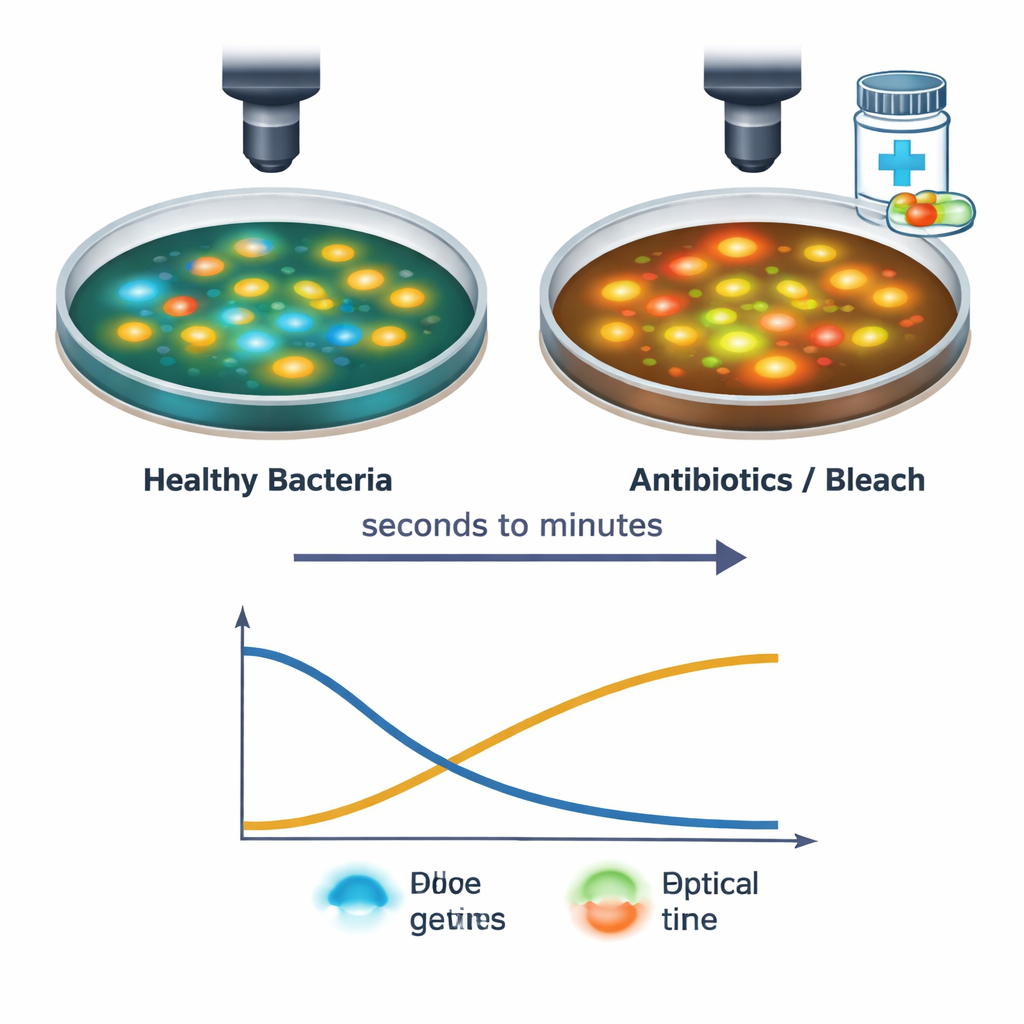
Een kijkje in de verborgen wereld van biofilms
Bacteriën leven in de natuur zelden alleen; in plaats daarvan bouwen ze slijmerige, beschermende gemeenschappen die biofilms worden genoemd, op oppervlakken variërend van medische implantaten tot tanden. In deze dichte lagen kunnen sommige cellen zeer actief zijn terwijl andere in rust verkeren — een mix die de gemeenschap helpt antibiotica te overleven. Met grote aaneengestikte beelden brachten de onderzoekers het metabolische landschap binnen S. aureus‑biofilms in kaart en vergeleken dat met vrijzwemmende cellen. Ze vonden heldere, metabolisch actieve pockets omgeven door minder actieve regio’s en lieten zien dat, over meerdere soorten heen, biofilmbacteriën de neiging hadden een meer geoxideerd metabolisch profiel te vertonen dan hun vrijlevende tegenhangers. Extra optische signalen wezen op meer lipiden en eiwitten, wat overeenkomt met het lijmachtige materiaal dat biofilms bij elkaar houdt.
Waarom dit ertoe doet voor toekomstige geneeskunde
Gezamenlijk tonen deze resultaten aan dat labelvrije optische metabolische beeldvorming snelle, gedetailleerde en niet‑invasieve momentopnames kan leveren van hoe bacteriën leven, zich aanpassen en sterven. Voor de niet‑specialist is de kernboodschap dat wetenschappers nu realtime kunnen “meeluisteren” naar het energieverbruik van bacteriën zonder de cellen te verstoren, met alleen zorgvuldig afgestemd licht. Op de lange termijn zou dit soort technologie kunnen helpen moeilijk te kweken bacteriën te identificeren, drug‑tolerante celletjes binnen biofilms op te sporen of snel te testen hoe de infectie van een patiënt op verschillende antibiotica reageert. Dat kan snellere, meer op maat gemaakte behandelingen ondersteunen en ons begrip verdiepen van de onzichtbare microbiele werelden die onze gezondheid dagelijks beïnvloeden.
Bronvermelding: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
Trefwoorden: bacteriële stofwisseling, optische beeldvorming, biofilms, antibioticarespons, microbioom