Clear Sky Science · nl
Enzymatisch verbeterde antibioticatherapie vermindert biofilms tot ondetecteerbare niveaus in een model van implantaat-geassocieerde infectie
Waarom hardnekkige implantaatinfecties ertoe doen
Heup- en knievervangingen veranderen levens, maar wanneer bacteriën deze metalen implantaten koloniseren, kunnen ze slijmachtige gemeenschappen vormen die biofilms worden genoemd. Deze biofilms werken als versterkte steden die ziekteverwekkers beschermen tegen zowel het immuunsysteem als antibiotica, wat leidt tot pijnlijke, langdurige infecties die zeer moeilijk te genezen zijn. Deze studie onderzoekt een nieuwe, tweetrapsbehandeling die eerst de verdediging van de biofilm helpt ontmantelen en vervolgens het gebied doordrenkt met hoge doses antibiotica—een benadering die mogelijk in de toekomst meer implantaten kan redden in plaats van ze te vervangen.
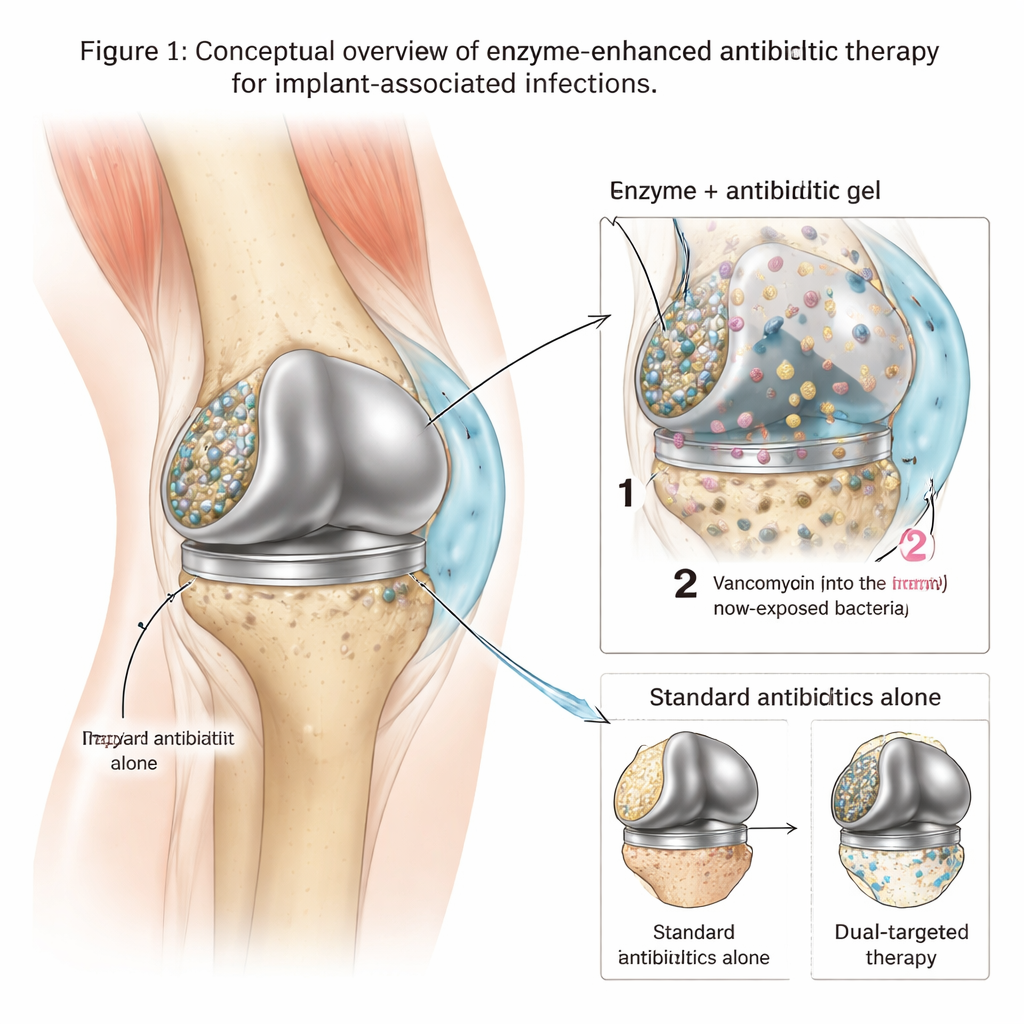
De verborgen bolwerken op metalen implantaten
Wanneer bacteriën zoals methicilline-resistente Staphylococcus aureus (MRSA) zich aan een kunstelijk gewricht hechten, bouwen ze snel een kleverige matrix van DNA, suikers en andere moleculen op het metalen oppervlak. Binnen dit afgeschermde biofilm groeien bacteriën langzaam, veranderen ze hun gedrag en kunnen ze tolereren dat antibioticaniveaus honderden of zelfs duizenden keren hoger zijn dan die welke vrij zwevende ziekteverwekkers doden. Daardoor falen standaardbehandelingen—zelfs sterke middelen zoals vancomycine—vaak in het volledig uitroeien van de infectie, waardoor patiënten meerdere operaties of volledige vervanging van het implantaat moeten ondergaan. Artsen hebben instrumenten nodig die niet alleen bacteriën doden, maar ook hun beschermende bolwerk openbreken zodat de medicijnen ze kunnen bereiken.
Een slimme gel die enzymen en antibiotica aflevert
De onderzoekers ontwierpen een lokale behandeling rond een thermogevoelige hydrogel gemaakt van een verbinding genaamd poloxameer 407. Deze gel is vloeibaar als hij koud is, waardoor hij gemakkelijk rond een implantaat kan worden geïnjecteerd, maar verandert snel in een zachte vaste vorm bij lichaamstemperatuur, waardoor hij op zijn plaats blijft. In deze gel laadde het team twee sleutelingrediënten: een krachtig antibioticum (vancomycine) en een cocktail van drie enzymen die belangrijke componenten van de biofilmmatrix afbreken. In laboratoriumtests stellen ze de gel zo af dat de enzymen eerst vrijkomen—waardoor de biofilm losser en dunner wordt—terwijl vancomycine langzamer over meerdere dagen vrijkomt en zeer hoge lokale medicijnspiegels behoudt precies daar waar de bacteriën leven.
Van petrischaaltjes naar cavia’s
Om te zien of de strategie echt werkte, testte het team die eerst op biofilms die in het laboratorium op titaniumstukjes waren gekweekt en vervolgens in een cavia-model dat geïnfecteerde implantaten nabootst. In vitro verminderden twee toepassingen van de enzym-antibioticumgel, 48 uur uit elkaar, het aantal levende bacteriën op metalen oppervlakken met meer dan 100.000 keer en wisten bijna de gehele biofilmmassa uit. In dieren plaatsten de onderzoekers chirurgisch geperforeerde kooitjes met titaniumparels onder de huid, infecteerden ze met MRSA en behandelden ze vervolgens met verschillende combinaties van systemische antibiotica en lokale gels. Het meest effectieve regime combineerde: (1) de lokale gel met zowel enzymen als vancomycine, tweemaal toegediend, en (2) behandeling over het hele lichaam met vancomycine plus een tweede antibioticum, rifampicine, dat bijzonder goed in biofilms kan doordringen.
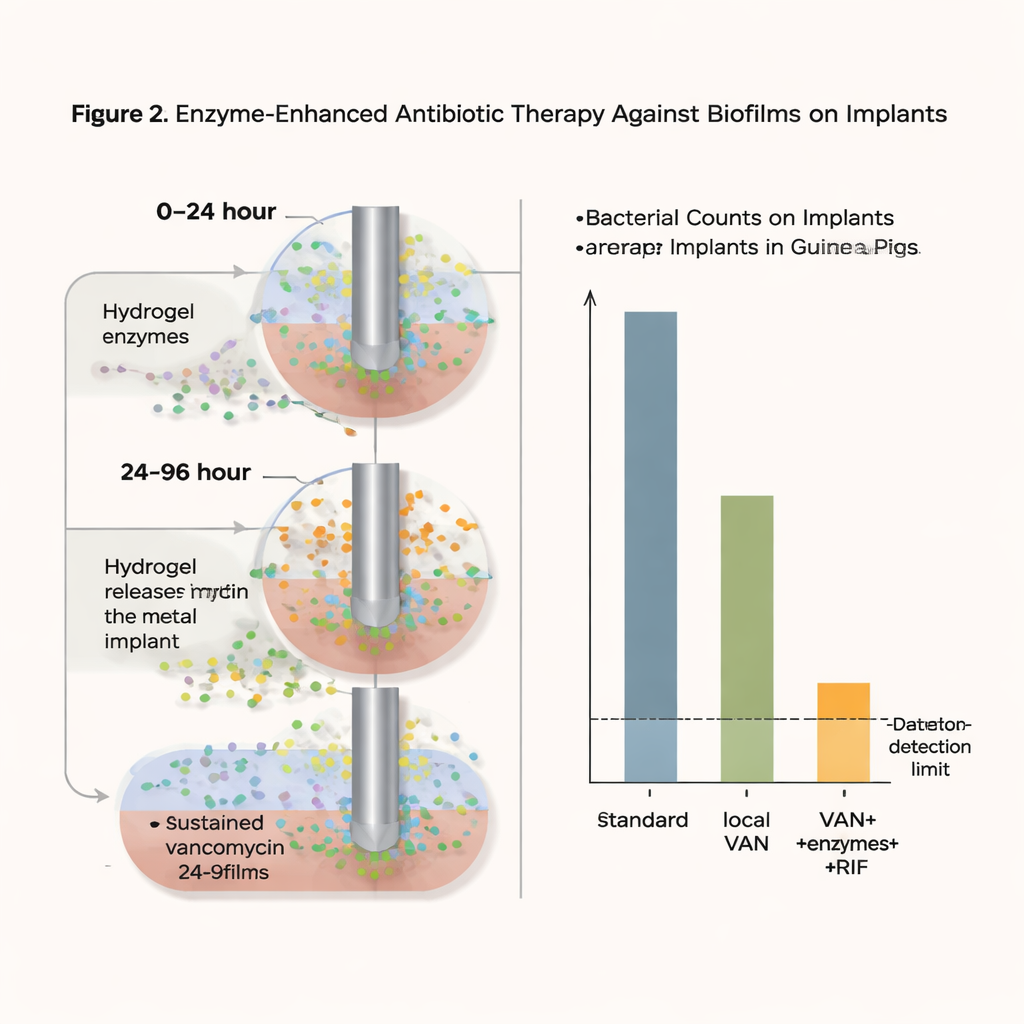
Wat de nieuwe benadering bereikte
Met deze intensieve maar gelokaliseerde strategie daalde het aantal bacteriën op het implantaatmateriaal tot de detectiegrens—effectief “geen terugvindbare bacteriën” in dit model—in 75 procent van de behandelde kooitjes één dag na beëindiging van de therapie, en in 37,5 procent zelfs vijf dagen later. Belangrijk is dat er geen toename van resistentie tegen vancomycine werd waargenomen, en hoge lokale vancomycinespiegels leken het ontstaan van rifampicine-resistente stammen te voorkomen. Veiligheidstests met gekweekte cellen en een gereconstrueerd menselijk huidmodel vonden geen tekenen van toxiciteit of irritatie door de gelformuleringen. Hoewel in sommige gevallen een lichte hergroei van bacteriën bleef optreden en de behandelingsduur korter was dan wat patiënten doorgaans ontvangen, laten de resultaten zien dat het combineren van biofilmontregelende enzymen met aanhoudende lokale antibiotische toediening hardnekkige infecties drastisch kan verkleinen.
Wat dit voor patiënten zou kunnen betekenen
Voor mensen met implantaat-gerelateerde infecties wijst dit werk op een toekomst waarin chirurgen mogelijk een slimme gel rond een geïnfecteerd gewricht injecteren in plaats van direct het implantaat te verwijderen of te vervangen. Door eerst het schild van de biofilm te verzwakken en vervolgens het gebied te overspoelen met hoge, aanhoudende doses antibiotica—ondersteund door behandeling van het hele lichaam—streeft deze dubbelgerichte strategie ernaar het aantal bacteriën tot ondetecteerbare niveaus te drukken en het risico op resistentie te verminderen. Hoewel meer studies, langere behandelingen en klinische proeven bij mensen nog nodig zijn, biedt de aanpak een veelbelovend stappenplan om sommige van de meest hardnekkige orthopedische infecties beter beheersbaar en mogelijk te genezen te maken.
Bronvermelding: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Trefwoorden: biofilminfectie, orthopedische implantaten, vancomycine, enzymtherapie, rifampicine