Clear Sky Science · nl
Een theoretische verkenning van protocollen voor de behandeling van prothese-gewrichtsinfecties met combinaties van antibiotica en bacteriofagen
Waarom infecties van gewrichtsprothesen belangrijk zijn
Heup- en knievervangingen hebben het leven van miljoenen mensen veranderd en stellen hen in staat pijnvrij te lopen. Maar wanneer bacteriën deze kunstgewrichten koloniseren, kunnen ze slijmerige gemeenschappen vormen die biofilms worden genoemd en die zich stevig hechten aan metalen en kunststof oppervlakken. Zodra een biofilm is gevormd, hebben normale antibiotica-doseringen en de afweer van het lichaam vaak moeite om deze te elimineren, wat soms leidt tot extra operaties voor patiënten. Deze studie onderzoekt of het toevoegen van virussen die specifiek op bacteriën jagen — bacteriofagen, of kortweg fagen — aan standaardantibiotica een betere manier kan bieden om deze hardnekkige infecties te behandelen.
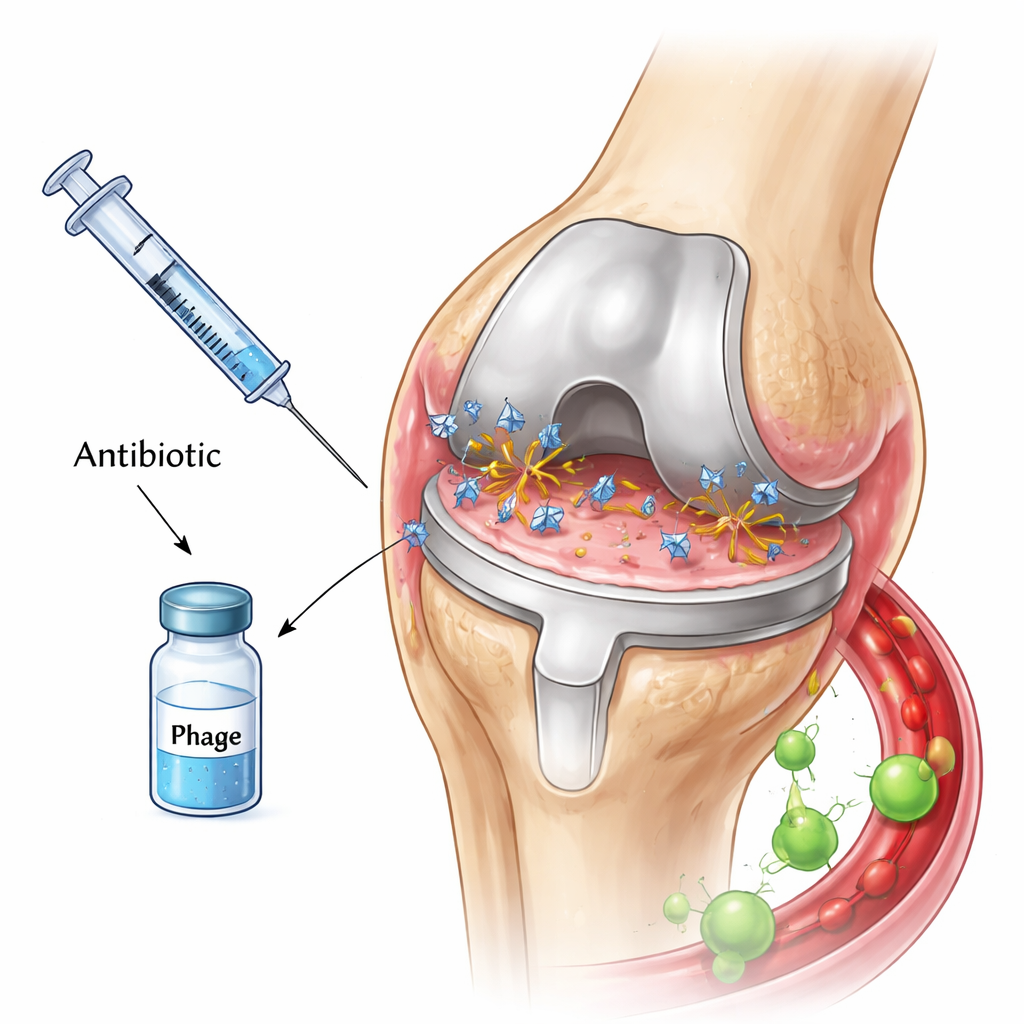
Miniatuurlijke virussen die bacteriën opjagen
Fagen zijn natuurlijke roofdieren van bacteriën. Ze hechten zich aan een bacteriële cel, injecteren hun genetisch materiaal, veranderen de cel in een virusfabriek en laten die uiteindelijk barsten, waarbij een wolk van nieuwe fagen vrijkomt. Sommige fagen dragen ook enzymen die het kleverige materiaal rond biofilms kunnen afbreken, waardoor beschermende lagen worden geopend die bacteriën tegen geneesmiddelen afschermen. Vanwege deze eigenschappen hebben veel onderzoekers gehoopt dat het combineren van fagen met antibiotica een krachtige tweeslag kan vormen tegen infecties van prothesen, vooral wanneer bacteriën resistent worden tegen de middelen.
Infecties bouwen in een computer
In plaats van direct over te gaan op proefdieren of klinische onderzoeken, bouwden de auteurs eerst een gedetailleerd wiskundig en computermodel van een prothese-gewrichtsinfectie. Hun virtuele systeem had twee hoofdzones: vrij zwevende bacteriën in lichaamsvloeistoffen en bacteriën ingebed in een biofilm op het implantaatoppervlak. Het model hield ook immuuncellen, voedingsstoffen voor bacteriegroei, antibiotica en fagen bij, die allemaal in en uit het gewricht bewogen. Door omstandigheden te wijzigen zoals medicijndosering, timing en de aanwezigheid van antibiotica-resistente bacteriën, konden ze vele behandelingsstrategieën onderzoeken die moeilijk, langzaam of duur zouden zijn om bij echte patiënten te testen.
Wanneer geneesmiddelen alleen en samen werken
De simulaties toonden aan dat noch het immuunsysteem noch antibiotica alleen biofilm-infecties gemakkelijk uitroept. Antibiotica verminderden de vrijzwevende bacteriën sterk, maar deden nauwelijks iets met de biofilmpopulatie. Fagen konden de infectie in eerste instantie effectiever onder controle krijgen, maar introduceerden ook boom-en-bustcycli: zodra fagen bacteriën doodden, werden hun prooien te schaars, waardoor het aantal fagen daalde en de bacteriën weer konden terugveren. Wanneer antibiotica en fagen gelijktijdig werden toegediend, domineerde het antibioticum vaak het resultaat, en voegde het bijgeven van fagen vaak weinig toe boven wat het antibioticum al kon bereiken.
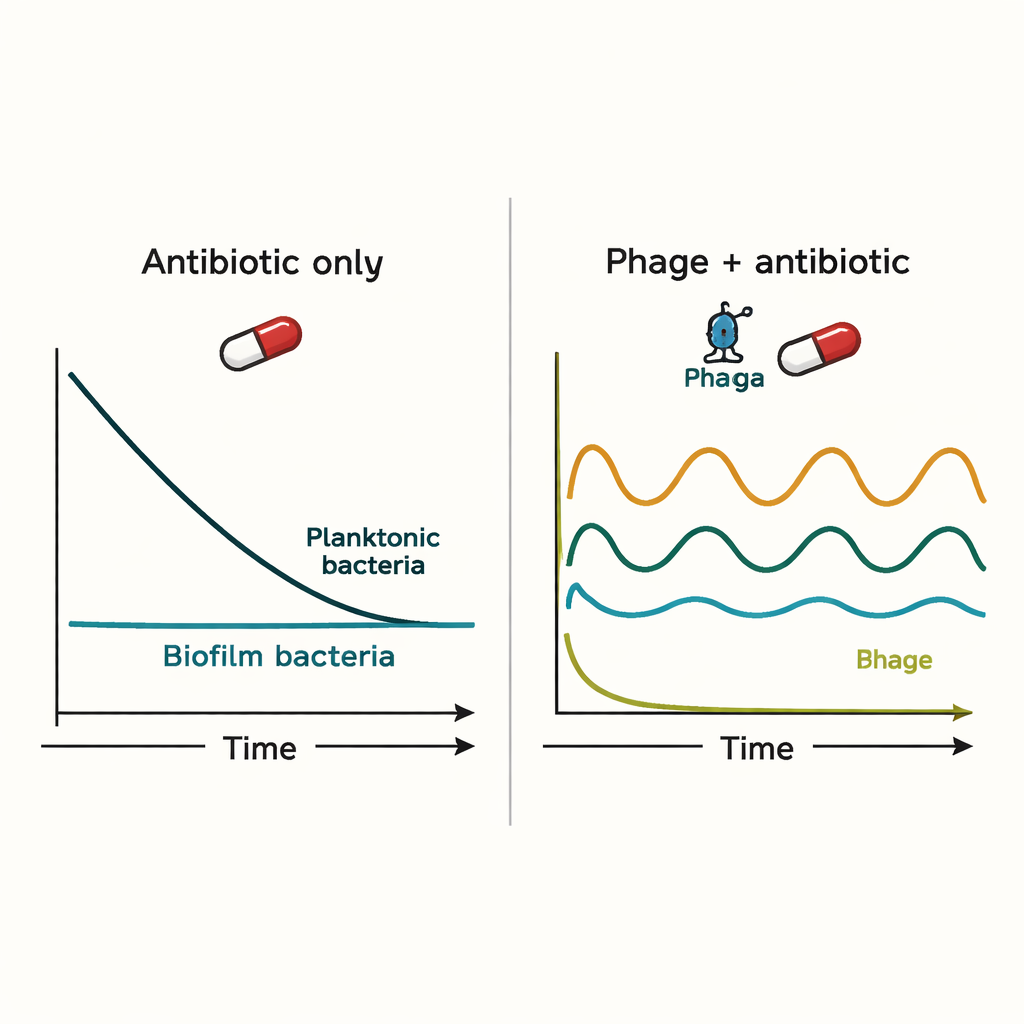
De speciale rol van timing en resistentie
Het model werd optimistischer toen antibiotica-resistente bacteriën werden meegenomen. Fagen konden deze resistente cellen aanvallen en ze soms volledig verwijderen. Als de faagbehandeling eerst begon en antibiotica enkele uren later werden toegevoegd, verminderde de gecombineerde strategie de vrijzwevende bacteriën met vele ordegroottes en werden resistente subpopulaties in de simulaties uitgeroeid. Zelfs dan werden de biofilm-geassocieerde bacteriën niet volledig uitgedelgd; hun aantallen werden op lagere niveaus gehouden die mogelijk gemakkelijker door het immuunsysteem te beheersen zijn. Dit suggereert dat fagen waarschijnlijk het meest nuttig zijn niet als wondermiddeltjes, maar als hulpverleners die resistentie voorkomen en infecties onder controle houden.
Wat dit betekent voor patiënten en artsen
Voor mensen met een geïnfecteerde gewrichtsprothese biedt dit werk zowel voorzichtigheid als hoop. Het model suggereert dat het simpelweg toevoegen van fagen aan standaardantibiotica waarschijnlijk niet op zichzelf diepe biofilm-infecties zal genezen. Fagen kunnen echter nog steeds waardevolle middelen zijn: ze kunnen helpen antibiotica-resistente bacteriën uit te roeien en het totale aantal kiemen zo ver te verminderen dat het lichaam het aankan, vooral als ze vóór of zorgvuldig getimed met antibiotica worden gebruikt. De auteurs benadrukken dat dit theoretische voorspellingen zijn, geen klinisch bewijs. Hun belangrijkste boodschap is dat doordachte experimenten — geleid door modellen zoals dit — nodig zijn om te ontdekken wanneer faagtherapie werkelijk de uitkomsten voor patiënten met prothese-gewrichtsinfecties kan verbeteren.
Bronvermelding: Levin, B.R., Gil-Gil, T., Berryhill, B.A. et al. A theoretical exploration of protocols for treating prosthetic joint infections with combinations of antibiotics and bacteriophage. npj Biofilms Microbiomes 12, 51 (2026). https://doi.org/10.1038/s41522-025-00908-2
Trefwoorden: infectie van een gewrichtsprothese, biofilm, bacteriofaagtherapie, antibioticaresistentie, wiskundige modellering