Clear Sky Science · nl
Fasen van biomoleculaire condensaatvorming bij pro-β-carboxysoomassemblage
Waarom piepkleine koolstoffabriekjes ertoe doen
De voedselketens op aarde zijn afhankelijk van fotosynthese, maar het sleutelenzym dat kooldioxide (CO2) uit de lucht haalt, Rubisco, is traag en raakt gemakkelijk verward door zuurstof. Cyanobacteriën – microscopische, fotosynthetische microben – hebben dit probleem lang geleden opgelost door eiwit-„microfabriekjes” te bouwen, carboxysomen genoemd, die CO2 rond Rubisco vasthouden. Deze studie ontrafelt hoe een cruciaal adaptorcomplex, bestaande uit de eiwitten ApN en CM, zich in fasen zelf assembleert om te helpen een werkend carboxysoom op te bouwen. Inzicht in dit ‘choreograferen’ kan pogingen sturen om vergelijkbare CO2-versterkende systemen in gewassen te installeren en zo de opbrengst te verhogen.
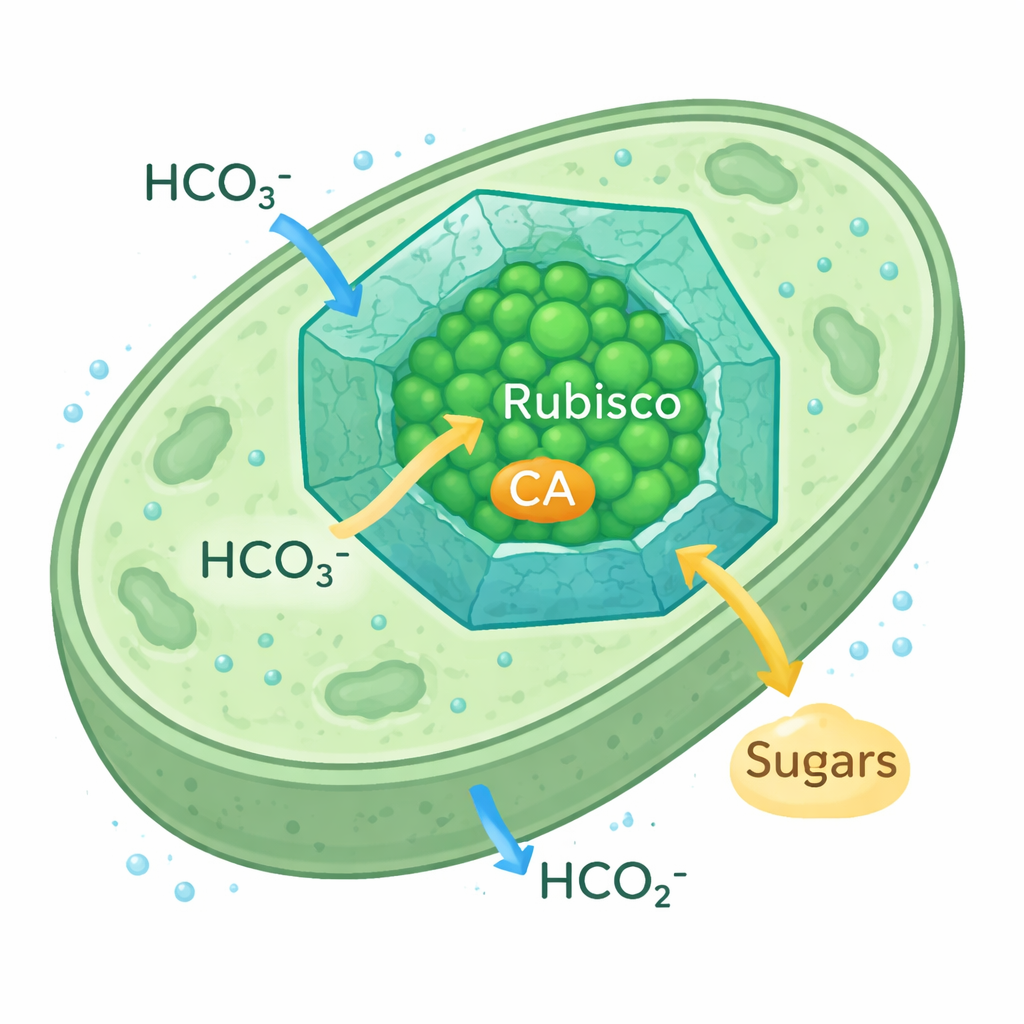
Hoe microben koolstofvangst superchargen
Cyanobacteriële carboxysomen zijn kleine, icosaëdrische eiwitcompartimenten in de cel. Hun eiwitmantel laat bicarbonaationen binnen terwijl het ontsnappen van CO2 wordt vertraagd, waardoor zich een CO2-rijke bubbel rond Rubisco en zijn partnerenzym, carbonic anhydrase (CA), vormt; CA zet bicarbonaat om in CO2. Dit CO2-concentrerende mechanisme stelt cyanobacteriën in staat te gedijen zelfs wanneer de omgevings-CO2 schaars is. Omdat de Rubisco-vorm die in deze carboxysomen wordt gebruikt op plant-Rubisco lijkt, zien onderzoekers ze als een realistisch model om plantenchloroplasten zodanig te herontwerpen dat ze koolstof efficiënter vangen.
Het puzzelstukje dat met de mantel praat
Voordat de harde eiwitmantel zich vormt, bouwen cyanobacteriën eerst een zacht, druppelachtig „pro-carboxysoom”-condensaat. Eerder werk toonde aan dat een scaffold-eiwit genaamd CM Rubisco en CA samenbrengt in deze druppel. De ontbrekende schakel was hoe het mantel-adaptoreiwit ApN zich bij deze structuur voegt en later verbinding maakt met mantelproteïnen. De auteurs vonden dat wanneer ApN alleen wordt geproduceerd, het een viervoudige bundel vormt die de andere carboxysoomcomponenten negeert. In deze staat kan ApN niet in druppels met Rubisco, CM en CA worden getrokken, wat suggereert dat tijdens de echte carboxysoomassemblage een andere vorm van ApN wordt gebruikt.
Gezamenlijk gebouwde adaptors en een redox-schakelaar
Door naar de genetische indeling in cyanobacteriën te kijken, merkte het team op dat apn direct achter cm in hetzelfde operon ligt, zodat de twee eiwitten meestal samen worden gemaakt. Het nagebootst in bacteriën door ApN en CM vanaf een gedeeld stuk DNA mede-expressief te maken. Onder deze omstandigheden vormde ApN geen zelfstandige tetramer meer. In plaats daarvan assembleerden drie ApN-subunits en één CM-subunit tot een specifiek viervoudig adaptorcomplex, aangeduid als (ApN)3:CM. Dit hetero-complex hechte gemakkelijk aan Rubisco, CA en CM en kon condensaten binnengaan. Structurele modellering en cryo-elektronenmicroscopie toonden dat ApN en CM elkaar ontmoeten via een fijn afgestelde „tong-en-groef”-interface; wanneer sleutelresiduen van ApN in deze interface werden gemuteerd, kon het adaptor niet vormen en faalden cellen in het bouwen van correcte carboxysomen.
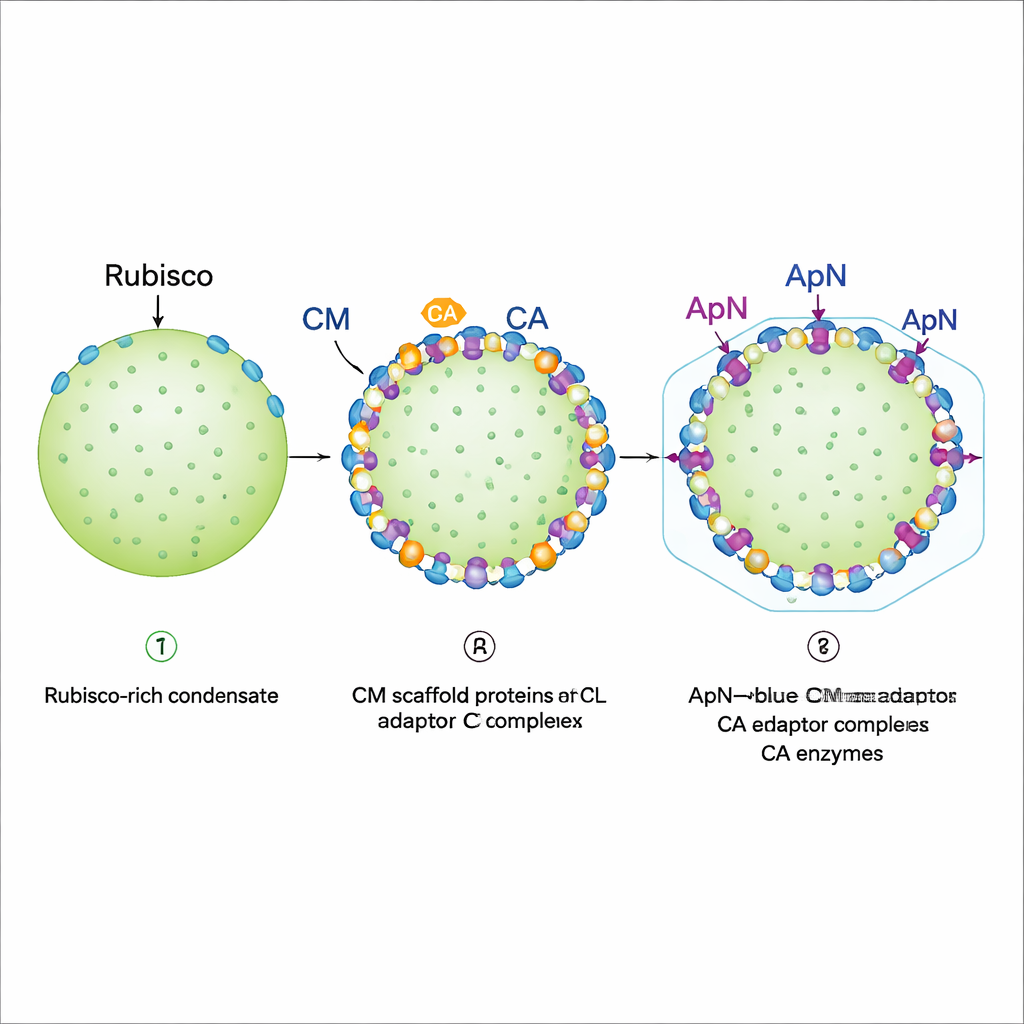
Plaatsing aan de rand en voorbereiding op de mantel
Fluorescentiebeeldvorming van gereconstitueerde druppels onthulde een stapsgewijs assemblageprogramma. Eerst vormen Rubisco, full‑length CM en een kortere CM-variant een dicht condensaat dat zich gedraagt als een gel: Rubisco zit feitelijk vast. Vervolgens worden CA en het (ApN)3:CM-complex toegevoegd. Beide gaan bij voorkeur aan de buitenrand van de bestaande druppel zitten, mits CA arriveert vóór of tegelijkertijd met (ApN)3:CM. Deze randlokalisatie is cruciaal omdat de staart van ApN een „encapsulatiepeptide” draagt dat aan mantelproteïnen bindt. De auteurs ontdekten ook een ingebouwde redox-schakelaar: naarmate het interieur van het rijpende carboxysoom oxiderender wordt, kunnen twee geconserveerde cysteïneresiduen in ApN geoxideerd raken, waardoor het adaptor wordt aangespoord van een (ApN)3:CM-tetramer naar een (ApN)2:CM-trimer. In levende cyanobacteriële cellen vertraagde het wijzigen van deze cysteïnes de groei en produceerde grotere maar nog steeds functionele carboxysomen, wat hun rol in het fijnstellen van rijping onderstreepte.
Lessenaars voor het bouwen van betere gewassen
Voor niet‑specialisten kunnen deze moleculaire details vergezocht klinken, maar ze komen neer op een eenvoudige boodschap: timing en partnerschap zijn belangrijk. Het werk toont aan dat ApN samen met CM moet worden geproduceerd om te voorkomen dat het een nutteloze zelf-cluster vormt en in plaats daarvan een adaptor wordt die zich op het oppervlak van het pro-carboxysoom parkeert, klaar om de mantel te rekruteren. Een redox‑gevoelige stap helpt vervolgens dit adaptor te herstructureren naarmate het compartiment sluit en de interne chemie verandert. Voor plantkundigen die hopen cyanobacteriële CO2-concentrerende machinerie in gewassen te transplanteren, benadrukt de studie dat het niet volstaat om individuele onderdelen te verplaatsen; men moet ook de volgorde, verhoudingen en chemische triggers respecteren die de carboxysoomassemblage in de natuur sturen.
Bronvermelding: Zang, K., Hong, X., Nguyen, N.D. et al. Stages of biomolecular condensate formation in pro-β-carboxysome assembly. Nat. Plants 12, 447–464 (2026). https://doi.org/10.1038/s41477-026-02227-6
Trefwoorden: carboxysoomassemblage, cyanobacterieel CO2-concentrerend mechanisme, Rubisco-condensaten, biomoleculaire condensaten, synthetische fotosynthese