Clear Sky Science · nl
Meerdimensionale moleculaire profilering verheldert de diagnose en gerichte therapie van desmoplastische kleinrondecele tumor
Een zeldzame kanker die betere antwoorden nodig heeft
Desmoplastische kleinrondecele tumor (DSRCT) is een uitermate zeldzame en agressieve kanker die vooral kinderen, tieners en jongvolwassenen treft. Omdat hij zo ongebruikelijk is en onder de microscoop andere tumoren kan nabootsen, hebben artsen vaak moeite om de juiste diagnose te stellen en effectieve behandelingen te kiezen. Deze studie stelt een eenvoudige maar krachtige vraag: als we DSRCT-tumoren diepgaand analyseren op meerdere moleculaire niveaus — niet alleen DNA, maar ook RNA, eiwitpatronen en chemische labels op DNA — kunnen we dan zowel de diagnose aanscherpen als nieuwe, meer precieze behandelingsopties onthullen voor patiënten van wie de standaardtherapieën zijn uitgeput?
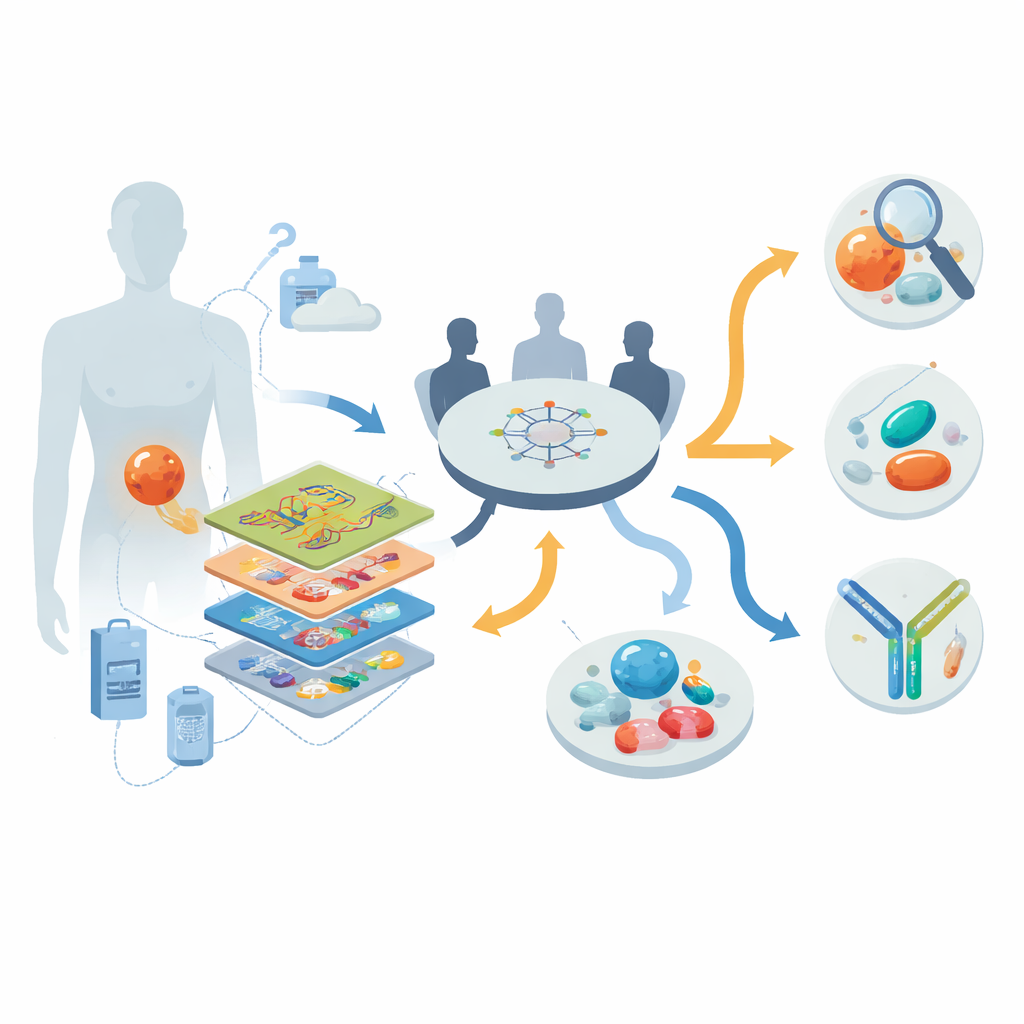
In tumors kijken, laag voor laag
De onderzoekers werkten binnen een landelijk precisie-oncologieprogramma in Duitsland en schreven tussen 2013 en 2022 dertig mensen met gevorderde, meestal therapieresistente DSRCT in. Voor elke patiënt pasten ze een “multi-omics”-gereedschapsset toe: whole-genome of exoomsequencing om het DNA te onderzoeken; RNA-sequencing om te zien welke genen actief zijn; DNA-methyleringsprofilering om epigenetische vingerafdrukken vast te leggen; en bij negen patiënten gedetailleerde metingen van eiwitten en fosfo-eiwitten die onthullen welke signaleringsroutes daadwerkelijk actief zijn. Een multidisciplinair tumordiscussiepanel besprak deze gegevens samen met de klinische geschiedenis van iedere patiënt om geïndividualiseerde aanbevelingen te formuleren voor diagnoseverduidelijking, gerichte medicijnen en klinische onderzoeken.
Foute diagnosen corrigeren en verborgen doelen onthullen
Een opvallende bevinding was hoe vaak diepgaande profilering de oorspronkelijke diagnose corrigeerde. Bij acht van de 30 patiënten werden tumoren die aanvankelijk als andere entiteiten waren aangeduid — zoals kanker van onbekende oorsprong of vaag gedefinieerde sarcomen — opnieuw geclassificeerd als DSRCT zodra een kenmerkende genfusieregel (EWSR1::WT1) en een karakteristiek methyleringspatroon werden geïdentificeerd. Tegelijk bleek het DNA van deze tumoren relatief rustig: er waren weinig mutaties en slechts af en toe veranderingen in kopieaantal, zodat klassieke “gemuteerd gen = geneesmiddeldoel”-benaderingen weinig opleverden. In plaats daarvan kwamen de rijkste aanwijzingen uit de RNA- en eiwitlagen. Door genactiviteit in DSRCT te vergelijken met honderden andere sarcomen, vond het team herhaalde overexpressie van meerdere oppervlaktemoleculen en signaalenzymen die in principe bestreden zouden kunnen worden met bestaande of opkomende geneesmiddelen.
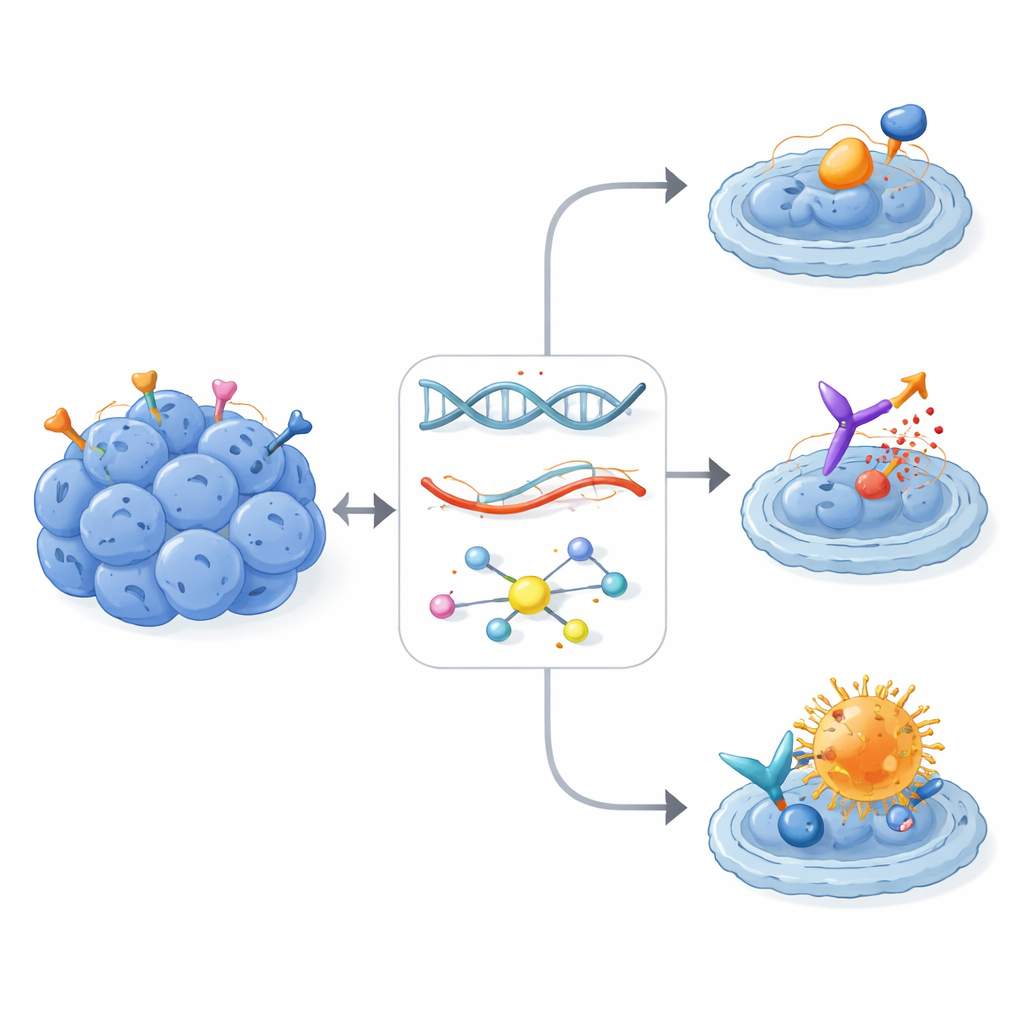
Van moleculaire signalen naar op maat gemaakte behandelingen
Op basis van deze patronen gaf het tumordiscussiepanel 107 moleculair geïnformeerde behandeladviezen voor 28 van de 30 patiënten. De meeste aanbevelingen betroffen middelen die tyrosinekinasen blokkeren — sleutelenzymen die celgroei en de vorming van bloedvaten aansturen — of nieuwere strategieën die zich hechten aan sterk tot expressie gebrachte oppervlaktemoleculen. Voorbeelden waren klein-molecuulkinaseremmers zoals pazopanib; peptide-gebaseerde bestraling gericht op somatostatine-receptoren; experimentele CAR-T-cellen die het adhesiemolecuul CLDN6 targeten; en antistof–geneesmiddelconjugaten die toxines afleveren aan cellen met de ERBB2 (HER2)-receptor. Zeventien patiënten kwamen in aanmerking voor biomarker-gematchte klinische trials, wat onderstreept hoe gedetailleerde moleculaire data toegang kunnen openen tot studies die anders moeilijk bereikbaar zouden zijn voor mensen met een ultra-zeldzame ziekte.
Reële impact bij zwaar voorbehandelde patiënten
Van alle aanbevolen gepersonaliseerde therapieën werden er 16 daadwerkelijk gegeven aan 13 patiënten, allemaal gestuurd door signalen op RNA-niveau en soms verfijnd door fosfo-eiwitgegevens. Ondanks dat deze personen al meerdere ronden chemotherapie en lokale behandelingen hadden ondergaan, bereikten acht van de 13 ziektecontrole — vijf met gedeeltelijke tumorkrimp en drie met stabiele ziekte. Multi-target tyrosinekinaseremmers, meestal pazopanib, leverden bij meerdere patiënten betekenisvolle en soms langdurige voordelen op, vooral wanneer de bekende doelen van het middel duidelijk overactief waren in de tumor. Misschien het meest opmerkelijk waren twee patiënten met hoge ERBB2-expressie die het antistof–geneesmiddelconjugaat trastuzumab deruxtecan (T-DXd) kregen. Beide rapporteerden langdurige responsen tot twee jaar of langer, ondanks dat ze veel eerdere behandelrondes hadden uitgeput en ondanks dat de ERBB2-receptor niet het sterke activatiepatroon liet zien dat doorgaans vereist is voor klassieke ERBB2-blokkerende middelen.
Wat dit betekent voor patiënten en toekomstige zorg
Voor mensen met DSRCT biedt de studie een behoedzaam optimistische boodschap. Hoewel deze kanker weinig duidelijke DNA-mutaties heeft om uit te putten, kan het kijken over meerdere moleculaire lagen zowel foutieve diagnosen corrigeren als handelbare kwetsbaarheden onthullen die standaardtests onzichtbaar laten. Het werk toont aan dat, zelfs bij een zeldzame en agressieve ziekte, een biologie-gestuurde aanpak reële klinische voordelen kan opleveren, inclusief duurzame responsen op middelen zoals pazopanib en trastuzumab deruxtecan. Breder gezien pleit het ervoor dat patiënten met DSRCT — en bij uitbreiding andere ultra-zeldzame kankers — zouden profiteren van routinematige toegang tot uitgebreide moleculaire profilering en deskundige beoordeling, waarmee de weg wordt vrijgemaakt voor toekomstige trials waarin behandelingen niet alleen op tumortype worden gekozen, maar op de unieke moleculaire vingerafdrukken van ieders kanker.
Bronvermelding: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
Trefwoorden: desmoplastische kleinrondecele tumor, precisie-oncologie, multi-omics profilering, gerichte therapie, antistof-geneesmiddelconjugaten