Clear Sky Science · nl
Samenspel van SLC33A1-afhankelijke en -onafhankelijke Golgi O-acetylatie van siaalzuur in CASD1-katalyse
Hoe kleine suikerwijzigingen gezondheid en ziekte kunnen beïnvloeden
Onze cellen zijn omgeven door complexe suikerketens die fungeren als moleculaire identificatiekaarten en zo immuunrespons, ontwikkeling en zelfs de manier waarop virussen zich hechten sturen. Deze studie onderzoekt een subtiele maar krachtige wijziging van die suikers — het toevoegen van kleine chemische “kapjes” genaamd acetylgroepen aan een uiteindelijke suiker genaamd siaalzuur — en onthult een verrassend tweedelig moleculair systeem dat dit proces binnen het Golgi-apparaat van de cel regelt. Inzicht in dit verborgen systeem helpt bepaalde ernstige neurologische aandoeningen te verklaren en geeft aanwijzingen over hoe cellen hun oppervlak in gezondheid en ziekte fijnregelen. 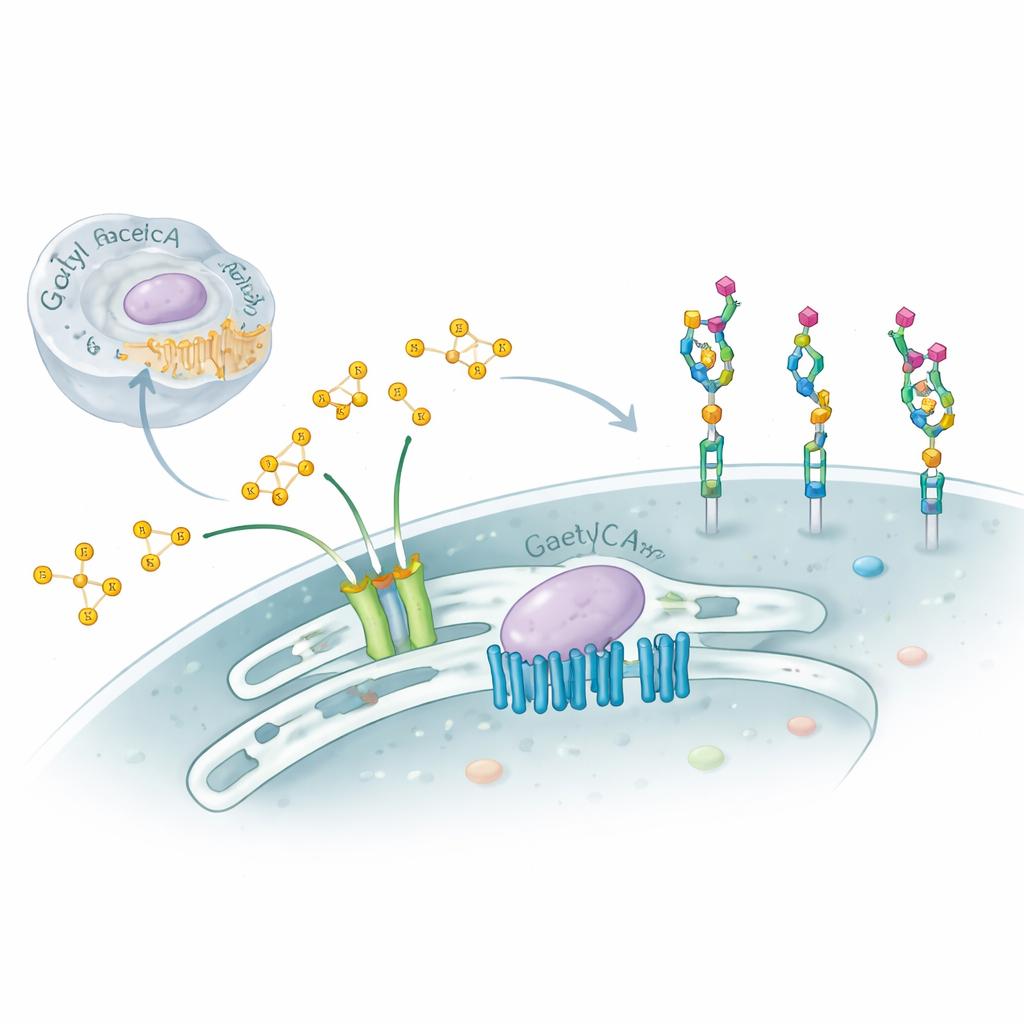
De bijzondere suikers aan het celoppervlak
Siaalzuren zitten aan de buitenste uiteinden van veel celoppervlakte-sugars op eiwitten en lipiden, met name op moleculen die in de hersenen gangliosiden worden genoemd. Door siaalzuren licht te wijzigen — bijvoorbeeld door één of twee acetylgroepen op specifieke posities toe te voegen — kunnen cellen bestaande herkenningsplaatsen maskeren of nieuwe creëren. Virussen zoals influenza C en sommige coronavirussen zoeken specifiek naar deze gewijzigde suikers, en geacetyleerde gangliosiden kunnen beïnvloeden of zenuwcellen overleven of afsterven, evenals hoe tumoren groeien. Ondanks hun belang waren de werkingsmechanismen van het cellulaire machinerie dat deze acetylgroepen in het Golgi plaatst slecht begrepen.
Een transporter en een enzym werken samen
De onderzoekers concentreerden zich op twee eiwitten die zich in of rond het Golgi bevinden: SLC33A1, een transporter die acetyl‑CoA (de belangrijkste acetyldonor van de cel) over membranen verplaatst, en CASD1, een enzym dat bekendstaat om het overdragen van acetylgroepen naar siaalzuren. Met genbewerking in menselijke en hamstercellijnen verwijderden ze SLC33A1 en onderzochten wat er met specifieke gangliosiden gebeurde. Cellen zonder SLC33A1 konden nog steeds de basale gangliosiden GD3 en GD2 maken, maar verloren volledig hun 9‑O‑geacetyleerde vormen, een kenmerkende modificatie die wordt gekoppeld aan kanker en neurale functie. Het herintroduceren van menselijk SLC33A1 herstelde deze geacetyleerde gangliosiden, wat aantoont dat SLC33A1 een cruciale leverancier van acetyl‑CoA voor deze route is. 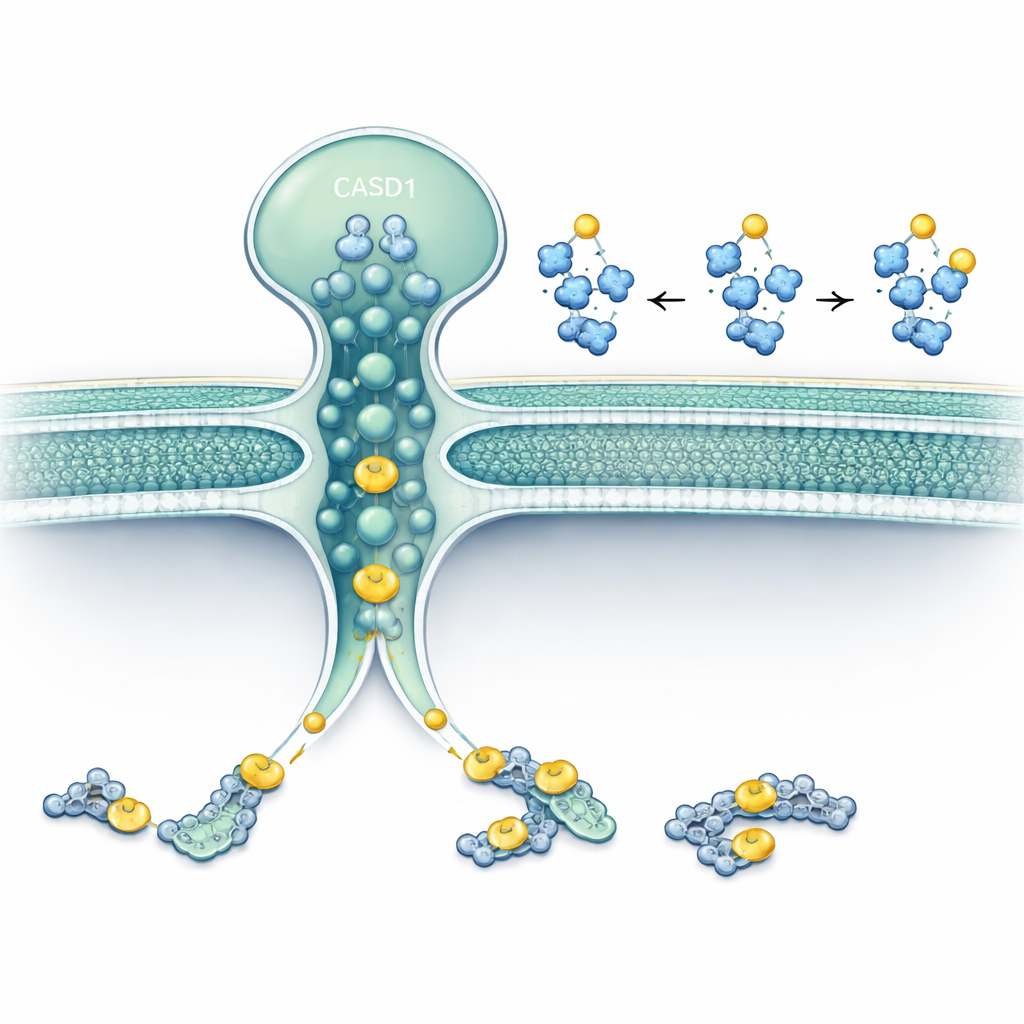
Patiëntmutaties tonen medische relevantie
SLC33A1 is geïmpliceerd in meerdere zeldzame neurologische aandoeningen, waaronder een ernstige kinderziekte (Huppke–Brendel-syndroom), een vorm van erfelijke spastische paraplegie en laat-beginnende cerebellaire ataxie. Het team reconstrueerde vier patiënt‑afgeleide SLC33A1‑varianten in cellen zonder de normale transporter en testte of deze gewijzigde eiwitten de ganglioside‑acetylatie konden herstellen. Alle vier toonden verminderde functie, en de ernstigste vroeg‑optredende mutaties herstelden nauwelijks enige acetylatie. Geleid door recent opgeloste driedimensionale structuren van SLC33A1 kaartten de auteurs deze mutaties op het eiwit en toonden ze aan hoe deze waarschijnlijk de architectuur verstoren of het vermogen om acetyl‑CoA te binden verminderen. Dit wijst sterk op dat aangetaste ganglioside‑acetylatie bijdraagt aan de neurologische symptomen die bij patiënten worden gezien.
Een verborgen tweede actieve plaats in CASD1
Het werk bracht ook een onverwachte wending aan het licht: CASD1 lijkt zelf een dubbeldoelig enzym te zijn. Het bekende luminale deel in het Golgi gebruikt acetyl‑CoA geleverd door SLC33A1. Maar wanneer SLC33A1 werd uitgeschakeld, slaagden cellen er onder sommige omstandigheden nog steeds in één acetylgroep op bepaalde siaalzuren te plaatsen, hoewel ze er niet in slaagden de tweede acetylgroep toe te voegen die nodig is voor complexere patronen. Met behulp van geavanceerde structuurvoorspelling en moleculaire simulaties toonden de auteurs aan dat het membraan‑overstekende deel van CASD1 sterk lijkt op een bekend transmembranair acetyltransferase uit lysosomen. Ze identificeerden sleutelaminozuren in dit gebied die acetyl‑CoA aan de cytosolische zijde binden en de acetylgroep direct door het membraan naar siaalzuur overdragen. Wanneer deze residuen werden gemuteerd, verloor CASD1 deze tweede activiteit zowel in reageerbuisexperimenten als in levende cellen.
Twee routes, één fijn afgestemde suikertaal
Samen ondersteunen de gegevens een model met "twee‑katalytische‑plaatsen." De ene route is afhankelijk van SLC33A1 die acetyl‑CoA naar het Golgi‑lumen brengt, waar het luminale domein van CASD1 een acetylgroep aan siaalzuur toevoegt en zowel eenvoudige als dubbele acetylatiepatronen mogelijk maakt. De andere route zit ingebouwd in de membraanliggende kern van CASD1, die rechtstreeks tapte in cytosolisch acetyl‑CoA en nog steeds een basaal niveau van acetylatie kan uitvoeren, zelfs wanneer SLC33A1 ontbreekt. Voor een leek betekent dit dat één enkel enzym, gevoed door twee verschillende acetylbronnen, subtiele "interpunctietekens" op celoppervlakte‑suikers schrijft. Wanneer de transporter of een van de delen van het enzym defect is, zijn deze tekens verplaatst of afwezig, wat kan helpen bepaalde neuro‑ontwikkelings‑ en neurodegeneratieve ziekten te verklaren en een nieuwe regellaag benadrukt in hoe onze cellen hun uiterlijke identiteit vormen.
Bronvermelding: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Trefwoorden: siaalzuur, Golgi-acetylatie, gangliosiden, SLC33A1, CASD1