Clear Sky Science · nl
Structurele dynamiek van het midnolin-proteasoom tijdens ubiquitine-onafhankelijke afbraak van substraten
Hoe cellen het afval snel verwijderen
In elke cel worden continu eiwitten gemaakt en afgebroken. Veel eiwitten krijgen vooraf kleine moleculen genaamd ubiquitine opgeplakt voordat ze in de belangrijkste recyclemachine van de cel, het proteasoom, belanden. Sommige nucleaire eiwitten moeten echter zo snel worden verwijderd dat er geen tijd is voor zo’n markering. Deze studie laat zien hoe een weinig bekend hulp-eiwit, midnolin, rechtstreeks in het proteasoom aansluit om deze dringende doelwitten te verwijderen, en geeft daarmee aanwijzingen voor hoe cellen genactiviteit strak en snel reguleren.
Een snelweg naar de cellulaire versnipperaar
Het 26S-proteasoom is een tonvormig complex dat eiwitten in kleine stukjes hakt. Traditioneel herkent het targets door ketens van ubiquitine die aan hen vastzitten. Recente studies hebben een alternatieve route blootgelegd: een “snelweg”-pad waarbij midnolin bepaalde nucleaire eiwitten rechtstreeks naar het proteasoom escorteert—vooral producten van immediate early-genen die genen razendsnel aan- en uitzetten—zonder ubiquitinetags. Deze eiwitten, zoals transcriptiefactoren die betrokken zijn bij stressreacties en ontsteking, moeten binnen enkele minuten verschijnen en verdwijnen. Het nieuwe artikel combineert cryo-elektronenmicroscopie met biochemische experimenten om, bijna frame voor frame, in kaart te brengen hoe midnolin zich aan het proteasoom hecht en zijn lading voor vernietiging positioneert.
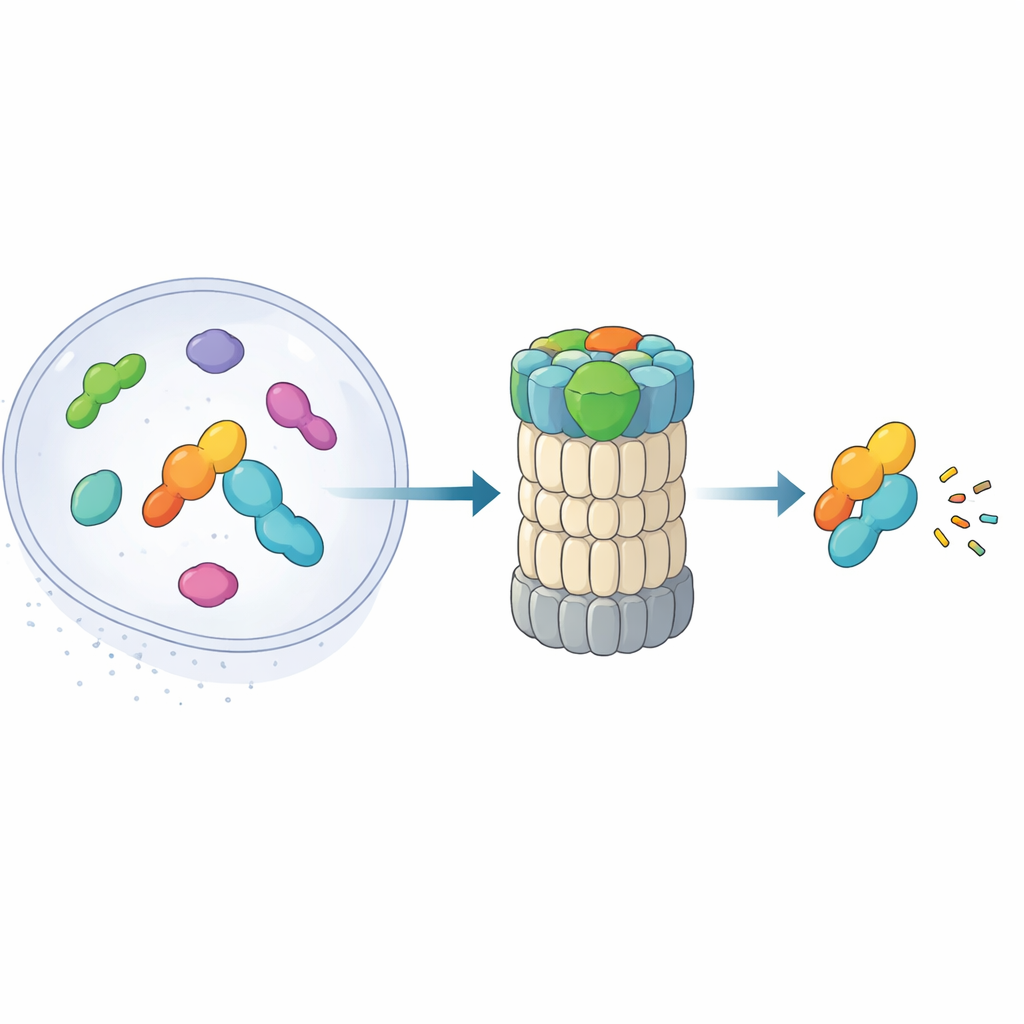
De drieledige helper die targets grijpt en richt
Midnolin werkt als een multigereedschap met drie belangrijke modules. Het ene uiteinde, een C-terminale helix, sluit aan op een dockingsite op een proteasoomcomponent genaamd RPN1 en verankert midnolin aan de recyclemachine. Een centraal “Catch”-gebied herkent en klemt een specifieke strengachtige eigenschap (een degron) in zijn doelwitten vast. Aan het andere uiteinde bevindt zich een ubiquitine-achtig domein. Verrassend genoeg dient dit domein hier niet voornamelijk om aan het proteasoom te binden, zoals vergelijkbare domeinen in andere shuttleeiwitten doen. De auteurs tonen in plaats daarvan aan dat het tegen RPN11 ligt, een enzym dat normaal ubiquitine van substraten afknipt. Hier fungeert RPN11 meer als een scaffold: door het ubiquitine-achtige segment van midnolin te omarmen, helpt het het Catch-domein en zijn gebonden lading direct boven de smalle toegangspore naar het proteasoom te positioneren.
Het eiwit richting de maalcore leiden
Zodra midnolin is gedockt, neemt de energievragende motor van het proteasoom—een AAA+ ATPase-ring—het over. Deze ring zit net onder de toegangspore en trekt ongeplooide eiwitketens stap voor stap in de kern. De cryo-EM-snapshots tonen een reeks "spiraaltrap"-posities die de zes subunits van de motor aannemen terwijl ze het substraat klemmen en door het centrale kanaal doorgeven. De auteurs vingen vier opeenvolgende stadia van deze cyclus, allemaal met midnolin-gebonden materiaal door de pore geregen, en zagen zelfs hoe het loslaten van een magnesiumion in één subunit samenvalt met een neerwaartse verschuiving van de hele ring. Dit suggereert dat gecoördineerd gebruik van ATP en vrijgave van magnesium helpen het eiwit dieper in de kamer te ratcheten waar de knippunten liggen.
Waarom positionering en co-expressie ertoe doen
Het team testte hoe elk midnolin-module bijdraagt aan de efficiëntie. De verankeringshelix alleen kan wel aan RPN1 binden maar verhoogt de proteasoomactiviteit niet significant. Het verwijderen van het Catch-domein laat veel proteasomen in een inactieve, substraatvrije staat hangen, zelfs als midnolin nog kan aanhechten; het vervangen van Catch door een permanent gefuseerd substraat herstelt ook de volledige activiteit niet. Deze bevindingen geven aan dat Catch meer doet dan alleen het target grijpen—het moet het eiwit ook precies op de pore-entrance oriënteren. Biochemische data en transcriptoomgegevens uit tumoren tonen verder dat midnolin de neiging heeft samen met zijn substraten te worden geproduceerd. Bij co-expressie vouwt midnolin beter en vormen zich stabiele complexen, waardoor een kant-en-klare "degradeer mij"-pakket ontstaat dat snel naar het proteasoom kan worden gebracht wanneer de cel genexpressie moet resetten.
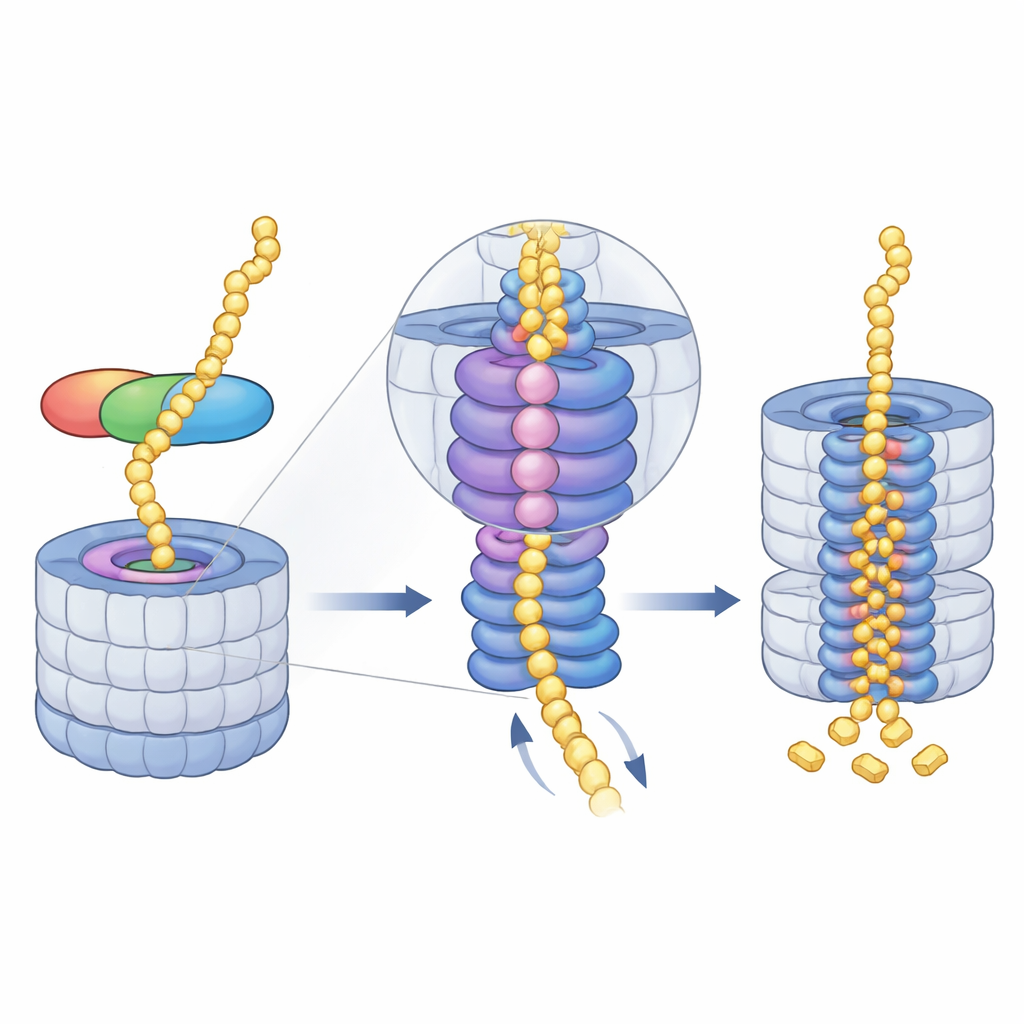
Zelfopruiming en toekomstige medische mogelijkheden
Nadat het doelwit naar binnen is getrokken en versneden, blijft midnolin zelf niet ongemoeid. Zijn eigen ongestructureerde regio’s kunnen in de motor worden geregen en in dezelfde vernietigingskamer gevoerd, wat voorkomt dat de helper onnodig ophoopt. Door deze ubiquitinevrije route naar het proteasoom te belichten, breidt de studie ons begrip uit van hoe cellen eiwitlevensduur op zeer korte tijdschaal beheren. Het wijst ook op nieuwe therapeutische strategieën: door midnolin-gebaseerde moleculen te ontwerpen die ziekteveroorzakende nucleaire eiwitten rechtstreeks aan het proteasoom koppelen, kunnen onderzoekers mogelijk ooit “on-drugbare” targets, waaronder bepaalde kankerdrijvers, sneller en selectiever elimineren.
Bronvermelding: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Trefwoorden: proteasoom, midnolin, eiwitafbraak, ubiquitine-onafhankelijke route, immediate early-genen