Clear Sky Science · nl
Ruimtelijke heterogeniteit van MDSC's gemedieerd door ANXA1-FPRs-signaalering veroorzaakt immuunsuppressie bij de progressie van OSCC
Waarom het lichaam moeite heeft met sommige mondkankers
Plaveiselcelcarcinoom van de mond, een veelvoorkomende vorm van mondkanker, is vaak bestand tegen de meest veelbelovende kankerbehandelingen van nu: immunotherapieën die het eigen afweersysteem ontketenen. Deze studie stelt een fundamentele maar cruciale vraag: waarom falen krachtige immuuncellen, die tumoren zouden moeten herkennen en vernietigen, zo vaak tegen deze tumoren? Door in kaart te brengen waar verschillende cellen zich binnen de tumor bevinden en hoe ze met elkaar communiceren, onthullen de onderzoekers een verschuivend „kat‑en‑muisspel” tussen kankercellen, immuunsuppressorcellen en dodelijke T‑cellen dat helpt te verklaren waarom behandelingen mislukken — en dat een manier aanwijst om dat te verhelpen. 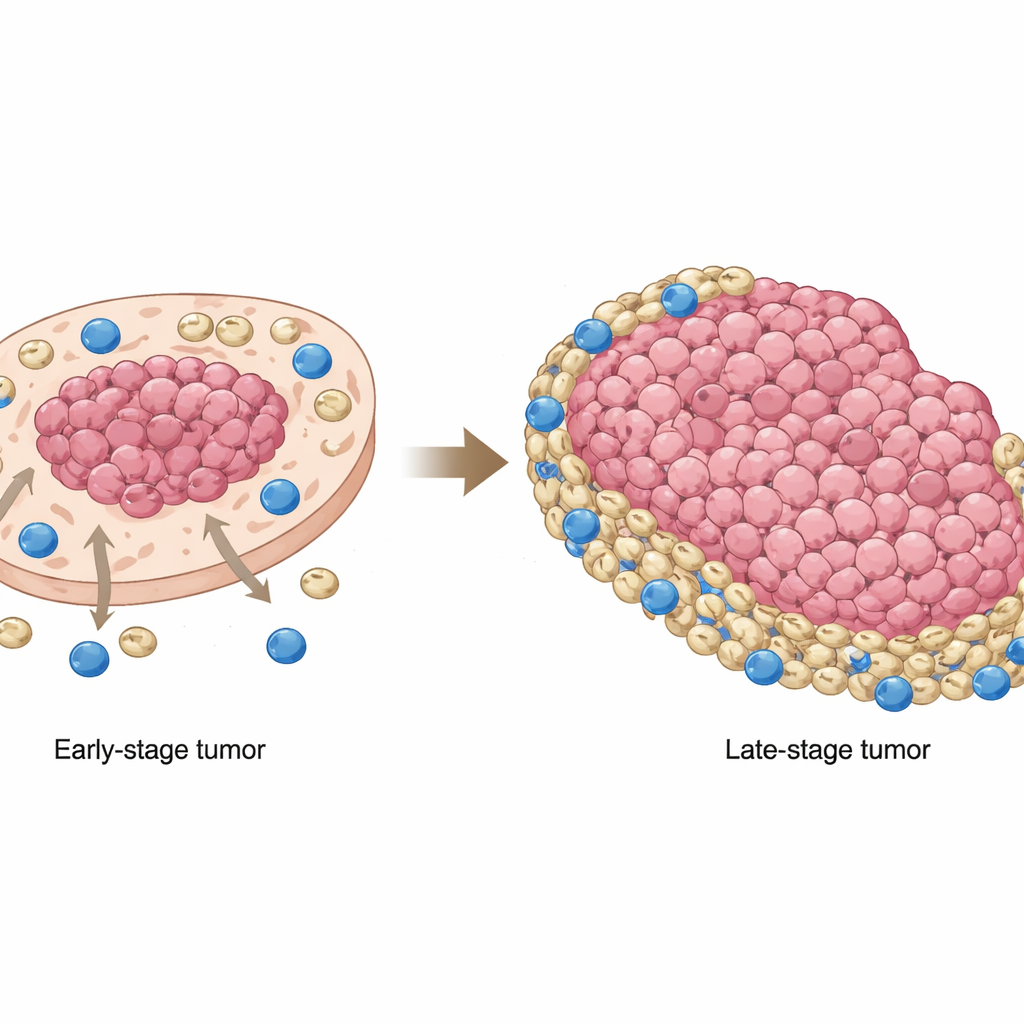
Het verborgen landschap in een tumor
De auteurs combineerden twee geavanceerde methoden: single‑cell RNA‑sequencing, die de activiteit van individuele cellen uitleest, en ruimtelijke transcriptomica, die laat zien waar die cellen zich bevinden in daadwerkelijke tumorweefseldoorsneden. Bij analyse van tumoren van patiënten met vroege en late stadia van mondkanker identificeerden ze de belangrijkste celspelers: kwaadaardige epitheelcellen, CD8‑"killer" T‑cellen, andere T‑ en B‑cellen, fibroblasten die structurele ondersteuning vormen, en gespecialiseerde immuuncellen die myeloïde afgeleide suppressorcellen (MDSC's) worden genoemd. Terwijl vroege tumoren meer actieve CD8‑T‑cellen bevatten, vertoonden tumoren in een laat stadium zwakkere T‑cel‑signaleringspatronen en sterkere immuundempende signalen van myeloïde cellen, wat wijst op een steeds vijandigere omgeving voor antikankerimmuniteit.
Suppressorcellen in beweging
Een van de meest opvallende bevindingen was hoe de positie van MDSC's veranderde naarmate tumoren vorderden. In vroeg‑stadiumkankers neigden deze suppressorcellen te clusteren binnen tumorcelrijke gebieden, dicht bij de kankerkern. In latere stadia verschoof hun locatie naar buiten, met accumulatie in tumorarme gebieden en aan de randen, waar CD8‑T‑cellen vaker voorkwamen. Dit betekende dat in gevorderde tumoren de killer‑T‑cellen grotendeels naar de randen werden verdrongen en daar werden geconfronteerd met een gordel van MDSC's, die hun vermogen om kankercellen aan te vallen dempte. Patiëntmonsters en muismodellen bevestigden dat deze herverdeling geen curiositeit was: wanneer MDSC's minder overlapten met kankercellen en in plaats daarvan in niet‑tumorregio's waren gehuisvest, hadden patiënten een slechtere algehele overleving. 
Een schakelaar in signalering tussen kanker- en suppressorcellen
De studie zoomde in op een moleculair „gesprek” tussen kankercellen en MDSC's dat een eiwit omvatte genaamd annexine A1 (ANXA1) op tumorcellen en een familie receptoren genaamd FPR's op myeloïde cellen. In vroege ziektefasen schakelde ANXA1 op kankercellen sterk in op FPR1 en FPR3, vooral op MDSC's en tumorgeassocieerde macrofagen, wat hielp deze suppressorcellen naar de tumorkern te rekruteren en daar te handhaven. Naarmate de kanker voortschreed, daalden de ANXA1‑niveaus op tumorcellen, waardoor deze oorspronkelijke verbindingen verzwakten. Tegelijkertijd begonnen meer MDSC's een andere receptor, FPR2, te gaan uitdrukken, en ontstond ANXA1–FPR2‑signalering als een compenserende route om MDSC's betrokken te houden. Een specifieke subset van tumorcellen met hoge ANXA1‑uitdrukking, die ook stam‑achtige kenmerken vertoonde, leek als „lokmiddel” te fungeren en vroegtijdig MDSC's aan te trekken; toen ANXA1 daalde, raakten MDSC's niet langer verankerd in de kern en verschoof hun aanwezigheid naar regio's rijk aan CD8‑T‑cellen.
Het schild uitschakelen om immunotherapie te helpen
Om te testen of het doorbreken van deze communicatie de behandeling kon verbeteren, gebruikten de onderzoekers een muismodel van mondkanker en blokkeerden FPR2 met een kleinmolecuulremmer genaamd WRW4. Alleen werkte FPR2‑inhibitie de aanwezigheid van MDSC's in de tumoromgeving terug en verhoogde de CD8‑T‑cellen, maar vertraagde de tumorgroei niet voldoende. Evenzo leverde behandeling met een anti–PD‑1 immuun‑checkpointantilichaam op zichzelf slechts bescheiden voordelen op, omdat MDSC's nog steeds een suppressieve barrière vormden. Toen beide middelen echter werden gecombineerd, werd de tumorgroei sterk geremd en leefden de muizen langer. Bij deze dieren daalde de infiltratie van MDSC's scherp, terwijl CD8‑T‑cellen dieper doordrongen in tumorcelrijke gebieden, wat suggereert dat blokkering van FPR2 een belangrijk schild weghaalt dat normaal gesproken kankercellen beschermt tegen immuunaanvallen.
Wat dit betekent voor toekomstige kankerzorg
Samengevat laat het werk zien dat niet alleen de soorten cellen, maar ook hun ruimtelijke ordening en signaalpartners bepalen of immunotherapie kan slagen bij mondkanker. Naarmate tumoren vorderen, migreren MDSC's van het centrum naar de randen, waar ze killer‑T‑cellen onderscheppen, en ANXA1–FPR2‑signalering helpt deze suppressieve ordening in stand te houden. Door deze route te verstoren — vooral in combinatie met bestaande checkpointmiddelen — zouden artsen in staat kunnen zijn de tumoromgeving te herbedraden zodat het eigen immuunsysteem kankercellen weer kan herkennen en vernietigen. Dit suggereert een concreet strategie: het combineren van FPR2‑blokkers met immunotherapie zou de uitkomsten kunnen verbeteren voor patiënten van wie de mondkanker momenteel weerstand biedt tegen de beste beschikbare behandelingen.
Bronvermelding: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
Trefwoorden: plaveiselcelcarcinoom van de mond, tumormicro‑omgeving, myeloïde afgeleide suppressorcellen, ruimtelijke transcriptomica, kankerimmunotherapie