Clear Sky Science · nl
FGFR-signaalvorming legt ruimtelijke gradiënten van secretorische celidentiteiten vast langs de proximale-distale as van de luchtwegen
Hoe onze luchtwegen stilletjes de lucht die we inademen sorteren en verdedigen
Elke ademhaling laat lucht langs miljoenen cellen stromen die onze luchtpijp en longen bekleden. Deze cellen doen veel meer dan een passief oppervlak bieden: ze ontgiften verontreinigingen, bestrijden ziekteverwekkers en helpen te voorkomen dat kleine luchtzakjes inklappen. Deze studie laat zien dat secretorische cellen in de muizenluchtweg niet allemaal hetzelfde zijn. In plaats daarvan zijn ze georganiseerd in vloeiende gradiënten van richting keel (proximaal) naar diep in de long (distaal), en een belangrijk signaalpad, FGFR2b genoemd, helpt deze geleidelijke verschuivingen in celidentiteit en functie op te zetten en te behouden. Inzicht in deze verborgen ordening geeft aanwijzingen voor hoe longen gezond blijven en wat er mis kan gaan bij chronische longaandoeningen.
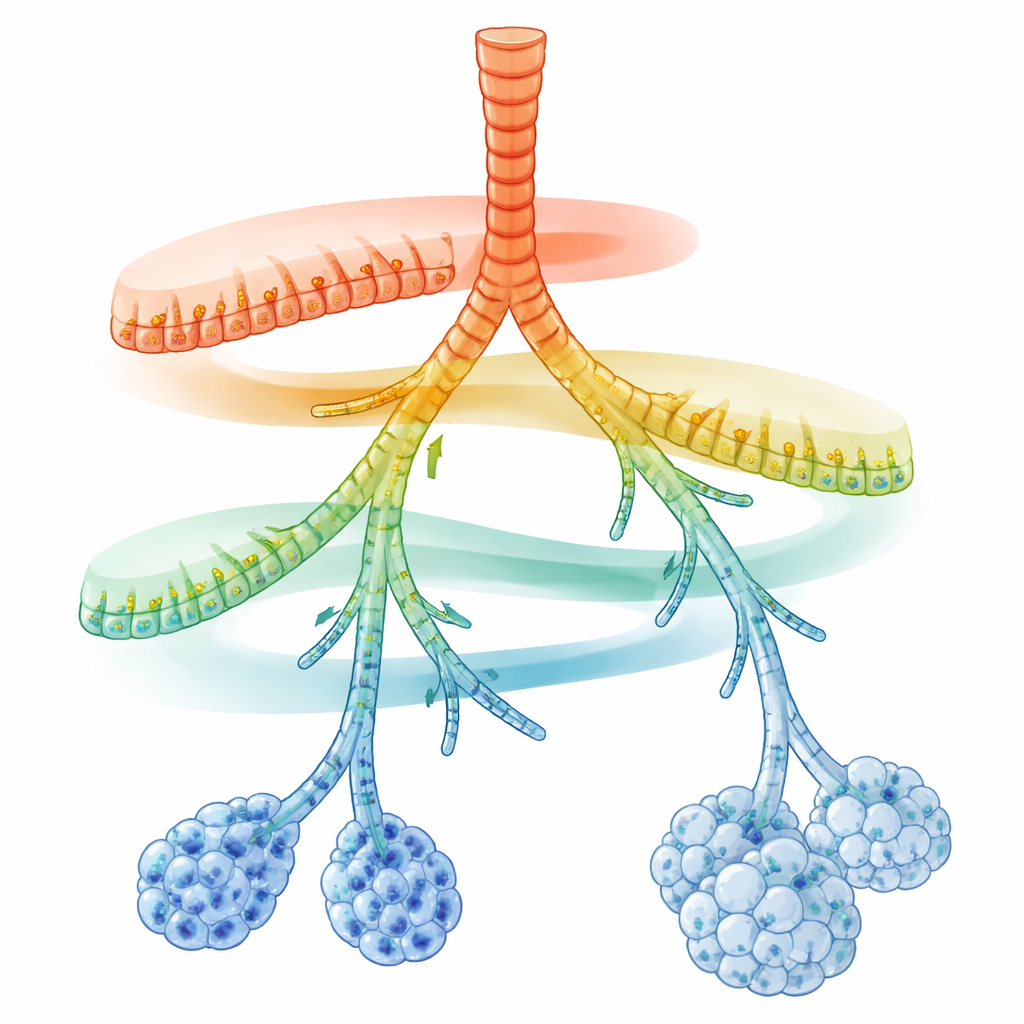
Een verborgen kaart langs de ademhalingsbuizen
De onderzoekers richtten zich op secretorische cellen, die de luchtwegbuizen bekleden en mucus, antimicrobiële peptiden en surfactant uitscheiden. Met single-cell RNA-sequencing bepaalden ze de actieve genen in duizenden individuele cellen uit volwassen muizenlongen. Wanneer ze deze cellen projecteerden in een kaart van moleculaire gelijkenis, vielen secretorische cellen niet in een paar starre types. In plaats daarvan vormden ze een continue keten van toestanden die grote luchtwegen verbindt met kleine luchtzakjes. Bovenop een gedeeld kernprogramma voor ontgifting van ingeademde chemicaliën verschenen twee tegengestelde gradiënten van genactiviteit: nabij de grotere luchtwegen waren genen voor snelle, aangeboren immuunverdediging het hoogst; richting de verste vertakkingen en alveoli domineerden genen voor lipideverwerking, surfactantproductie en antigeenpresentatie.
Van één beginpunt naar vele gespecialiseerde celtoestanden
Om te zien hoe dit patroon ontstaat, labelden de onderzoekers secretorische voorlopercellen in de late foetale periode en volgden hun nakomelingen in de vroege levensfase met lineage tracing en single-cell analyse. Deze gelabelde cellen vormden aanvankelijk een onrijk pool met sterke eiwitproductiemachinerie en genen die gekoppeld zijn aan weefselopbouw. Na de geboorte, toen ademhaling en blootstelling aan de buitenwereld begonnen, diversifieerden deze cellen geleidelijk in meerdere rijpe groepen: proximale secretorische cellen rijk aan aangeboren verdedigingsgenen, meer centrale cellen met ontwikkelings- en regulatorische signaturen, dubbel-positieve cellen die luchtweg- en alveolaire identiteiten overbruggen, en alveolaire type 2-cellen gespecialiseerd in surfactant. Het ontgiftingsprogramma schakelde vroeg en breed aan, terwijl aangeboren immuun- en antigeenpresentatieprogramma’s later en in specifieke regio’s aan gingen, wat aangeeft dat secretorische celfuncties in een bepaalde volgorde in de tijd worden verworven.
Hoe een groeisignaal de distale luchtwegidentiteit vormgeeft
Een belangrijk aanknopingspunt voor wat deze gradiënten aandrijft was een receptor genaamd FGFR2b, onderdeel van een groeifactor-signaalpad dat al bekend is als essentieel voor alveolaire type 2-cellen. FGFR2b en zijn doelgenen waren actiever in distale luchtweg- en alveolaire cellen dan in proximale. Toen de onderzoekers FGFR2b specifiek in secretorische cellen uitschakelden net na de geboorte, stokte het normale distale programma. Genen die nodig zijn voor surfactantproductie en vesikeltransport namen af, terwijl genen die typerend zijn voor platte alveolaire type 1-cellen, mitochondriale componenten, ionkanalen en stress-overlevingsfactoren toenamen. Sommige intermediaire luchtwegcellen gingen nu matige niveaus van zowel proximale aangeboren-verdedigingsmarkers als distale markers tegelijk tot expressie brengen, waardoor het normale ruimtelijke patroon vervaagde. In organoïdculturen gekweekt uit luchtwegcellen onderdrukte toevoeging van FGFR-liganden proximale aangeboren-verdedigingsmarkers en versterkte het surfactant-gerelateerde genen op een wijze die overeenkwam met de in vivo bevindingen, wat bevestigt dat activering van FGFR2b voldoende is om cellen naar een distale secretorische identiteit te duwen.
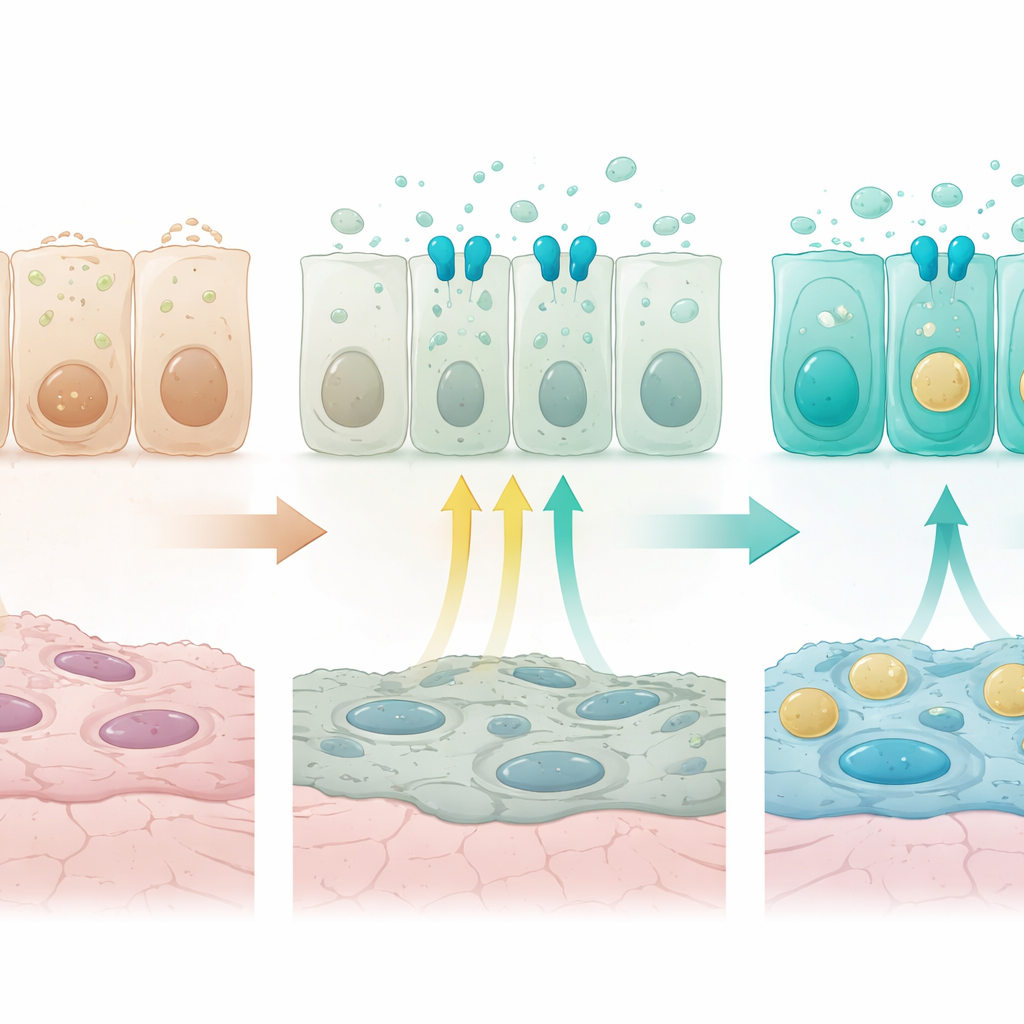
Fijnregeling door interactie met andere signalen
Het team onderzocht ook hoe FGFR2b-signaalvorming samenwerkt met een ander pad aangedreven door VEGFA, voornamelijk bekend van de vorming van bloedvaten. In organoïden kon VEGFA alleen sommige aangeboren-verdedigingsgenen dempen, en het blokkeren van zijn receptor veranderde bepaalde distale markers, maar het kon FGFR2b niet volledig vervangen. Sterker nog, verlies van FGFR2b in vivo verlaagde Vegfa-expressie, en gecombineerde stimulatie van beide paden gaf terugkoppeling die FGFR2b-niveaus deed dalen, wat wijst op een complexe kruisregeling tussen deze signaalroutes. Bij volwassen muizen leidde het uitschakelen van FGFR2b niet langer tot dramatische herschikking van aangeboren-immuniteitsgradiënten, maar het bleef nodig om expressie van belangrijke distale markers te behouden, zoals het surfactantgen Sftpb en de klassieke luchtweg-secretoriemarkergene Scgb1a1, en om hybride luchtweg–alveolaire cellen te bewaren.
Waarom deze gradiënten belangrijk zijn voor longgezondheid
Het beeld dat naar voren komt is dat het luchtwegepitheel eerder een fijn afgestemd landschap is dan een lappendeken van geïsoleerde zones. Proximale regio’s zijn afgestemd op snelle, slijmgebaseerde verdediging, terwijl distale regio’s surfactantproductie combineren met meer gespecialiseerde immuuncommunicatie. FGFR2b-signaalvorming helpt deze indeling te vestigen en te behouden, vooral in de distale compartimenten, door lipide- en vesikelgerelateerde programma’s te bevorderen en ongepaste proximale eigenschappen te remmen. Het verstoren van deze gradiënten, door genetica, milieu of ziekte, kan het evenwicht verschuiven tussen verdediging, ontgifting en ondersteuning van gasuitwisseling, wat bijdraagt aan aandoeningen waarbij distale luchtwegen meer proximale kenmerken aannemen. Dit kader biedt een nieuwe manier om na te denken over longaandoeningen die de luchtwegboom "herpatroniseren" en kan toekomstige strategieën sturen om de juiste cellulaire organisatie te herstellen.
Bronvermelding: Sountoulidis, A., Theelke, J., Liontos, A. et al. FGFR signaling establishes spatial gradients of secretory cell identities along the airway proximal-distal axis. Nat Commun 17, 2651 (2026). https://doi.org/10.1038/s41467-026-70842-0
Trefwoorden: luchtwegepitheel, secretorische cellen, FGFR2b-signaalvorming, longontwikkeling, ruimtelijke gradiënten