Clear Sky Science · nl
Protonkanalen regelen de vesiculaire koolstofzuurchemie in mineralisende cellen van een mariene calcificator
Hoe kleine bouwers onze planeet vormgeven
Een groot deel van ’s werelds kalkstenen kliffen en koraalriffen wordt opgebouwd door microscopische bouwers die opgeloste ingrediënten uit zeewater halen en omzetten in vast gesteente. Deze studie kijkt in één zo’n bouwer — de larvale fase van een zee-egel — om een verwonderlijk basale vraag te beantwoorden: hoe regelen de cellen hun zuurgraad terwijl ze een skelet van calciumcarbonaat opbouwen? Het antwoord onthult een elegant elektrisch trucje dat ook kan verklaren waarom mariene schelpdieren zo kwetsbaar zijn voor een zuurdere oceaan.
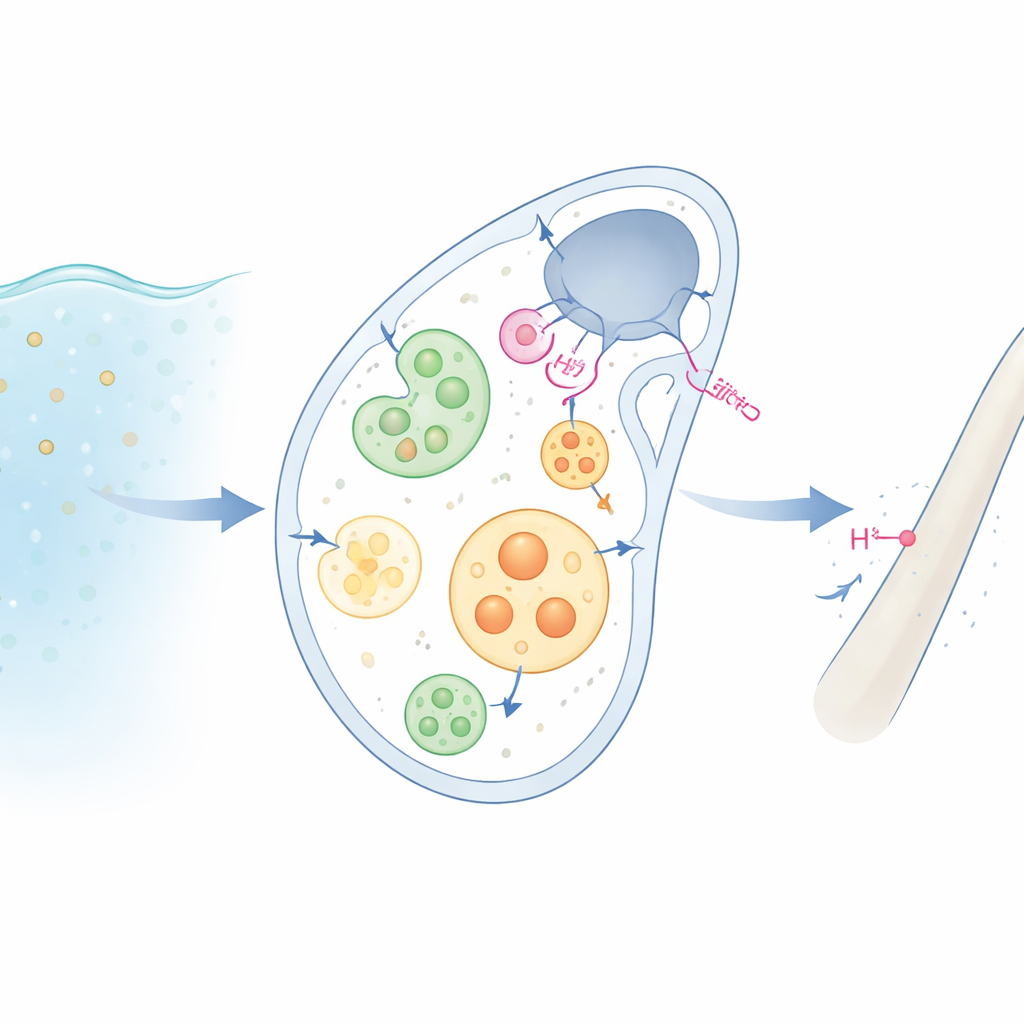
Van zeewater naar skelet
Zee-egellarven verharden hun lichamen met kleine calcietstaafjes van calciumcarbonaat. Daartoe zuigen gespecialiseerde “mineraliserende” cellen eerst zeewater op en verpakken dit in kleine interne druppels, of vesikels. In deze druppels worden de bouwstoffen voor het mineraal — calcium, carbonaat en andere ionen — geconcentreerd tot een amorfe, glasachtige voorloper die later tot kristal verhardt. Maar telkens wanneer calciumcarbonaat vormt, ontstaat extra zuur (protonen). Als dat zuur zich zou ophopen, zou het juist het mineraal oplossen dat de cellen proberen te maken. Hoe de cellen deze zelfvernietiging voorkomen, is lange tijd een raadsel geweest.
Zuurgraad meten in bewegende druppels
De onderzoekers gebruikten live‑imaging en pH‑gevoelige fluorescentiedyes om de chemie in deze vesikels in real time te volgen. Ze vonden dat bijna de helft van de vesikels sterk alkalisch was — basischer dan normaal zeewater — terwijl de rest neutraal of licht zuur was. Toen ze kort de zuurgraad van het omringende zeewater veranderden, verschoof zowel het interne milieu van de cellen als dat van de vesikels, wat aantoont dat protonen relatief vrij over deze membranen kunnen bewegen. Vesikels waren echter deels afgeschermd ten opzichte van het celinterieur: ze reageerden langzamer en minder uitgesproken, wat wijst op een gecontroleerde “lekkage” die helpt gunstige condities voor mineraalvorming te handhaven.
Elektrische lekken die zuur verwijderen
Om te achterhalen wat deze lekkage veroorzaakt, richtte het team zich op een protonkanaaleiwit genaamd Otop2l, eerder gekoppeld aan de skeletgroei van zee-egels. Met behulp van antilichamen zagen ze dat Otop2l niet alleen in het buitenmembraan van de mineraliserende cellen zit, maar ook op de membranen van grote interne vesikels. Toen ze Otop2l‑niveaus verlaagden met een gerichte genetische remmer, werden zowel de cellen als hun vesikels minder responsief voor veranderingen in externe pH, wat aangeeft dat dit kanaal een hoofdroute is voor protonen om te ontsnappen. Elektrische opnames in kikkereieren en menselijke cellen die geprogrammeerd waren om Otop2l te produceren, toonden dat het kanaal opengaat bij alkalische condities en in aanwezigheid van calcium en magnesium — precies de situatie in calcificerende vesikels. In wezen gebruiken de cellen hun natuurlijke spanningsverschil over het membraan, samen met Otop2l, om zuur naar buiten te drijven zonder veel metabole energie te verbruiken.
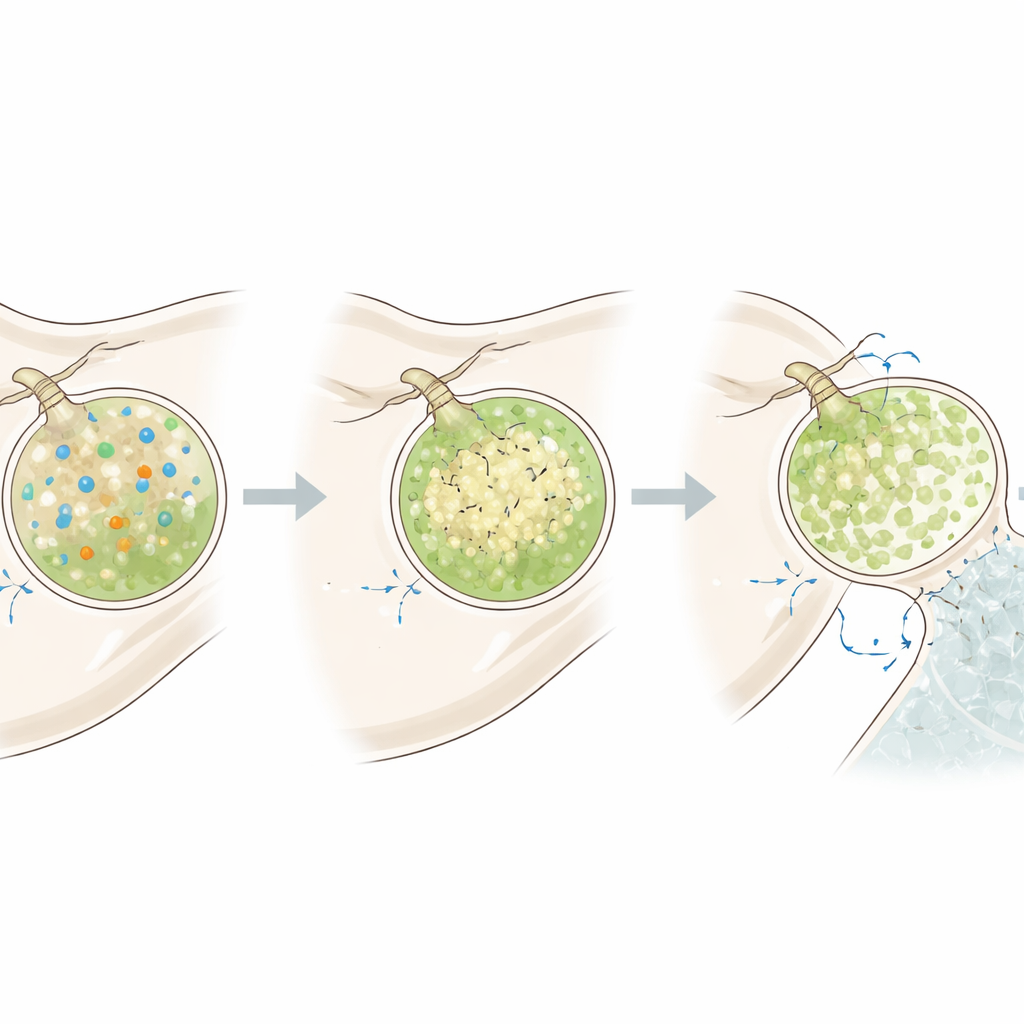
Vesikels die opschalen voor herstel
Het team vroeg vervolgens wat er gebeurt wanneer de larven hun skelet moeten herbouwen na beschadiging. Ze losten de larvale skeletten op door ze kort aan laag‑pH zeewater bloot te stellen, zetten ze daarna terug in normaal water en volgden de vesikels tijdens de hergroei. Tijdens deze fase van hoge vraag produceerden mineraliserende cellen in totaal meer vesikels, met een sterke toename van alkalische, calciumrijke exemplaren. Deze vesikels konden hun hoge pH sneller herstellen na een zuurprikkel, en ook het celinterieur werd alkalischer. Toch bleef het elektrische potentieel van de cellen vergelijkbaar, wat impliceert dat ze zich voornamelijk aanpassen door de aanvoer van carbonaat en de protongeleiding te verhogen, in plaats van hun elektrische toestand grondig te veranderen.
Waarom verzuring van de oceanen ertoe doet
Gezamenlijk ondersteunen de bevindingen een model waarin zee-egelmineraliserende cellen een “open” systeem runnen: ze endocyteren continu zeewater, pompen koolstof in vesikels en vertrouwen op protonkanalen en membraanspanning om overtollig zuur terug in de omringende oceaan te laten wegvloeien. Deze opzet is efficiënt zolang de externe pH binnen het nauwe, stabiele bereik blijft dat een groot deel van de recente aardgeschiedenis heeft gekenmerkt. Maar als het zeewater zuurder wordt — zoals vandaag het geval is door stijgende CO2‑concentraties — kan deze uitgaande stroom van protonen verzwakken of zelfs omkeren. Het werk biedt daarmee mechanistisch inzicht in waarom veel mariene calcifiers moeite hebben onder oceaanverzuring: dezelfde kanalen die biomineralisatie ooit goedkoop en robuust maakten, kunnen in een snel veranderende zee een zwak punt worden.
Bronvermelding: Jonusaite, S., Przibylla-Diop, C., Musinszki, M. et al. Proton channels govern vesicular carbonate chemistry in mineralizing cells of a marine calcifier. Nat Commun 17, 2578 (2026). https://doi.org/10.1038/s41467-026-70837-x
Trefwoorden: biomineralisatie, zee-egellarven, protonkanalen, verzuring van de oceanen, calciumcarbonaat