Clear Sky Science · nl
Een enkele cluster van RNA-polymerase II-moleculen is stabiel geassocieerd met actieve genen
Hoe cellen genen krachtig in korte uitbarstingen inschakelen
Elke cel in je lichaam moet beslissen welke genen ze gebruikt en wanneer, en schakelt die vaak in korte, intense uitbarstingen aan. Decennialang vermoedden wetenschappers dat de enzymen die DNA lezen zich clusteren in kleine “warme plekken” in de kern om dit proces te versterken, maar het werkingsmechanisme van die clusters bleef omstreden. Deze studie kijkt met geavanceerde microscopen in levende vruchtvliegembryo’s en toont dat elk actief gen gepaard gaat met één enkele, stabiele cluster van het enzym dat DNA in RNA omzet, en dat deze clusters zich meer gedragen als drukke werkplaatsen dan als exotische druppels van cellulaire “fase-gescheiden” materie.
Kleine machines die het genoom lezen
Het enzym in het middelpunt van dit verhaal is RNA-polymerase II, een moleculaire machine die langs DNA schuift en genen kopieert naar RNA, de eerste stap naar eiwitsynthese. Eerder onderzoek gaf tegenstrijdige beelden: sommige experimenten suggereerden dat polymerasemoleculen zich groeperen in grote, langdurige “fabrieken” die meerdere genen tegelijk bedienen, terwijl andere alleen vluchtige samenkomsten van enkele moleculen zagen. De auteurs richtten zich op een dramatisch moment in de vroege ontwikkeling van de vruchtvlieg, zogeheten zygotische genoomactivatie, wanneer een stil embryo plotseling duizenden van zijn eigen genen inschakelt. Deze natuurlijke toename van activiteit bood een krachtig testveld om te observeren hoe polymerasemoleculen bewegen, samenkomen en omgaan met genen in real time.
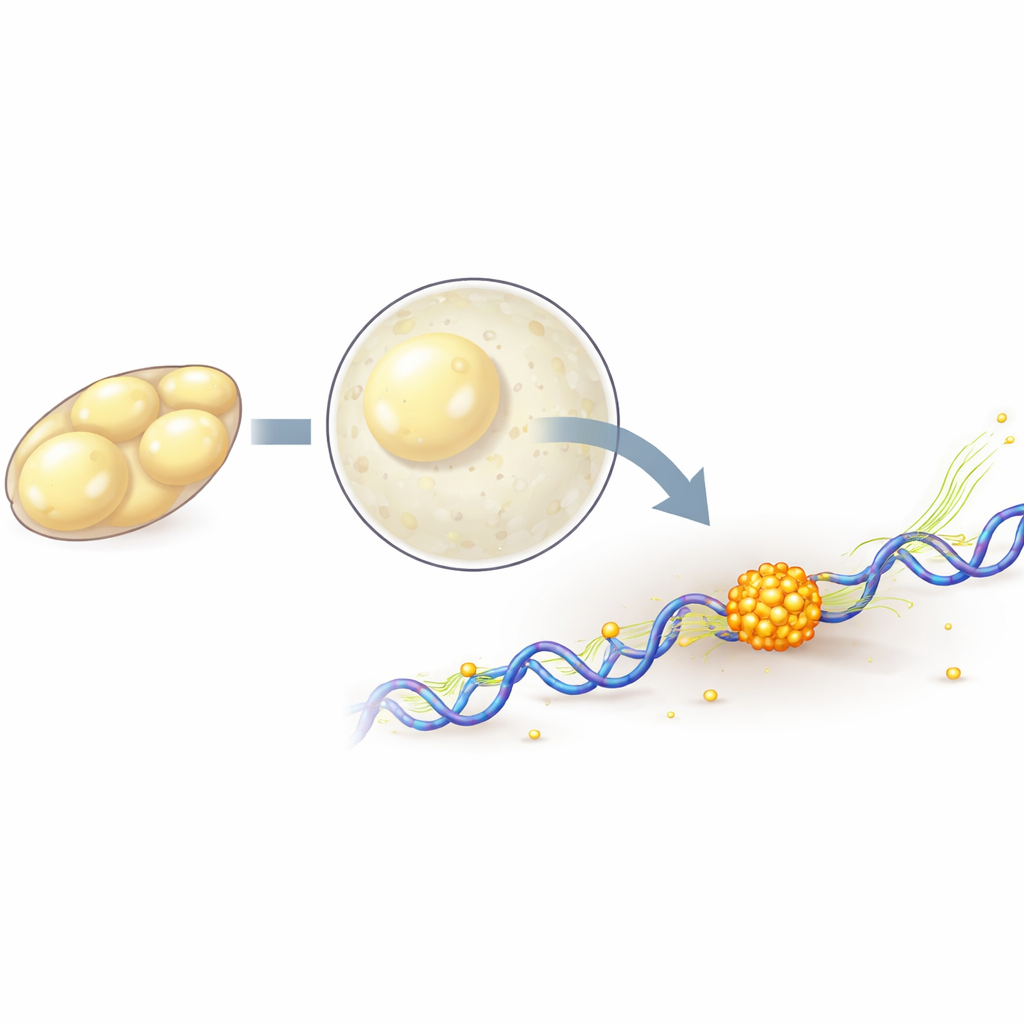
Enkele moleculen volgen in een levend embryo
Om individuele polymerasemoleculen te volgen, tagde het team genetisch een van hun kerncomponenten met fluorescent eiwitten en gebruikte vervolgens lattice light-sheet microscopie en single-molecule tracking om hun beweging in 3D vast te leggen met hoge snelheid en milde belichting. Ze ontdekten dat wanneer het embryo zijn belangrijkste activatiefase ingaat, meer polymerasemoleculen stevig aan DNA gebonden raken, wat overeenkomt met meer ingeschakelde genen. Door kort verschillende stappen in de transcriptiecyclus met geneesmiddelen te blokkeren, konden ze moleculen scheiden die net aan een gen beginnen van degenen die actief langs het gen voortbewegen. Deze analyse toonde aan dat clusterformatie afhangt van de allereerste stappen van het inschakelen van een gen, terwijl actief kopiëren langs het gen de clusters eerder verzwakt en verkort.
Clusters die van aard veranderen tijdens de ontwikkeling
Door hele kernen in de tijd te filmen, zagen de onderzoekers tientallen kleine polymeraseclusters lang voordat de genoombrede activatiegolf begon, waarbij hun aantal en onderlinge afstand veranderde naarmate de kerndelingen vertraagden. Vroeg in de ontwikkeling duren veel clusters bijna even lang als de pauze tussen celdelingen, wat suggereert dat ze worden gedomineerd door polymerasen in een vroege, “gepoiseerde” staat die vaak geen volledige RNA-moleculen produceert. Later, wanneer transcriptie toeneemt, worden clusters dynamischer: hun levensduur volgt niet meer simpelweg de celcyclus en hun interne samenstelling verschuift richting polymerasen die daadwerkelijk verlengen langs genen. Andere metingen van hoe moleculen zich binnen en buiten clusters bewegen geven aan dat polymerasemoleculen nabij actieve genen meer ingesloten zijn en waarschijnlijk vaker terugstoten naar dezelfde locaties, wat het idee ondersteunt van een lokaal druk werkgebied in plaats van een losse, vloeibare druppel.
Één cluster, één gen tijdens een burst
Om clusters rechtstreeks aan genexpressie te koppelen, bekeken de onderzoekers specifieke rapportergenes die oplichten waar nieuw RNA wordt gemaakt, terwijl ze tegelijkertijd polymerase volgden. Voor meerdere verschillende genen zagen ze consequent slechts één polymerasecluster op elke actieve genkopie tijdens een transcriptieburst. De intensiteit van de cluster steeg en daalde synchroon met de hoeveelheid nieuw gevormd RNA, en wanneer gedupliceerde zuster-genkopieën resolvabel waren, droeg elke kopie haar eigen afzonderlijke cluster in plaats van er één te delen. Computersimulaties, afgestemd op de beeldvormingscondities, toonden aan dat genen met sterke polymerasebelading zichtbare clusters vormen, terwijl zwakkere genen mogelijk wel polymerase aantrekken maar te zwak blijven om te detecteren, wat verklaart waarom slechts een minderheid van actieve genen duidelijke clusters in de microscoop toont.
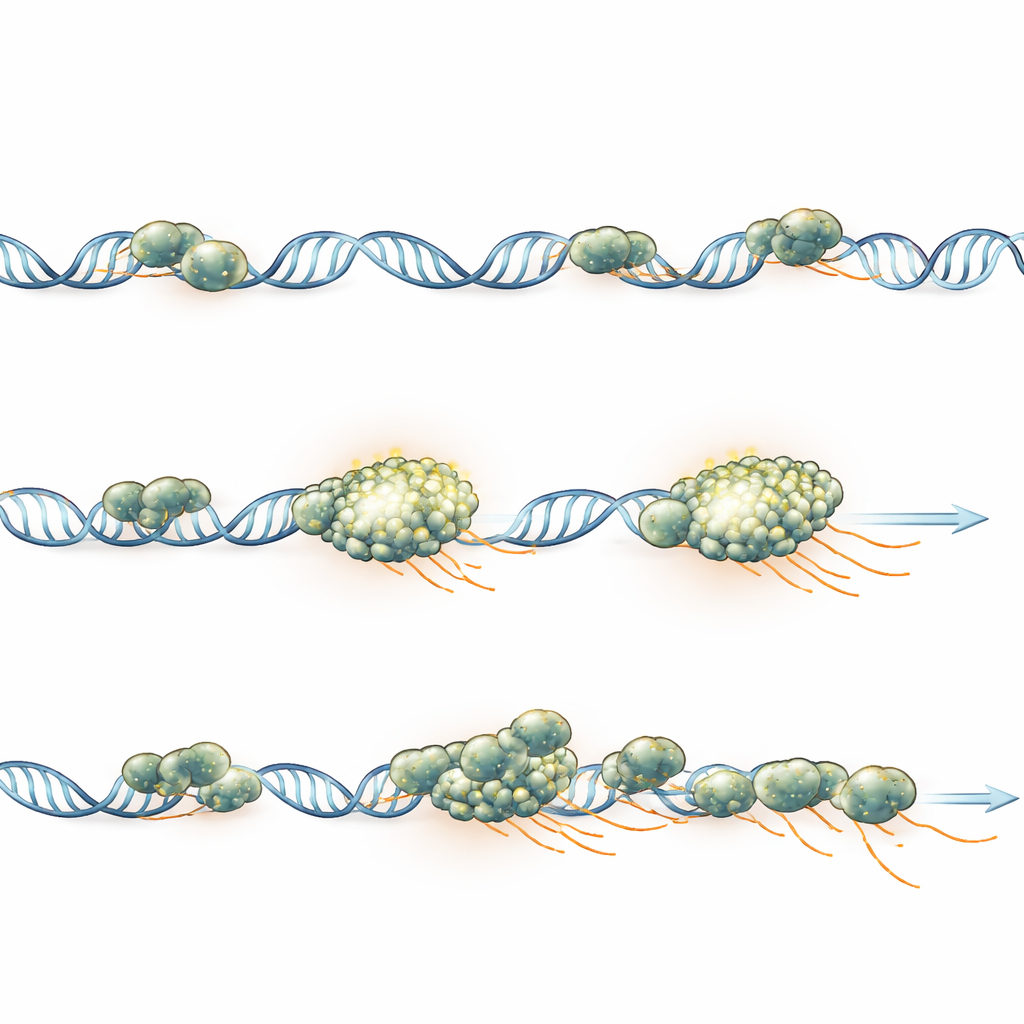
Wat dit betekent voor genregulatie
Dit werk pleit ervoor dat polymeraseclusters in deze embryo’s vooral weerspiegelen hoeveel enzymen actief betrokken zijn bij een enkel gen, en niet een aparte “fabriek”-structuur of een speciale druppel die moet ontstaan om transcriptie mogelijk te maken. Een cluster verschijnt wanneer veel polymerasen in snel tempo worden geladen, blijft stabiel geassocieerd met dat ene gen gedurende een activiteitsburst en verspreidt zich geleidelijk naarmate polymerasen het kopiëren voltooien en vertrekken. Voor de niet-specialist is de kernboodschap dat geninschakeling georganiseerd is via gerichte, gen-voor-gen hubs van activiteit: elk actief gen verzamelt tijdelijk zijn eigen team kopieermachines, en de omvang en levensduur van dat team weerspiegelen direct hoe sterk het gen is ingeschakeld.
Bronvermelding: Mukherjee, A., Kapoor, M., Shankta, K. et al. A single cluster of RNA Polymerase II molecules is stably associated with active genes. Nat Commun 17, 2580 (2026). https://doi.org/10.1038/s41467-026-70775-8
Trefwoorden: clustering van RNA-polymerase II, zygotische genoomactivatie, transcriptie-bursts, genregulatie in embryo’s, single-molecule beeldvorming