Clear Sky Science · nl
Synthetische aptameer-mechanoreceptoren maken celspecifieke krachtsensing en temporele controle via DNA-circuitry mogelijk
Luisteren naar cellen via zachte trekkrachten
Ons lichaam zit vol cellen die voortdurend duwen en trekken aan hun omgeving, waarbij kleine krachten bepalen wanneer ze groeien, bewegen of veranderen. Deze studie beschrijft een nieuwe manier om in die krachten mee te luisteren met DNA-gebaseerde apparaten die kunnen worden afgestemd op specifieke celtypen en over de tijd aan- en uitgezet kunnen worden. Zulke technologie kan in de toekomst ingenieurs helpen weefselgroei te sturen, te begrijpen hoe tumoren zich gedragen, of slimme materialen te ontwerpen die in realtime reageren op levende cellen.
DNA als een tiny mechanische schakelaar
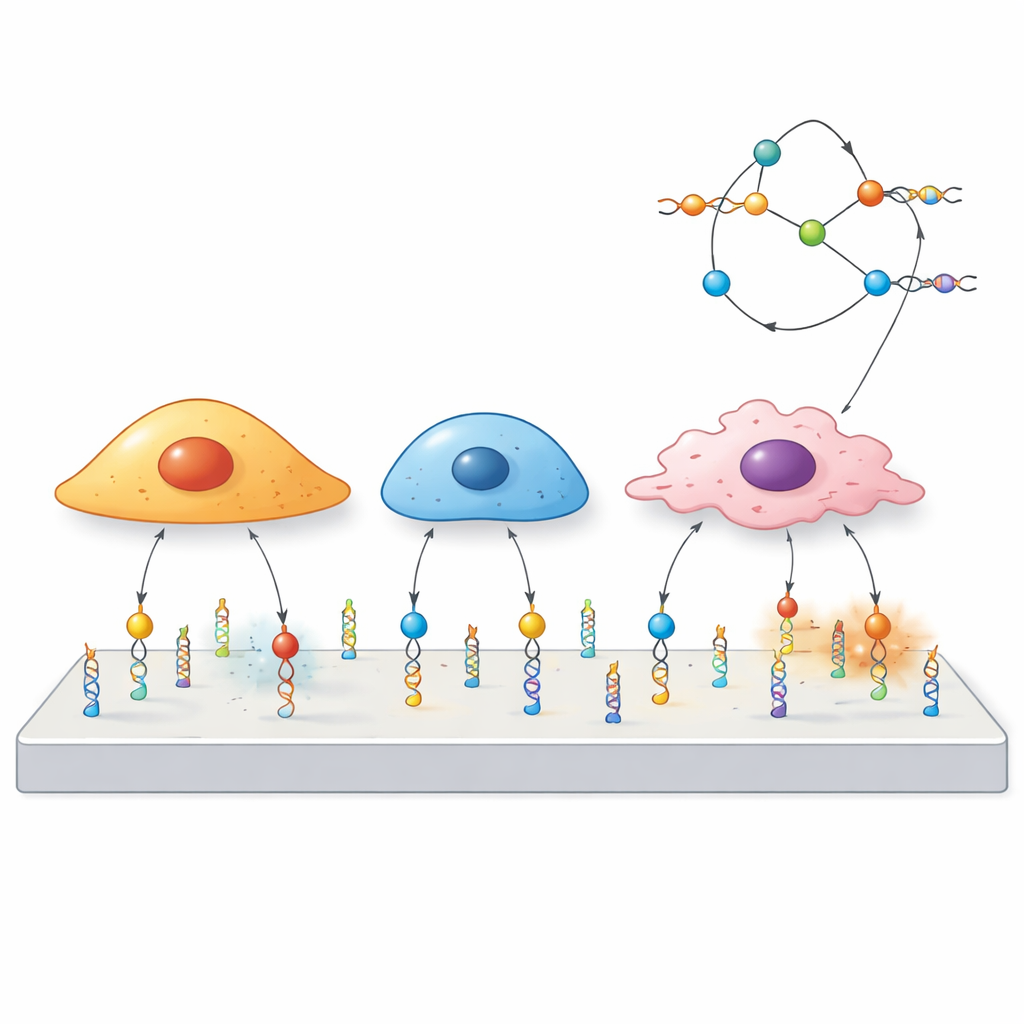
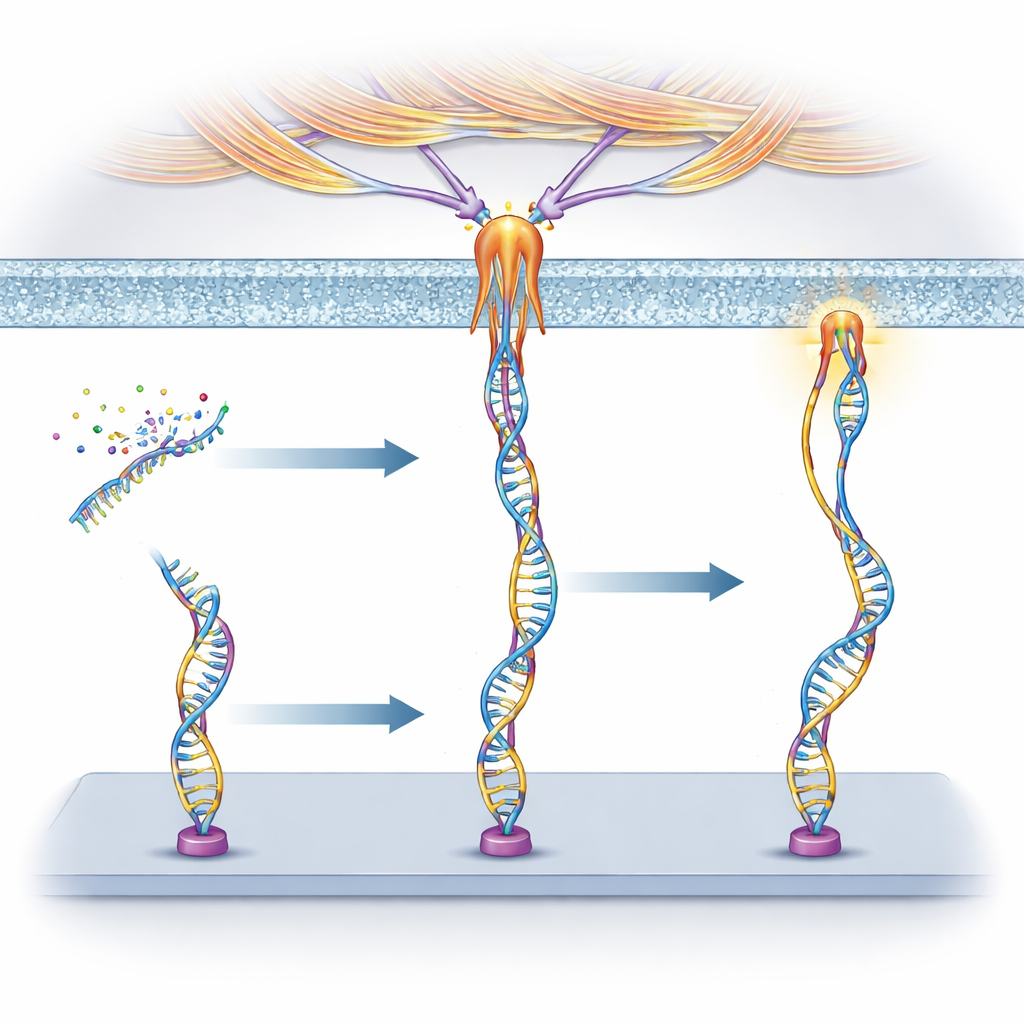
De onderzoekers bouwden “mechanoprobes” uit DNA, hetzelfde molecuul dat genetische informatie draagt. Elke probe heeft drie delen: een korte DNA-sequentie, een aptameer, die zich hecht aan een gekozen eiwit op het celoppervlak; een gekoppeld DNA-segment dat fungeert als een veer die is afgesteld om bij een bepaalde kracht te breken; en een fluorescerende kleurstof die oplicht wanneer die veer loskomt. Wanneer een cel sterk genoeg trekt aan de receptor waaraan het aptameer bindt, opent de DNA-duplex en gaat het signaal aan. Omdat verschillende aptameren zich vasthechten aan verschillende receptoren, kan het team van tevoren bepalen welke cellen of eiwitten de probe kunnen activeren.
Verborgen krachtpaden op celmembranen vinden
De meeste bestaande krachtsensoren richten zich op integrines, bekende eiwitten die cellen helpen zich vast te grijpen aan hun omgeving maar in veel celtypen voorkomen, wat selectiviteit beperkt. Hier richtte het team zich in plaats daarvan op “niet-canonische” receptoren die gewoonlijk niet als mechanisch worden beschouwd. Ze toonden aan dat een aptameer genaamd AS1411, dat bindt aan een eiwit nucleoline dat veel voorkomt op kankercellen, alleen een signaal produceerde wanneer het specifiek zijn doel herkende. Door probes te ontwerpen die bij zwakkere of sterkere krachten opengingen, ontdekten ze dat nucleoline matige krachten doorgeeft vergeleken met integrines en op zichzelf de spreiding van cellen op een oppervlak niet ondersteunt. Daarentegen kon een ander aptameer, Sgc8, dat de receptor PTK7 herkent, krachten rapporteren zelfs wanneer cellen nauwelijks adhesie hadden, en vormde ringachtige patronen die wezen op een andere bron van beweging.
Herleiden waar de krachten vandaan komen
Om te begrijpen wat aan deze DNA-apparaten trok, gebruikten de onderzoekers medicijnen die selectief verschillende celprocessen blokkeren. Voor nucleoline vonden ze dat de krachten sterk afhankelijk waren van myosine, hetzelfde motorische eiwit dat spieren helpt samentrekken, en verschenen op plaatsen waar de cel focale adhesies vormt—speciale contactpunten die gebruikt worden om te grijpen en stijfheid te voelen. Dit suggereert dat nucleoline indirect verbonden is met het interne actine–myosine-systeem van de cel en daarmee contractiele krachten kan delen. Voor PTK7 echter, verminderde het blokkeren van een proces genaamd macropinocytose—waarbij cellen hun membranen oprollen en vloeistof inslikken—het signaal sterk. De krachten ontstonden vooral door vroege membraanruiseling aangedreven door actine-groei, niet door latere stappen in blaasjesvorming, wat een afwijkend mechanisch pad onthult.
Celselectiviteit fijn afstemmen met moleculaire precisie
Aangezien elk aptameer een bepaald oppervlaktereceptor herkent, kan hetzelfde DNA-scaffold eenvoudig worden geherprogrammeerd door het ene aptameer door een ander te vervangen. Het team toonde dit aan met probes voor drie verschillende doelen—PTK7, mucin-1 en EpCAM—over een paneel van kankercellijnen met hoge of lage niveaus van elk eiwit. Cellen rijk aan een bepaalde receptor produceerden sterke signalen, terwijl cellen met weinig receptor nauwelijks reageerden, zelfs wanneer ze door elkaar in hetzelfde schaaltje werden geplaatst. Opmerkelijk was dat cellen die dezelfde receptor deelden toch verschillende ruimtelijke krachtspectra konden tonen, wat benadrukt dat de krachtstroom door een receptor niet alleen afhangt van de aanwezigheid ervan, maar ook van de interne bedrading van elk celtype.
Programmeren wanneer cellen mogen trekken
Gewerkt makend van het feit dat aptameren uit DNA bestaan, koppelden de onderzoekers hun probes aan DNA-reactienetwerken die bepalen of het aptameer zich überhaupt kan binden. Complementaire “blokker”-strengen kunnen het aptameer tijdelijk verbergen, en “activator”-strengen kunnen later de blokkers verwijderen via een strenguitwisselingsreactie, waardoor de krachtsensitiviteit wordt hersteld. Ze ontwierpen ook een RNA-gebaseerde blokker die door een enzym genaamd RNase H kan worden gekapt, en vertraagden deze knip verder met decoy-moleculen die met het enzym concurreren. Op deze manier veranderden ze mechanosensing in een getimed programma: cellen konden alleen signalen genereren na een ingebouwde vertraging of binnen gekozen tijdvensters.
Waarom dit ertoe doet voor toekomstige levende materialen
In gewone bewoordingen verandert dit werk DNA in een slimme mechanische slot dat alleen opengaat voor bepaalde cellen, alleen onder bepaalde krachten en alleen op gekozen tijden. Door aan te tonen dat minder voor de hand liggende receptoren zoals nucleoline en PTK7 mechanische informatie via heel verschillende routes binnen cellen kunnen doorgeven, verbreedt het ons beeld van hoe cellen hun omgeving “voelen”. Omdat het hele systeem is opgebouwd uit nucleinezuren, kan het direct worden geïntegreerd in de snelgroeiende gereedschapskist van DNA-circuits en nanodevices. Dit legt een basis voor materialen en ontworpen weefsels die niet alleen detecteren wanneer cellen duwen of trekken, maar ook reageren met zorgvuldig getimede biochemische acties, mogelijk het sturen van genezing, groei of kankerbehandeling op een zeer programmeerbare manier.
Bronvermelding: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Trefwoorden: mechanotransductie, DNA-aptameren, celmechanica, synthetische biologie, DNA-reactienetwerken