Clear Sky Science · nl
Structurele overgangen bij de stapsgewijze assemblage van proteasoomkerncomplexen
Hoe cellen het moleculaire afval verwijderen
In elke cel moeten versleten en beschadigde eiwitten worden afgebroken voordat ze zich opstapelen als afval. Een reusachtig moleculair apparaat, het proteasoom, voert veel van dit opruimwerk uit en is al een doelwit voor kankertherapieën. Deze studie werpt een blik achter de schermen op hoe het katalytische kerncomplex van het proteasoom in gistcellen stap voor stap wordt opgebouwd, en onthult onverwachte snelkoppelingen en veiligheidscontroles die ervoor zorgen dat het uiteindelijke complex precies werkt en alleen wanneer het er klaar voor is.
Een eiwitversnipperende ton bouwen
Het werkende deel van het proteasoom is een tonvormige kern opgebouwd uit gestapelde ringen van eiwitsubeenheden. In deze ton bevinden zich de verborgen snijplaatsen die andere eiwitten in kleine stukjes hakken. Omdat het gevaarlijk zou zijn deze snijwerktuigen te vroeg te activeren, bouwen cellen de ton op via een reeks gedeeltelijk voltooide tussenstappen. De auteurs concentreerden zich op vroege versies van de kern, bekend als precursorcomplexen, die gewoonlijk zeldzaam en vluchtig zijn. Door één van de laatste assemblagestappen iets te vertragen, konden ze deze vroege vormen uit gist vastleggen en zuiveren en ze beeldvormen met hoge-resolutie kryo-elektronenmicroscopie, die moleculen bevriest in actie en hun driedimensionale vormen onthult.
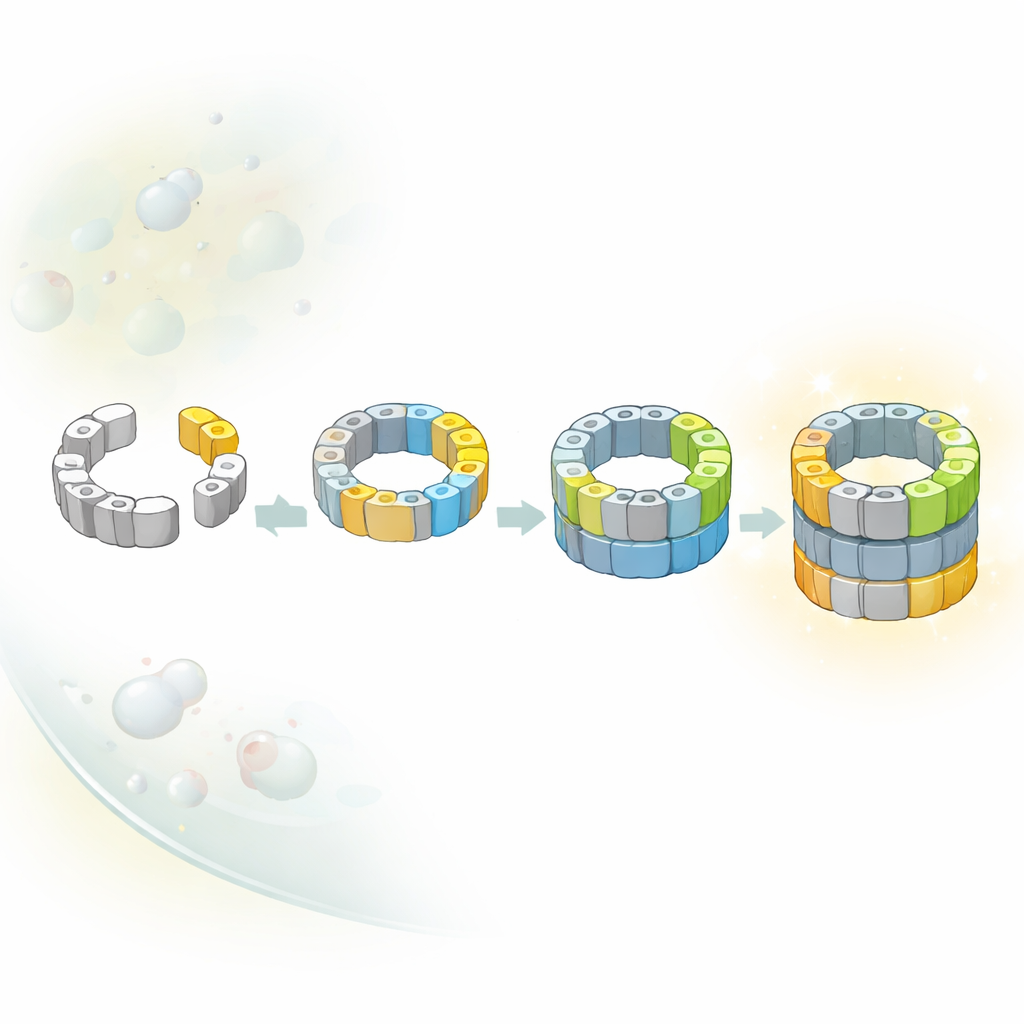
Meerdere wegen naar dezelfde kern
Traditionele leerboekdiagrammen suggereren vaak dat complexe machines in cellen langs één vaste route worden opgebouwd. Hier ontdekten de onderzoekers dat dat niet het geval is voor de proteasoomkern. Zij identificeerden meerdere onderscheidende tussenstappen die verschillen in welke katalytische subeenheden zich bij de halfafgewerkte ton hebben gevoegd. Door structurele momentopnamen te combineren met genetische trucs die individuele subeenheden aan- en uitzetten, toonden ze aan dat minstens twee alternatieve paden leiden van een vroege halfton naar een bijna complete ton. In het ene pad arriveert een specifieke subeenheid, β5, eerst; in het andere kan een andere subeenheid, β1, eerder binnentreden. De verhouding tussen deze routes hangt waarschijnlijk af van welke bouwstenen het meest beschikbaar zijn in de drukke omgeving van de cel.
Van losse onderdelen naar een vergrendelde snijkamer
De structuren tonen ook hoe de snijplaatsen van het proteasoom zorgvuldig worden voorbereid naarmate de assemblage vordert. In vroege tussenstappen zijn sleutel-lusregio’s rond de verborgen snijresiduen soepel en slecht geordend, en zijn de katalytische centra nog geblokkeerd door korte “propeptide”-segmenten. Naarmate extra subeenheden om de ring heen klikken, nemen deze lussen geleidelijk meer gedefinieerde vormen aan die cruciale aminozuren op één lijn brengen die nodig zijn voor zelfactivatie. Pas wanneer twee halftonnen uiteindelijk samenkomen en de dubbele-ring voltooien, vergrendelen deze lussen volledig in hun actieve configuratie en wordt de blokkering verwijderd. Deze koppeling van geometrie en chemie helpt ervoor te zorgen dat krachtige knipactiviteit alleen binnen een afgesloten kamer verschijnt, ter bescherming van de rest van de cel.
Chaperonnes begeleiden en laten vervolgens los
Onderweg begeleiden gespecialiseerde hulp-eiwitten, chaperonnes genoemd, de assemblerende ton en voorkomen verkeerde combinaties. Eén chaperonne, Ump1, begint grotendeels ongestructureerd maar vouwt zich geleidelijk naarmate meer subeenheden zich eromheen scharen; uiteindelijk raakt Ump1 opgesloten in de centrale holte en wordt het afgebroken zodra de ton actief is. Een ander chaperonnepaar, Pba1–Pba2, grijpt het buitenste ringoppervlak op twee slimme manieren vast. Een flexibele lus van Pba1 klemt zich tussen twee buitenringsubeenheden als een afstandhouder, houdt ze iets uit elkaar en voorkomt voortijdig sluiten. Tegelijk helpt de staart van een buitenringsubeenheid (α1) aangrenzende segmenten te positioneren zodat, in de laatste fase, de chaperonnes kunnen worden losgelaten en de ring correct kan sluiten. Toen de onderzoekers de α1-staart verwijderden, stokte de ton in een late, bijna voltooide staat die koppig zijn chaperonnes vasthield, wat bevestigt dat dit kleine gebied deel uitmaakt van een losschakelaar.
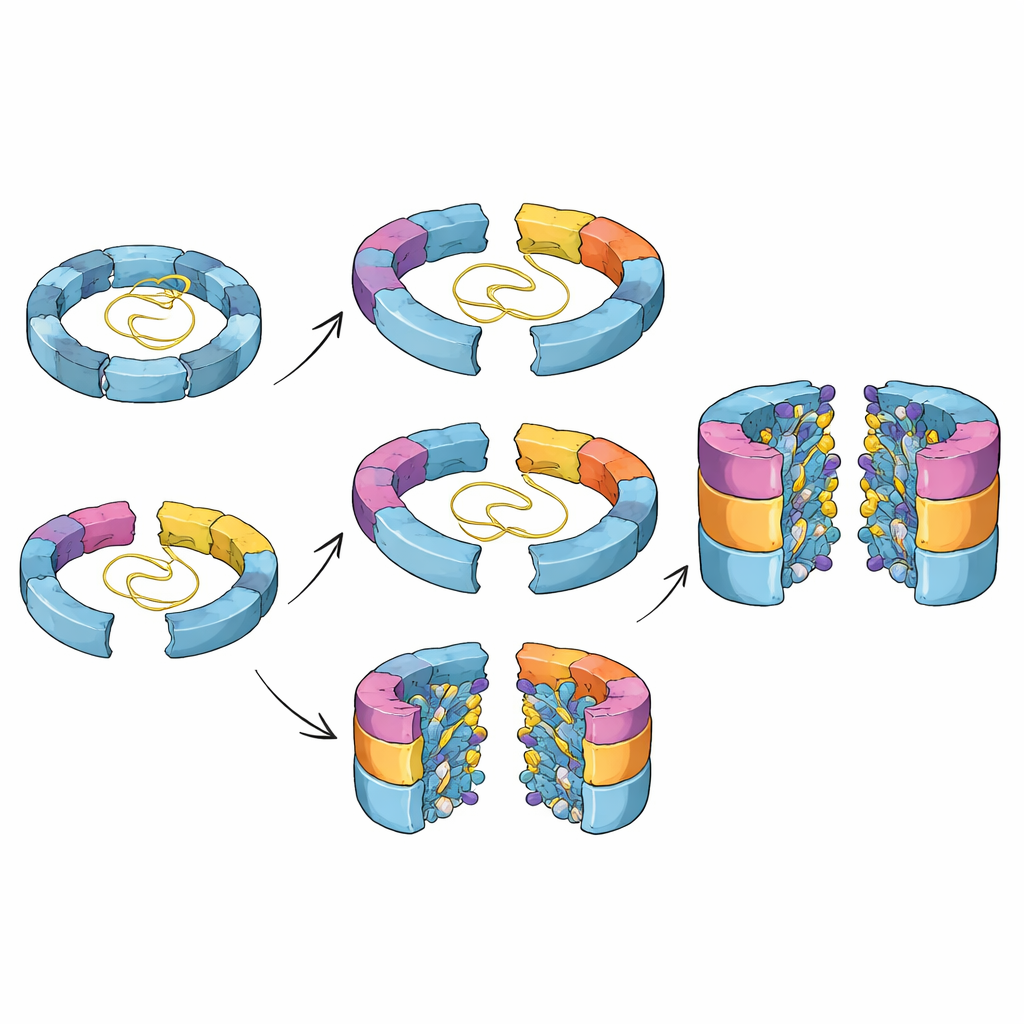
Waarom deze verborgen stappen ertoe doen
Gezamenlijk schetsen deze bevindingen een gedetailleerd beeld van hoe cellen de assemblage van een gevaarlijke maar essentiële eiwitversnipperaar choreograferen. Het werk toont aan dat de proteasoomkern via meer dan één route kan worden opgebouwd, dat zijn actieve plaatsen geleidelijk vorm krijgen, en dat hulp-eiwitten niet alleen vroege tussenstappen stabiliseren maar ook zijn ingebed in een tijdschakelaar die ervoor zorgt dat ze precies op het juiste moment vertrekken. Inzicht in deze verborgen stappen helpt verklaren hoe kleine genetische veranderingen in assemblagefactoren kunnen bijdragen aan ziekte en kan het ontwerp van geneesmiddelen vergemakkelijken die de proteasoomactiviteit fijnregelen bij kanker, immuunstoornissen of neurodegeneratie door de constructie te richten in plaats van alleen het eindvormige complex.
Bronvermelding: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
Trefwoorden: assemblage van het proteasoom, eiwitafbraak, moleculaire chaperonnes, kryo-elektronenmicroscopie, cellulaire kwaliteitscontrole