Clear Sky Science · nl
Labelvrije massawaardering en maatkarakterisatie van biomoleculen van enkele kDa met hiërarchische vision transformer-ondersteunde nanofluidische verstrooiingsmicroscopie
De allerkleinste moleculen zichtbaar maken
Veel van de belangrijkste boodschappers in het lichaam — zoals hormonen en immuunsignalen — zijn zo klein dat ze met krachtige microscopen vrijwel onzichtbaar blijven tenzij ze met fluorescentielabels worden gemarkeerd. Die labels kunnen het gedrag van moleculen veranderen, wat een groot nadeel is voor geneesmiddelenontwikkeling en fundamentele biologie. Deze studie introduceert een manier om individuele moleculen ter grootte van insuline te wegen en te meten zonder labels, door nanofluidische chips te combineren met geavanceerde kunstmatige intelligentie. Het opent een weg om sleutelbiomoleculen in hun natuurlijke staat, één voor één, te observeren.
Minieme kanaaltjes als reageerbuisjes
In het hart van de methode staat nanofluidische verstrooiingsmicroscopie, die gebruikmaakt van een nagelgrote chip met extreem smalle kanalen. Deze kanalen zijn slechts enkele tientallen nanometers breed — duizenden keren dunner dan een mensenhaar. Opgeloste moleculen drijven vrij door deze kanalen in plaats van aan een oppervlak vast te zitten. Wanneer de chip wordt verlicht met zichtbaar licht, verstrooien zowel de kanaalwanden als passerende moleculen licht. Omdat het kanaal veel groter is dan het molecuul, interfereert het verstrooide licht zodanig dat het optische signaal van het molecuul sterk wordt versterkt. Door beelden van een leeg kanaal af te trekken van beelden waarin een molecuul aanwezig is, krijgen de onderzoekers een filmachtige registratie (een kymograaf) van de doorgang, met informatie over zowel de massa als de diffusiesnelheid.
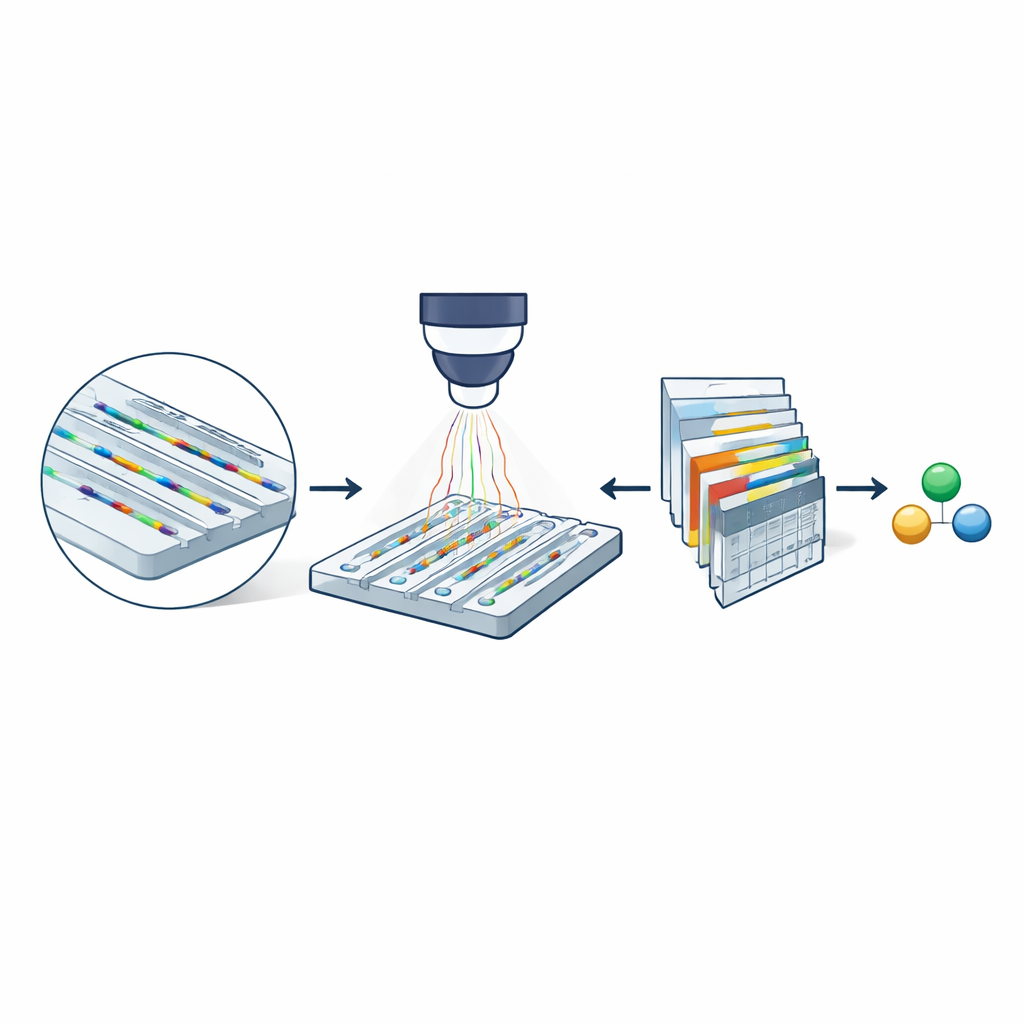
Waarom kleinere kanalen ertoe doen
Zelfs met deze optische versterking konden eerdere versies van de techniek alleen moleculen zwaarder dan ongeveer 60 kilodalton karakteriseren — typische grote eiwitten — omdat signalen van kleinere soorten verloren gingen in ruis. Het team toont aan dat het verkleinen van de dwarsdoorsnede van de nanochannels de gevoeligheid dramatisch verbetert: het optische contrast van een molecuul neemt toe naarmate het kanaaloppervlak kleiner wordt. Experimenten die twee kanaalgroottes vergelijken met het eiwit bovien serumalbumine laten zien dat het pad duidelijk zichtbaar is in het smallere kanaal maar vrijwel verloren gaat in het bredere. Deze eenvoudige geometrische wijziging suggereert dat in principe veel kleinere biomoleculen detecteerbaar zouden zijn als hun zwakke signalen betrouwbaar uit rumoerige beeldreeksen kunnen worden gehaald.
Een AI laten lezen uit rumoerige films
Om dit regime te bereiken ontwikkelden de onderzoekers een gespecialiseerd deep-learningmodel genaamd een hiërarchische vision transformer. In plaats van te proberen elk molecuulspoor pixel voor pixel te reconstrueren, scant het model de kymograaf op meerdere schalen en produceert twee uitkomsten: een waarschijnlijkheidsmap die aangeeft waar een molecuul waarschijnlijk is op elk punt in ruimte en tijd, en een eigenschapsmap die schattingen van moleculaire massa en hydrodynamische grootte codeert. Door eigenschapschattingen te wegen met de waarschijnlijkheidsmap kan het model regio’s negeren die voornamelijk ruis bevatten. De training berust volledig op gesimuleerde trajecten over experimenteel gemeten achtergrondruis, waardoor het systeem leert hoe echte signalen eruit moeten zien, zelfs wanneer ze met het blote oog nauwelijks zichtbaar zijn.
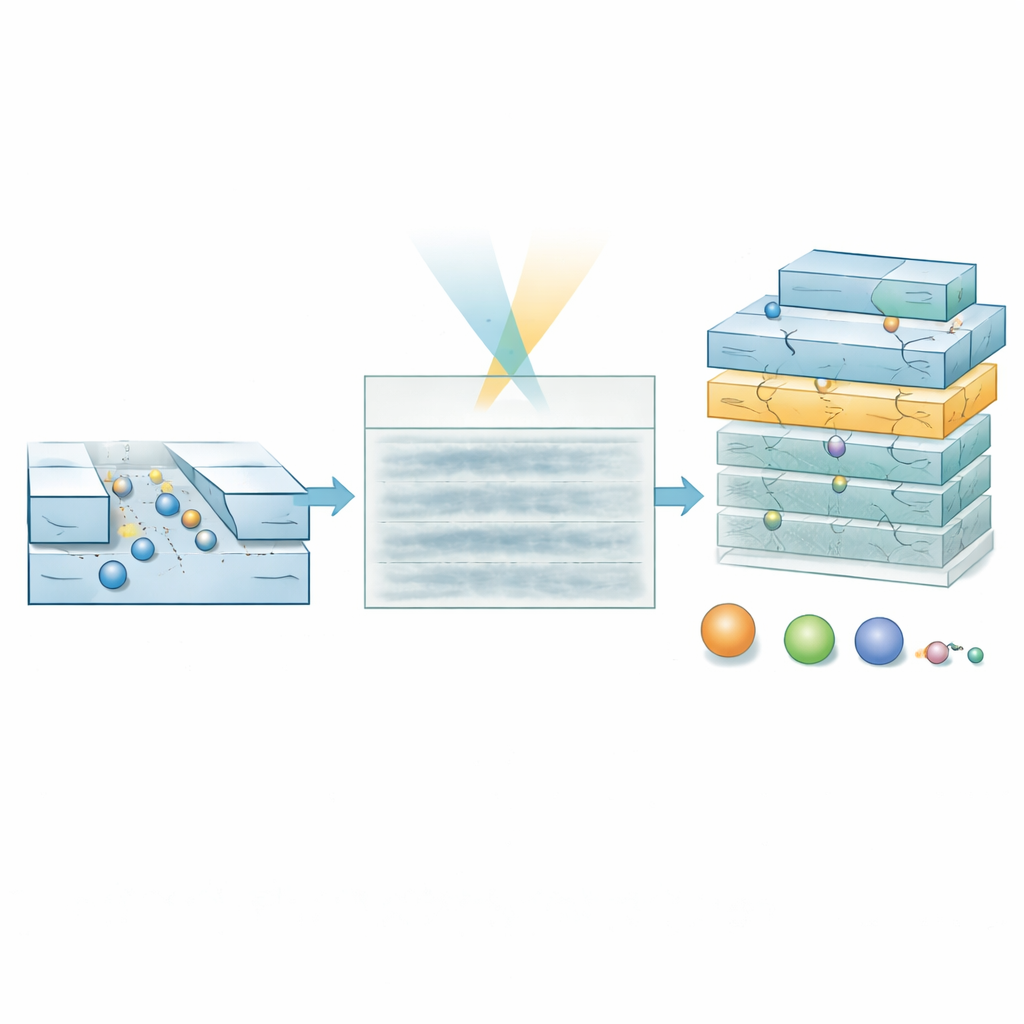
Testen met DNA en hormoonmoleculen
De auteurs valideerden de aanpak eerst met een standaard DNA-„ladder”, een mengsel van dubbelstrengs fragmenten met bekende lengtes en massa’s, in relatief brede kanalen waar alle fragmenten opzettelijk onder de gebruikelijke detectiedrempel lagen. In de ruwe films zijn geen duidelijke DNA-sporen te zien. Toch produceert het AI-model waarschijnlijkheidskaarten die correct aangeven waar moleculen passeren en voorspelt het massa’s die na filtering van onzekere gegevens overeenkomen met de verwachte waarden. De methode rapporteert ook terecht kleinere effectieve groottes voor de stijve, staafachtige DNA-fragmenten dan hun volledige fysieke lengte, wat weerspiegelt hoe vorm diffusie beïnvloedt. De meest veeleisende test gebruikte ultrasmalle kanalen om het peptidehormoon insuline te bestuderen, dat slechts ongeveer 5,8 kilodalton weegt en circa 1,5 nanometer groot is. Ook hier lijken de kymografen vlak, maar het model extraheert een nauwe cluster van massa- en groottewaarden die uitstekend overeenkomen met literatuurwaarden, duidelijk gescheiden van buffer-only controles.
De grenzen oprekken
Om te begrijpen hoe ver deze strategie kan reiken vergeleek het team de precisie van het model met de Cramér–Rao ondergrens, een statistische limiet die de best mogelijke nauwkeurigheid voor elke onpartijdige schatter definieert gegeven de ruis in de data. Met grote sets simulaties tonen ze aan dat zodra het aantal frames dat bijdraagt aan een molecuultraject ongeveer tienduizend overschrijdt, de schattingen van massa en grootte van het model deze theoretische optimums benaderen, zelfs voor een deeltje van zes kilodalton. Experimenten met insuline bij verschillende concentraties reproduceren dezelfde trend: langere effectieve trajecten leveren preciezere metingen op, voornamelijk begrensd door hoe lang kleine, snel diffuserende moleculen in beeld blijven. De auteurs stellen toekomstige strategieën voor — zoals zachtjes het vangen van moleculen in de kanalen of hergebruik van data met bootstrapping — om de bruikbare observatietijd verder te vergroten.
Wat dit betekent voor biologie en geneeskunde
In gewone bewoordingen toont dit werk aan dat het nu mogelijk is om sommige van de kleinste en meest belangrijke moleculen van het lichaam individueel te wegen en te meten, zonder ze aan te raken met fluorescentietags of aan een oppervlak te plakken. Door nanogefabriceerde kanalen te combineren met een speciaal ontwikkelde AI die rumoerige lichtverstrooiingsfilms leest, verlaagt de methode de massa-detectiegrens van deze labelvrije microscopiebenadering met ongeveer een factor tien. Dit opent de deur naar het bestuderen van families van kleine signaaleiwitten en peptidehormonen — zoals cytokines, chemokines en insuline — op enkel-molecuulniveau, en naar het karakteriseren van kleine biologische nanodeeltjes en medicijndragers met ongekende gevoeligheid. Naarmate de technologie rijpt kan het een krachtig hulpmiddel worden in geneesmiddelenontdekking, diagnostiek en fundamenteel onderzoek naar hoe moleculaire interacties het leven op de kleinste schalen vormgeven.
Bronvermelding: K. Moberg, H., Yeroshenko, B., Fritzsche, J. et al. Label-free mass and size characterization of few-kDa biomolecules by hierarchical vision transformer augmented nanofluidic scattering microscopy. Nat Commun 17, 2533 (2026). https://doi.org/10.1038/s41467-026-70514-z
Trefwoorden: labelvrije enkel-molecuulmicroscopie, nanofluidische verstrooiing, vision transformer, kleine biomoleculen, insulinedetectie