Clear Sky Science · nl
Sororin vergrendelt de DNA‑uitgangspoort van cohesine om zusterchromatidecohesie te behouden
Gekopieerde chromosomen veilig bijeenhouden
Elke keer dat een cel deelt, moet ze haar DNA kopiëren en vervolgens één volledige set aan elke dochtercel geven. Als die kopieën te vroeg uit elkaar drijven, kan dat breuken in chromosomen, genetische chaos en ziekte veroorzaken, waaronder kanker. Deze studie onthult hoe een klein eiwitdeel, de staart van Sororin, fungeert als een fysieke vergrendeling op een ringvormige klem die zuster‑DNA‑kopieën bijeenhoudt, en verklaart hoe cellen chromosomen gekoppeld houden tot het exacte moment van scheiding.
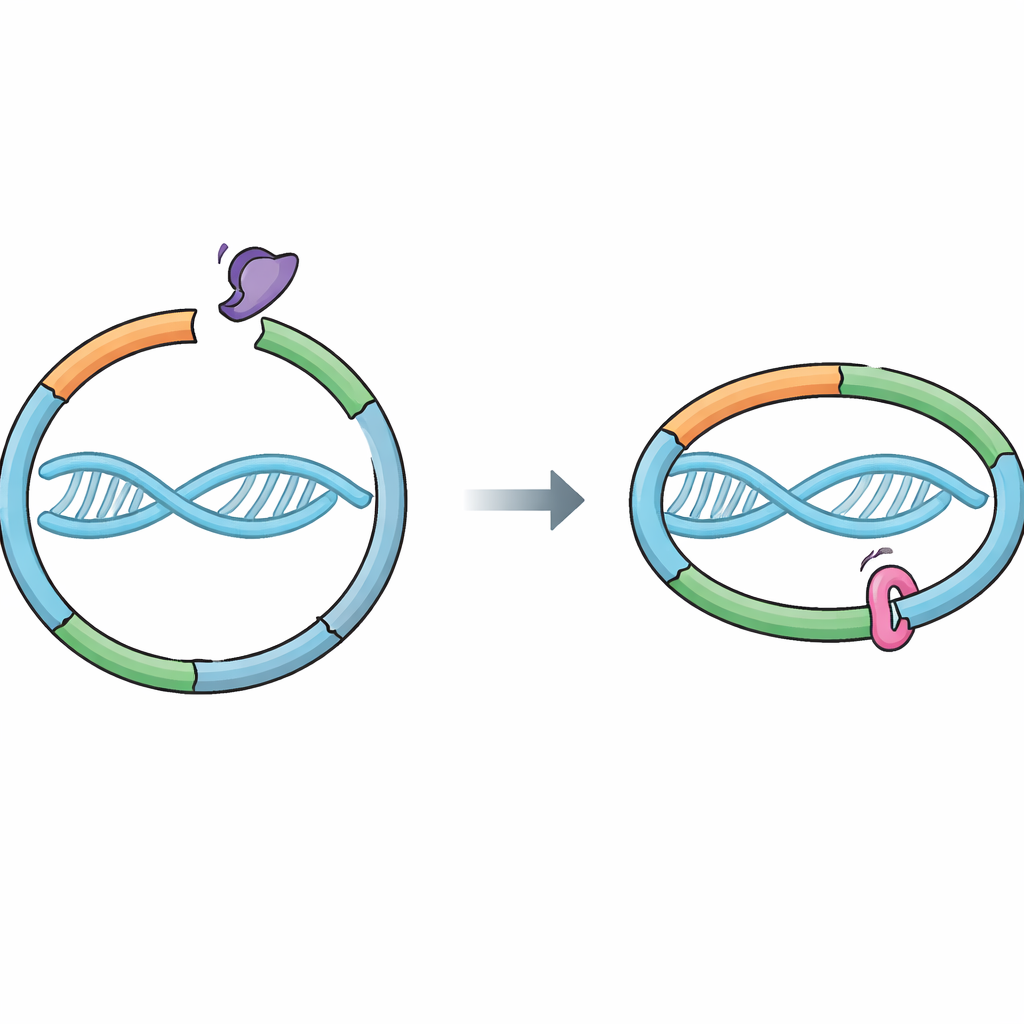
Een moleculaire ring die ons genoom bewaakt
Cellen vertrouwen op een proteïnemachine genaamd cohesine om nieuw gekopieerde chromosomen bij elkaar te houden. Cohesine vormt een ring die om het DNA heen slaat en de twee zusterstrengen verbindt die tijdens DNA‑replicatie zijn ontstaan. Deze verbinding moet sterk genoeg zijn om alle schokken van celdeling te doorstaan, maar ook losgelaten kunnen worden op het juiste moment zodat de zusters schoon van elkaar kunnen scheiden. Een helper‑eiwit, Wapl, bevordert het openen van een specifieke “uitgangspoort” in de ring waar twee cohesineonderdelen, RAD21 en SMC3, samenkomen. Het openen van deze poort maakt het mogelijk dat DNA naar buiten glipt en cohesine loslaat. Tot nu toe werd gedacht dat Sororin cohesie vooral behoudt door de partner van Wapl, Pds5, te blokkeren, maar het was onduidelijk of Sororin ook direct de cohesine‑ring aanraakt.
Een piepkleine staart met grote houdkracht
De auteurs richtten zich op het uiterste staartuiteinde van Sororin—de laatste ~30 aminozuren, het zogeheten C‑terminale gebied (CTR). Door Sororin in stukken te knippen en die in menselijke cellen te testen, vonden ze dat deze kleine CTR zowel noodzakelijk als voldoende is om zusterchromosomen gekoppeld te houden. Wanneer de CTR kunstmatig aan centromeren werd verankerd, de centrale plekken waar zusters het langst verbonden blijven, bracht dat de cohesie bijna volledig terug in cellen zonder volledige Sororin. Omgekeerd, wanneer de CTR langs het gehele chromatine werd vastgezet, kon cohesine niet efficiënt worden verwijderd en konden chromosomen niet goed compacteren en ontwarren. Deze cellen toonden lange, vage mitotische chromosomen, DNA‑bruggen tussen scheidende zusters en segregatiefouten—problemen die opvallend lijken op wat er gebeurt wanneer Wapl zelf wordt verwijderd.
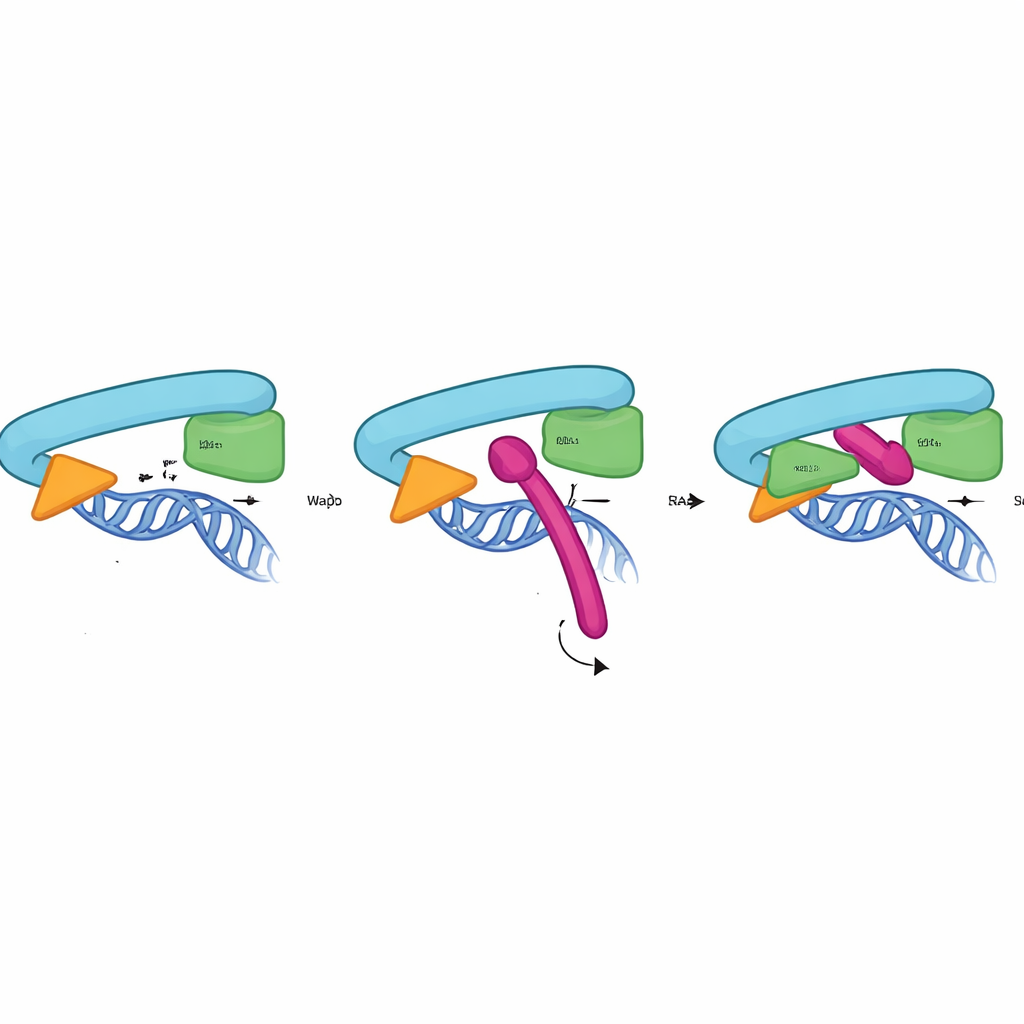
Hoe Sororins vergrendeling de ring vastgrijpt
Om te begrijpen hoe de CTR op atomair niveau werkt, combineerden de onderzoekers biochemische testen, mutagenese en AlphaFold3‑structuurvoorspellingen. Ze toonden aan dat de CTR direct en specifiek bindt aan het interface tussen RAD21 en het hoofdgedeelte van SMC3—juist die plek die de DNA‑uitgangspoort vormt. Deze interactie vereist niet Pds5 of de SA2‑subunit en vindt alleen plaats op chromatine‑gebonden cohesine, met een piek in de fase waarin cohesie stabiel behouden moet worden. Het structurele model suggereert dat een korte helix binnen de CTR in een pocket past die gevormd wordt door RAD21 en SMC3, en dat een cluster van geconserveerde hydrofobe en negatief geladen residuen gebruikt wordt om zich vast te klampen. Het muteren van slechts een paar van deze contactpunten in Sororin, RAD21 of SMC3 was voldoende om de binding te aboleren en voortijdige zuster‑scheiding te veroorzaken, wat bevestigt dat dit oppervlak fungeert als een fysieke poortvergrendeling.
Een getimede vrijgaveschakelaar voor chromosoomscheiding
Cellen moeten cohesine ook op het juiste moment loslaten. Het team ontdekte dat Sororin een nabijgelegen controlesite draagt, één aminozuur (S145) dat door de mitotische kinase Aurora B gefosforyleerd wordt. Deze modificatie breekt specifiek Sororins greep op Pds5, waardoor Wapl opnieuw kan binden en de verwijdering van cohesine van chromatidearmen bevordert, terwijl de CTR‑contacten met de RAD21–SMC3‑poort grotendeels intact blijven. In centromeren rekruteert een andere factor, Sgo1, een fosfatase die deze fosfaatgroep weghaalt, waardoor de Sororin–Pds5‑binding en sterke poortvergrendeling behouden blijven tot de definitieve knip van RAD21 in anafase. Genetische testen toonden dat wanneer Wapl wordt verwijderd, de cohesiedefecten veroorzaakt door het verstoren van de CTR–poortinteractie verdwijnen, wat onderstreept dat Sororins essentiële taak is om de uitgangspoort specifiek te beschermen tegen door Wapl gedreven opening.
Wat dit betekent voor genoomstabiliteit en ziekte
Gezamenlijk herschikken deze bevindingen Sororin als een bewaker met een dubbele functie: het concurreert met Wapl om toegang tot Pds5 en klemt direct de DNA‑uitgangspoort van cohesine dicht via zijn kleine CTR. Deze dubbele controle zorgt ervoor dat cohesie sterk is waar dat nodig is, vooral bij centromeren, maar ook dat cohesie vroeg in mitose van chromatidearmen kan worden verwijderd om juiste compacting en ontwarring mogelijk te maken. Omdat mutaties in cohesine en zijn regulatoren vaak voorkomen bij ontwikkelingsstoornissen en kankers, benadrukt het nauwkeurig in kaart gebrachte contactvlak tussen Sororin, RAD21 en SMC3 een nieuwe kwetsbaarheid waar kleine veranderingen chromosomen kunnen destabiliseren—en een potentiële doelwitplaats voor toekomstige therapieën die willen bijsturen hoe stevig ons genetisch materiaal bijeengehouden wordt.
Bronvermelding: Chen, Q., Yuan, X., Shi, M. et al. Sororin locks the DNA-exit gate of cohesin to preserve sister-chromatid cohesion. Nat Commun 17, 2284 (2026). https://doi.org/10.1038/s41467-026-70484-2
Trefwoorden: zusterchromatidecohesie, cohesinecomplex, Sororin, chromosoomsegregatie, genoomstabiliteit