Clear Sky Science · nl
Een pathogene Tau-mutatie veroorzaakt autophagie‑lysosoomdisfunctie die Tau‑afbraak beperkt in een model van frontotemporale dementie
Als de opruimploegen van de hersenen achter raken
Waarom krijgen sommige mensen tientallen jaren voor de oude dag ernstige geheugen‑ en gedragsproblemen? Deze studie pakt die vraag aan door in te zoomen op één herseneiwit, Tau, en de kleine cellulaire "recyclingcentra" die het normaal onder controle houden. Door levende menselijke zenuwcellen onder super‑scherpe microscopen te volgen, laten de onderzoekers zien hoe een ziekteveroorzakende Tau‑mutatie het afvalverwerkingssysteem van de cel verstopt en hoe het stimuleren van dat systeem met een kleine molecule kan helpen de rommel op te ruimen. Hun bevindingen wijzen mogelijk op nieuwe behandelstrategieën voor bepaalde vormen van dementie.
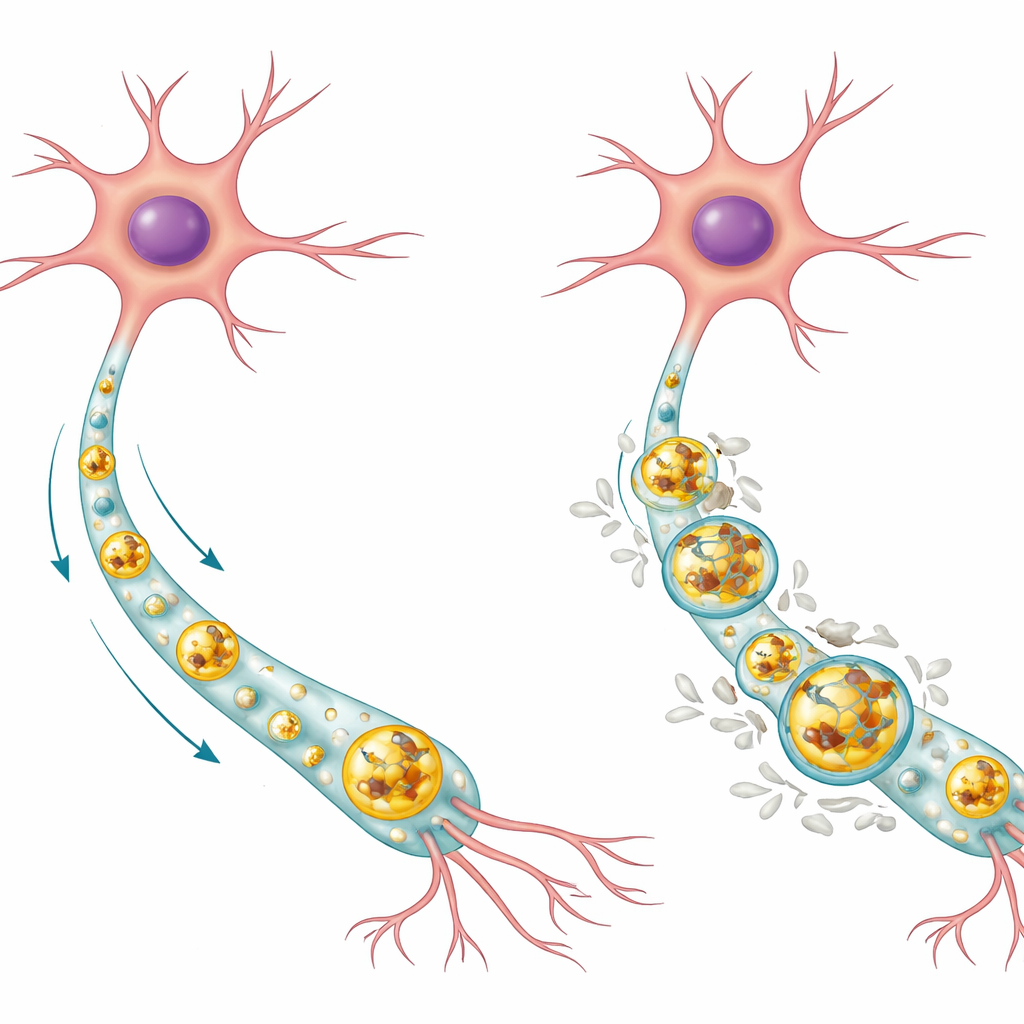
Hoe hersencellen normaal het afval afvoeren
Zenuwcellen zijn langlevende cellen die zich niet eenvoudigweg kunnen delen om beschadigd materiaal te verdunnen, dus ze vertrouwen sterk op interne opruimsystemen. Een belangrijke route is het autofagie‑lysosoompad. In dit proces worden ongewenste eiwitten en versleten onderdelen ingepakt in membraanzakken genaamd autofagosomen, die vervolgens fuseren met enzymrijke compartimenten die lysosomen worden genoemd, waar de lading wordt afgebroken en gerecycled. In gezonde menselijke neuronen vonden de auteurs dat normaal Tau‑eiwit de neiging heeft zich op te hopen in het zure centrum van lysosomen, waar het kan worden afgebroken, terwijl de gefosforyleerde vorm van Tau (een chemische modificatie die met ziekte wordt geassocieerd) zich meer op het buitenmembraan van het lysosoom bevindt. De meeste lysosomen in gezonde cellen waren helemaal vrij van Tau, wat suggereert dat dit systeem doorgaans Tau‑niveaus laag en goed gereguleerd houdt.
Wat er misgaat bij een genetische vorm van dementie
Het team concentreerde zich op een mutatie in het MAPT‑gen, p.R406W genoemd, die een erfelijke vorm van frontotemporale dementie veroorzaakt en geheugenverlies kan nabootsen dat lijkt op Alzheimer. Met stamceltechniek programmeerden ze huidcellen van patiënten om tot geïnduceerde pluripotente stamcellen en vervolgens tot grote aantallen menselijke neuronen die ofwel de mutatie droegen ofwel door genbewerking weer normaal waren gemaakt. In de gemuteerde neuronen waren totaal Tau en gefosforyleerd Tau duidelijk hoger, niet omdat de cellen meer Tau produceerden, maar omdat ze het minder efficiënt verwijderden. Superresolutie‑imaging toonde aan dat bijna alle lysosomen in de gemuteerde cellen gevuld waren met Tau en vooral met gefosforyleerd Tau dat het lysosoommembraan bedekte. Deze opeenhoping wees erop dat de belangrijkste eiwitafvoerroute van de cel vastzat.
Verstopte recyclingcentra en trage verkeersstroom
Bij nadere bestudering van de recyclagemachines zagen de onderzoekers dat lysosomen in gemuteerde neuronen talrijker, groter en geneigd waren verder van het cellichaam te liggen. Live‑imaging met fluorescerende kleurstoffen toonde dat deze lysosomen langzamer bewogen en kortere afstanden aflegden langs de zenuwvezels, hoewel de onderliggende microtubule‑sporen er normaal uitzagen. De gemuteerde neuronen bevatten ook meer autofagosomen, meer van het cargo‑adaptereiwit p62 en extra lipidedruppels—tekens dat materiaal werd gemarkeerd voor verwijdering maar niet volledig werd afgebroken. Met een pH‑gevoelige reporter vonden ze dat autofagosomen in gemuteerde cellen vaak niet goed fuseerden met lysosomen, wat leidde tot een opstapeling van "half‑afgewerkte" recyclingsblaasjes en brede defecten in de cellulaire opruiming, niet alleen voor Tau maar ook voor ander celmateriaal.
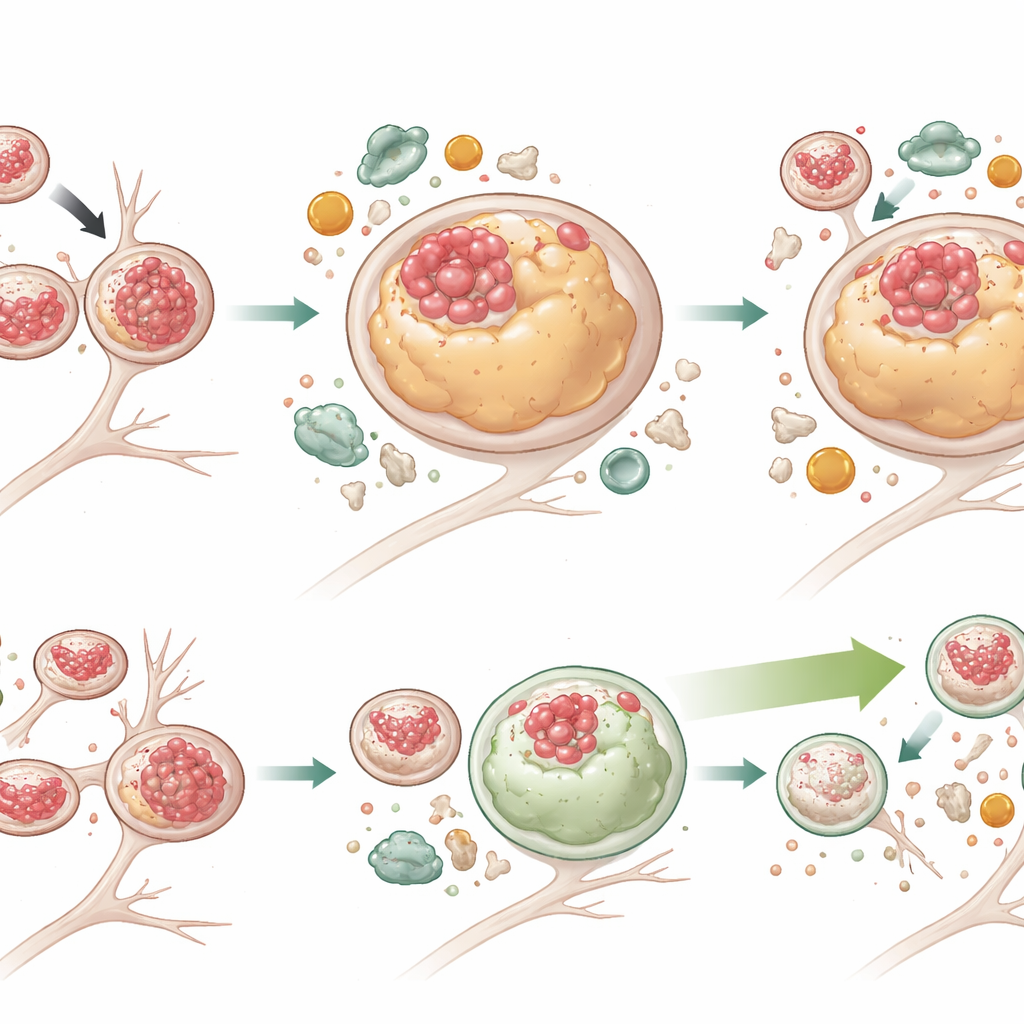
De cellulaire schoonmaak oppeppen zonder de verkeersopstopping te herstellen
Om te testen of het versterken van autofagie deze problemen kon overwinnen, behandelde het team neuronen met G2‑567, een kleine molecule die eerder is getoond het autofagie‑lysosoomsysteem te stimuleren. Na twee weken behandeling hadden de gemuteerde neuronen aanzienlijk lagere gehalten van zowel totaal Tau als gefosforyleerd Tau, en veel meer lysosomen waren opnieuw vrij van Tau. Lysosomen krimpten ook weer naar een meer normale grootte. Merkers van actieve autofagie namen toe, terwijl p62—een indicator van vastgelopen degradatie—afnam in gemuteerde cellen, wat een effectievere afbraak van cargo aantoont. Interessant genoeg corrigeerde G2‑567 niet alle defecten: lysosomen in gemuteerde neuronen bleven de neiging houden verder van het cellichaam te liggen en traag te bewegen, en een adaptereiwit (JIP3) dat aan lysosoomtransport is gekoppeld bleef verhoogd. Dit suggereert dat de bewegings‑ en afbraakfuncties van lysosomen deels ontkoppeld kunnen zijn en dat het verbeteren van de afbraak op zichzelf voldoende kan zijn om toxische Tau‑ophopingen te verminderen.
Wat dit betekent voor toekomstige dementiebehandelingen
Voor niet‑specialisten is de belangrijkste conclusie dat in dit genetische model van frontotemporale dementie het probleem niet alleen is dat Tau abnormaal wordt; het probleem is dat het neuronale recyclingsysteem het niet bijhoudt. De p.R406W‑Tau‑mutatie verstoort rechtstreeks meerdere stappen van het autofagie‑lysosoompad, waardoor Tau—vooral de gefosforyleerde vorm—zich ophoopt op en in lysosomen, samen met ander onverwerkt materiaal. Door het cellulair opruimmechanisme farmacologisch een zetje te geven, konden de onderzoekers Tau‑niveaus verlagen en de lysosoomgrootte normaliseren, ook al bleven transportdefecten bestaan. Deze bevindingen versterken het idee dat geneesmiddelen die veilig autofagie en lysosomale functie stimuleren, kunnen helpen het eiwit evenwicht te herstellen bij tau‑gerelateerde dementieën en mogelijk ook bij meer voorkomende aandoeningen zoals de ziekte van Alzheimer.
Bronvermelding: Mirfakhar, F.S., Marsh, J.A., Sato, C. et al. A pathogenic Tau mutation drives autophagy-lysosome dysfunction that limits Tau degradation in a model of frontotemporal dementia. Nat Commun 17, 2699 (2026). https://doi.org/10.1038/s41467-026-70473-5
Trefwoorden: tau‑eiwit, autofagie, lysosoomdysfunctie, frontotemporale dementie, neurodegeneratie