Clear Sky Science · nl
Oppervlaktehydrofobiciteit en stijfheid bepalen het proteïnecorona op oraal toegediende nanodeeltjes voor de behandeling van colitis
Tabletten verandert in slimmere behandelingen
Mensen met inflammatoire darmaandoeningen zoals colitis gebruiken vaak sterke ontstekingsremmers, maar een groot deel van elke dosis gaat verloren of veroorzaakt bijwerkingen elders in het lichaam. Deze studie onderzoekt een nieuwe manier om orale medicijnen meer als geleide raketten te laten werken: door het ontwerpen van kleine, medicijn-dragende deeltjes die de eigen darmproteïnen van het lichaam inzetten als een natuurlijk targetsysteem, zodat geneesmiddelen zich richten op de immuuncellen die de ontsteking in de darm aansturen.
Hoe de darm nanodeeltjes aankleedt
Wanneer een nanodeeltje het lichaam binnendringt, wordt het snel bedekt door een dunne laag eiwitten, het zogenaamde “proteïnecorona.” In de zieke darm verschilt dat corona sterk van dat in gezond weefsel omdat de lokale eiwitmix is veranderd. De auteurs ontdekten eerder dat colitis een specifiek intestinaal corona genereert dat deeltjes lichtjes richting immuuncellen genaamd macrofagen stuurt, cellen die zowel ontsteking aanjagen als helpen oplossen. Hier wilden ze dat corona doelbewust vormen door twee basiskenmerken van medicijndragende deeltjes aan te passen — hun waterafstotendheid (hydrofobiciteit) en hun stijfheid (rigiditeit) — om een bescheiden, door de ziekte gemaakte werking om te zetten in een krachtige targetingstrategie.
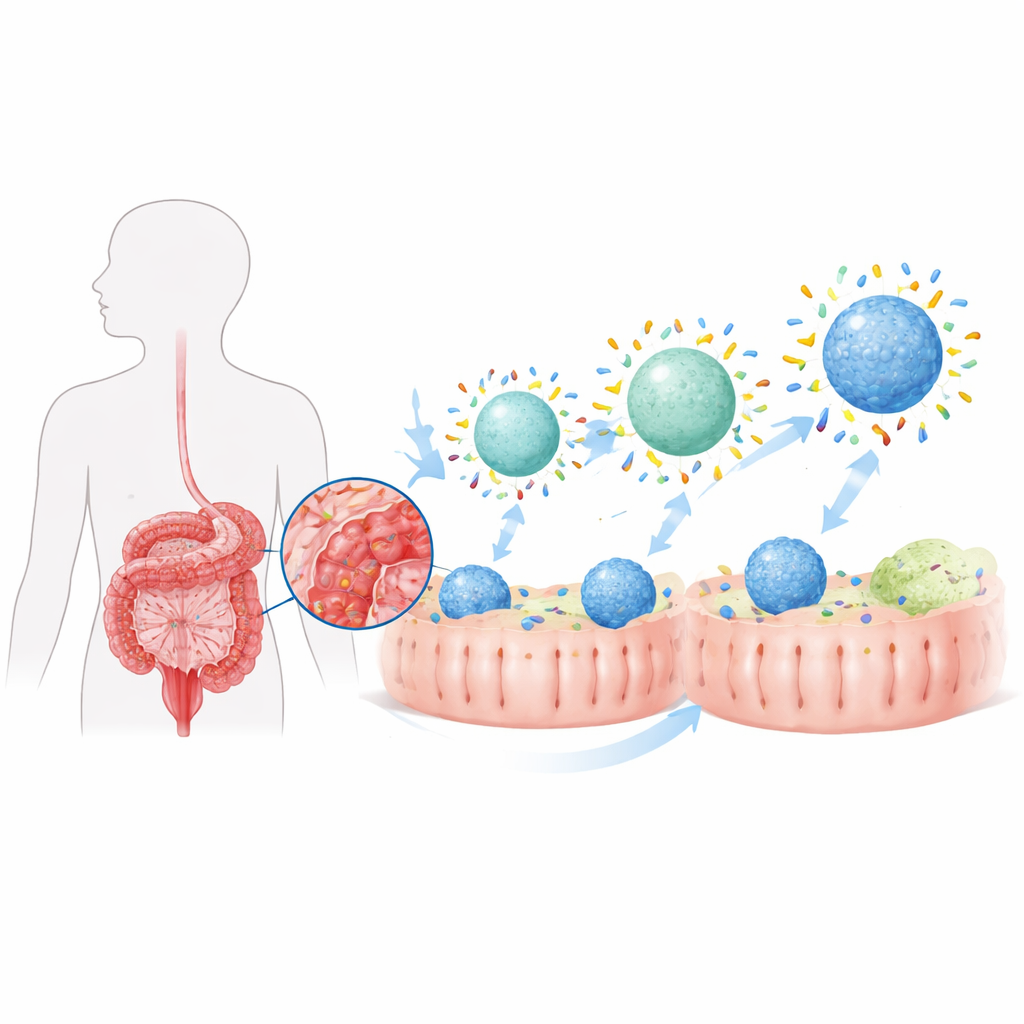
Deeltjes aantrekkelijker maken voor eiwitten
Het team bouwde lipide-gebaseerde nanodeeltjes, vergelijkbaar met kleine vetbelletjes, en stelde de mate waarin hun oppervlak waterminnend of waterafstotend was bij door verschillende hoeveelheden van een veelgebruikt polymeercoating toe te voegen. Deeltjes met meer hydrofobe oppervlakken bonden veel meer darmproteïnen wanneer ze werden blootgesteld aan colitisvloeistoffen, zowel in dieren als in reageerbuizen. Wanneer deze “phobic” deeltjes werden geladen met het steroid budesonide en oraal aan ratten met colitis werden gegeven, leverden ze veel meer geneesmiddel aan colon-macrofagen dan meer waterminnende varianten. Daardoor kregen behandelde dieren meer lichaamsgewicht terug, vertoonden ze minder verkorting en weefselschade van de darm en hadden ze lagere niveaus van ontstekingsmoleculen in de darm. Hoewel de ontsteking verbeterde, keerde de toestand niet volledig terug naar gezond, wat suggereert dat het simpelweg vergroten van de totale hoeveelheid coronaproteïnen niet voldoende was.
Deeltjes verharden om betere partners te kiezen
Om het concept verder te brengen, hielden de onderzoekers de oppervlakken hydrofoob maar veranderden ze de interne structuur om de deeltjes zacht, gematigd of stijf te maken door hun kern te vullen met plastic bolletjes van verschillende grootte. Alle drie namen nog steeds vergelijkbare totale hoeveelheden darmproteïne op, maar de samenstelling van die eiwitten veranderde. De stijfste deeltjes vormden coronas die bijzonder rijk waren aan eiwitten die zich kunnen hechten aan receptoren op macrofagen of kleine voedingsstoffen kunnen vervoeren die die cellen opnemen. Een van die eiwitten, S100A8, is overvloedig aanwezig in ontstoken darmen en kan specifieke macrofaagreceptoren aanspreken. Het blokkeren van S100A8 op het corona verminderde sterk de opname van de stijve deeltjes door macrofagen, wat het als een sleutelcomponent van targeting identificeert die door de stijfheid van het deeltje werd geselecteerd.
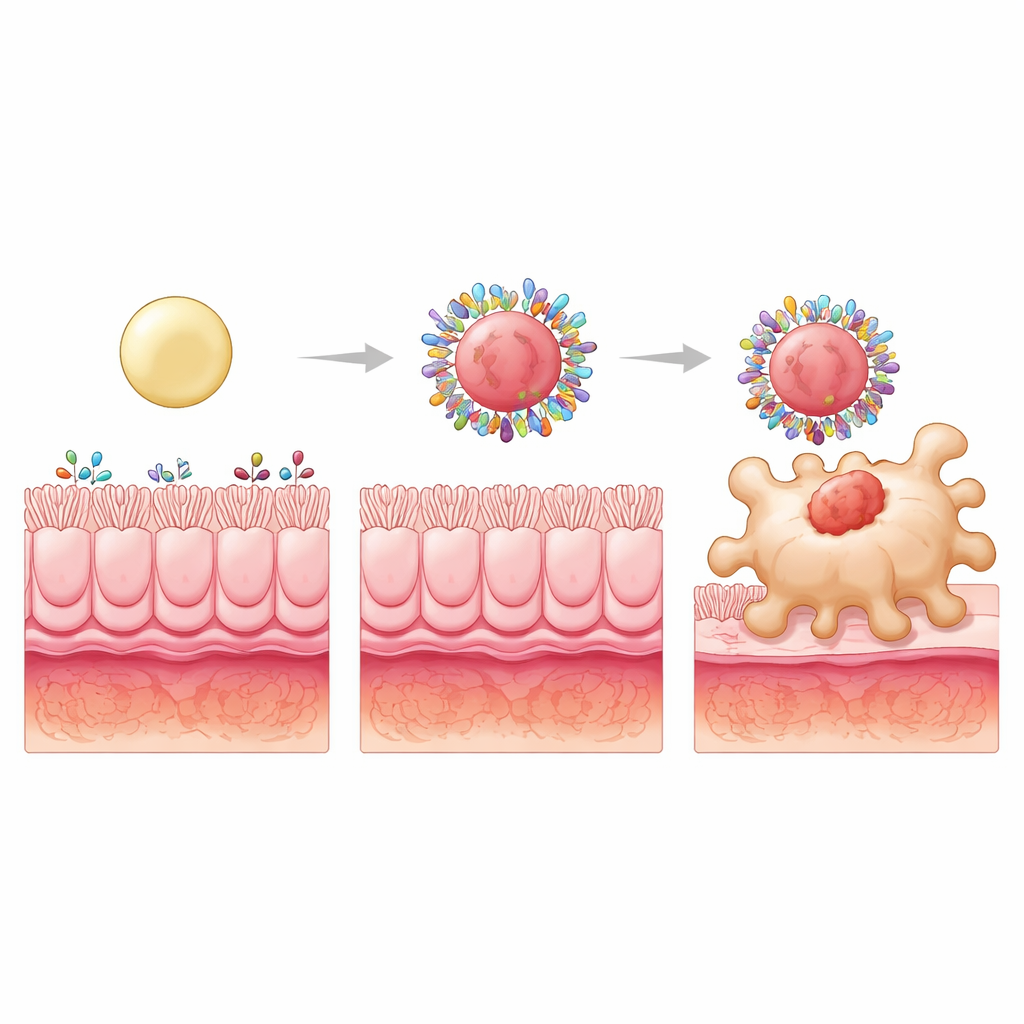
Van betere targeting naar betere genezing
Wanneer budesonide in deze hoog-hydrofobe, hoog-stijve deeltjes werd verpakt en oraal aan ratten met colitis werd toegediend, waren de voordelen opvallend. De stijve formulering verminderde niet alleen darmschade en oxidatieve stress, maar normaliseerde ook meerdere ontstekingssignalen tot niveaus die in gezonde dieren werden gezien. Het herstelde een gezondere balans tussen ‘aanvallende’ en ‘kalmerende’ macrofaagtypen en versterkte regulerende T-cellen, die helpen immuunreacties in bedwang te houden. Belangrijk is dat deze verbeteringen afhankelijk waren van de door de ziekte gewijzigde proteïne-omgeving in colitis; hetzelfde ontwerp toonde geen bijzondere targeting in gezonde ratten, wat benadrukt dat het corona een dynamische, ziekte-specifieke bondgenoot is.
Waarom dit ertoe doet voor toekomstige medicijnen
Dit werk laat zien dat we de eigen eiwitten van het lichaam kunnen sturen om als slimme, zichzelf vernieuwende “labels” op orale geneesmiddeldragers te fungeren door simpelweg de oppervlakte- en mechanische eigenschappen van de dragers af te stemmen. Door eerst de eiwitvangst te vergroten via hydrofobe oppervlakken en vervolgens stijfheid te gebruiken om macrofaag-homing eiwitten zoals S100A8 te bevoordelen, creëerden de onderzoekers nanodeeltjes die van nature de immuuncellen zoeken die colitis aansturen en therapie afleveren waar die het meest nodig is. Dezelfde ontwerplogica — het manipuleren van hoe deeltjes aanvoelen en zich gedragen aan het darmslijmvlies — kan worden aangepast aan vele typen nanotherapieën en ziekten, en biedt een nieuwe, subtiele route naar gerichte behandeling zonder het bevestigen van kunstmatige targetmoleculen.
Bronvermelding: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
Trefwoorden: nanodeeltjes geneesmiddelafgifte, inflammatoire darmziekte, proteïnecorona, orale nanotherapie, macrofagen targeting