Clear Sky Science · nl
Een geslachtsbrede interactie-atlas over NS4B-orthologen identificeert een geconserveerde rol voor UFMylatie bij orthoflavivirusreplicatie
Waarom deze virusstudie ertoe doet
Virussen zoals dengue, Zika en West-Nijl verspreiden zich naar nieuwe gebieden en kunnen uiteenlopende ziekten veroorzaken, van koorts tot herseninfecties en aangeboren aandoeningen. Toch missen we nog steeds brede, betrouwbare behandelingen. Deze studie onderzoekt hoe een verborgen samenwerking tussen deze virussen en een weinig bekend cellulair etiquetteringssysteem, UFMylatie, de vermenigvuldiging van de pathogenen bevordert. Door deze relatie te charten over veel verwante virussen, onthullen de auteurs een gedeelde kwetsbaarheid die benut zou kunnen worden voor de ontwikkeling van toekomstige antivirale middelen.
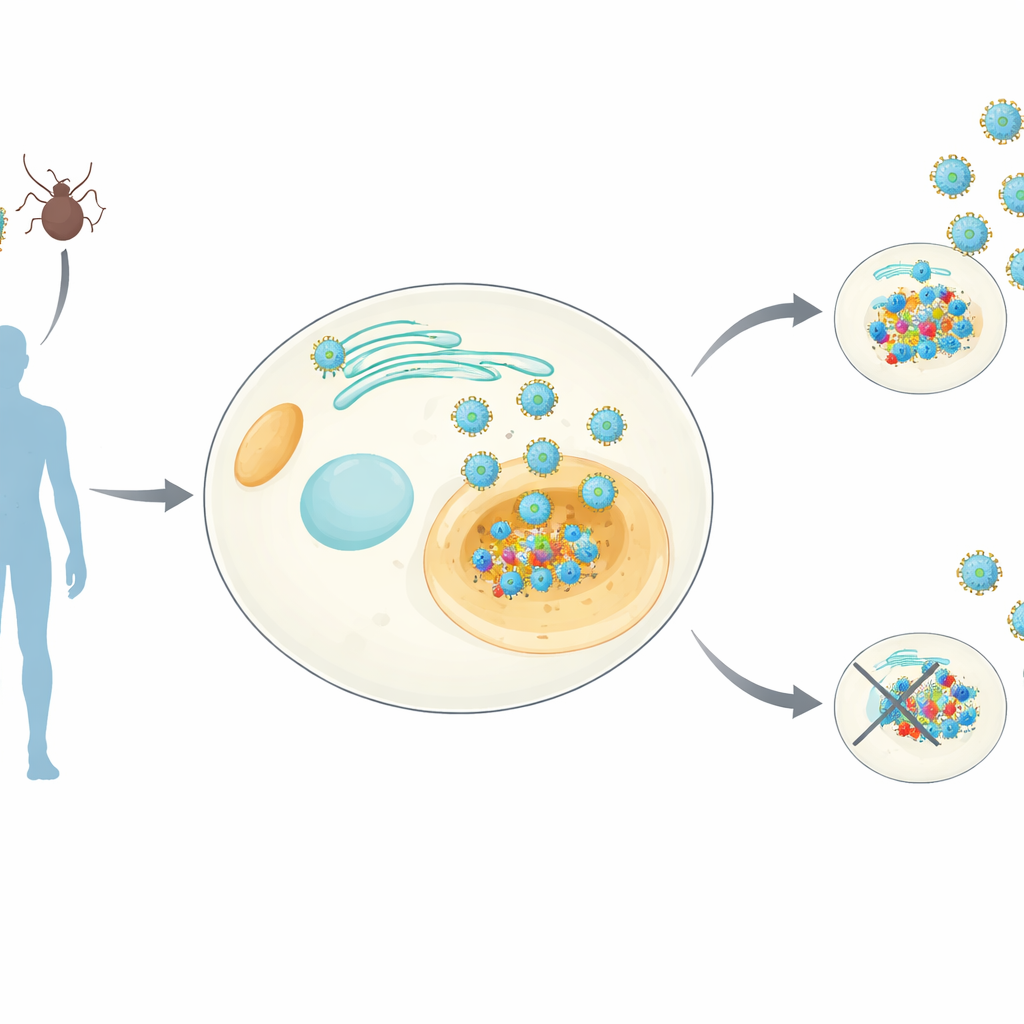
Een belangrijke virale insider volgen
Orthoflavivirussen – de groep waartoe dengue, Zika, gele koorts en andere behoren – dragen allemaal een klein eiwit genaamd NS4B dat zich nestelt in membranen binnen onze cellen. NS4B is bekend als essentieel voor virale replicatie, maar de precieze functies bleven onduidelijk. De onderzoekers creëerden humane cellijnen die stabiel NS4B van acht verschillende orthoflavivirussen produceren. Vervolgens gebruikten ze gevoelige massaspectrometrietegnieken om NS4B samen met eventuele eraan gebonden menselijke eiwitten te isoleren, en maten parallel hoe de expressie van NS4B de totale samenstelling van eiwitten in de cel verandert. Dit leverde een geslachtsbrede "interactie-atlas" op – die zij de NS4Bome noemen – waarmee zowel gemeenschappelijke als virus-specifieke gastheereiwitdoelen werden getoond.
Gedeelde trucs en op maat gemaakte hacks
De atlas liet 538 menselijke eiwitten zien die met NS4B interageren en meer dan 500 waarvan de hoeveelheid verandert wanneer NS4B aanwezig is. Veel van deze eiwitten concentreren zich in paden die energieproductie in mitochondriën beheren, de vorming van interne membranen en het transport van nieuwgemaakte eiwitten en vetten. Sommige interacties waren gedeeld door de meeste virussen, wat wijst op evolutionair geconserveerde trucs die alle orthoflavivirussen gebruiken. Andere verschenen alleen in bepaalde species of stammen, wat mogelijk verklaart waarom sommige virussen muggen boven teken verkiezen, of hersenziekte veroorzaken in plaats van hemorragische koorts. Dit systematische overzicht zet een wirwar van eerdere, gefragmenteerde studies om in een coherent kaartbeeld van hoe deze virussen de cel herschakelen.
Een verrassende bondgenoot: het UFMylatiesysteem
Onder de vele partners waaraan NS4B zich hechtte, stak er één bovenuit: UBA5, het startenzym van de UFMylatie-route. UFMylatie is een cellulair systeem dat een klein eiwitlabel, UFM1, aan geselecteerde doelwitten koppelt en zo processen beïnvloedt zoals eiwitkwaliteitscontrole en stressreacties. Met RNA-interferentie en CRISPR-gebaseerde genuitwissing toonde het team aan dat cellen zonder UBA5 of anderszins niet in staat om UFMylatie uit te voeren, een sterk gereduceerde replicatie van Zika en verschillende verwante virussen vertoonden. Het opnieuw introduceren van normaal UBA5 herstelde de virusgroei, terwijl mutantvormen die UFMylatie niet meer konden aandrijven dat niet deden, wat bewijst dat de etiquetteringsactiviteit zelf cruciaal is voor infectie.
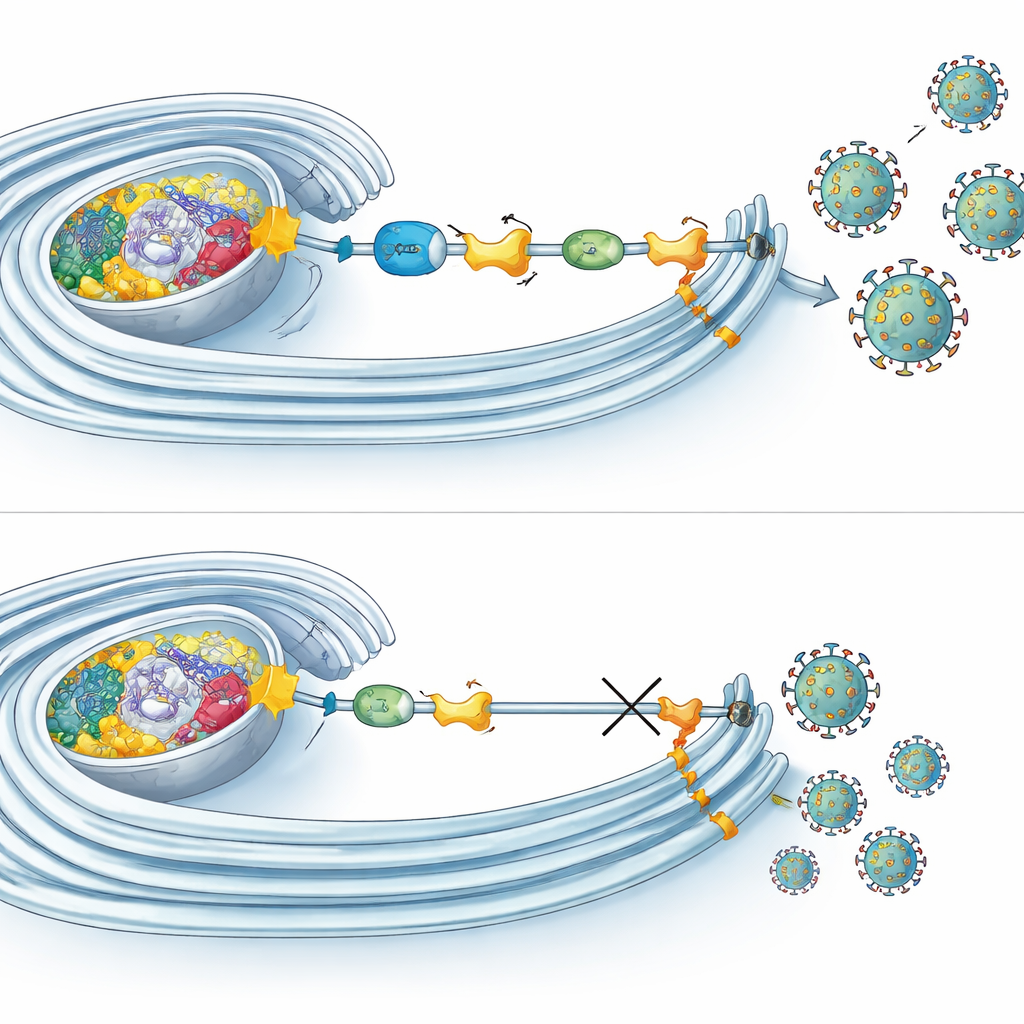
Hoe etiquettering virale fabrieken ondersteunt
Microscopie- en biochemische experimenten toonden aan dat meerdere UFMylatiecomponenten zich verzamelen op precies die locaties waar viraal RNA wordt gekopieerd binnen heringerichte membranen. Daar associëren ze niet alleen met NS4B, maar ook met andere virale eiwitten die het replicatiemechanisme vormen. Interessant genoeg stopte het blokkeren van UFMylatie de virale binnenkomst, RNA-productie of eiwitsynthese niet. In plaats daarvan verlamde het vooral de late stadia van de cyclus, zoals de assemblage of het vrijkomen van infectieuze deeltjes. Tegelijk bleek UFMylatie invloed te hebben op de ademhaling van mitochondriën: wanneer de route werd uitgeschakeld, vertoonden cellen verminderde zuurstofconsumptie en gewijzigde mitochondriale vormen. In tegenstelling daarmee nam de mitochondriale ademhaling vroeg tijdens Zika-infectie juist toe, wat suggereert dat virussen mogelijk UFMylatie aanboren om de energieproductie van de cel te verhogen op het moment dat ze die het meest nodig hebben.
Een geneesmiddel testen in cellen en kleine vissen
De auteurs richtten zich vervolgens op een kleinmolecuulverbinding, DKM 2-93, die het actieve centrum van UBA5 blokkeert. In gekweekte menselijke cellen verminderde deze remmer de Zikavirusproductie ruwweg tienvoudig bij doseringen die de cellen grotendeels gezond lieten en toonde activiteit in verschillende celtypes. Om te onderzoeken of deze strategie in een levend organisme zou werken, gebruikten ze een zebravismodel van Zika-infectie, dat belangrijke kenmerken van de ziekte in de zich ontwikkelende hersenen nabootst. Behandeling van geïnfecteerde embryo’s met DKM 2-93 tijdens vroege hersenontwikkeling verlaagde het virale RNA-niveau aanzienlijk en verminderde het aandeel vissen met ernstige misvormingen, wat wijst op een reëel antiviraal voordeel in vivo.
Wat dit betekent voor toekomstige behandelingen
Door een uitgebreid kaartbeeld te maken van hoe NS4B van vele orthoflavivirussen met menselijke eiwitten interageert, benadrukt deze studie UFMylatie als een geconserveerd hulptraject waarop deze virussen vertrouwen om infectieuze deeltjes te produceren. Aangezien hetzelfde gastsysteem dengue, Zika, West-Nijl en anderen lijkt te ondersteunen, zouden geneesmiddelen die UFMylatie selectief dempen als breed-spectrum antiviralia kunnen werken, in plaats van één virus tegelijk aan te pakken. Hoewel meer onderzoek nodig is om precies te begrijpen welke eiwitten worden getagd en om de veiligheid te waarborgen, identificeren de bevindingen een veelbelovend op gastheer gebaseerd doel dat op een dag zou kunnen helpen uitbraken van meerdere door muggen en teken overgedragen ziektes met één therapeutische benadering te verminderen.
Bronvermelding: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
Trefwoorden: Zikavirus, dengue, gastheer–virusinteracties, UFMylatie, breed-spectrum antiviralia