Clear Sky Science · nl
3D pentacultuurmodel onthult door kwaadaardige cellen aangedreven macrofaagpolarisatie bij hooggradig sereus ovariumcarcinoom
Waarom dit onderzoek ertoe doet
Eierstokkanker wordt vaak laat ontdekt en kan hardnekkig resistent zijn tegen behandeling. Een reden is dat kankercellen leven binnen een ondersteunende buurt van immuun- en bindweefselcellen die hen helpen medicijnen en de afweer van het lichaam te ontwijken. Deze studie bouwt een geavanceerd laboratoriummodel—met vijf typen humane cellen in 3D—om die buurt na te bootsen en in real time te observeren hoe kankercellen nabije immuuncellen, zogenaamde macrofagen, zover krijgen dat ze de tumor helpen in plaats van bestrijden.
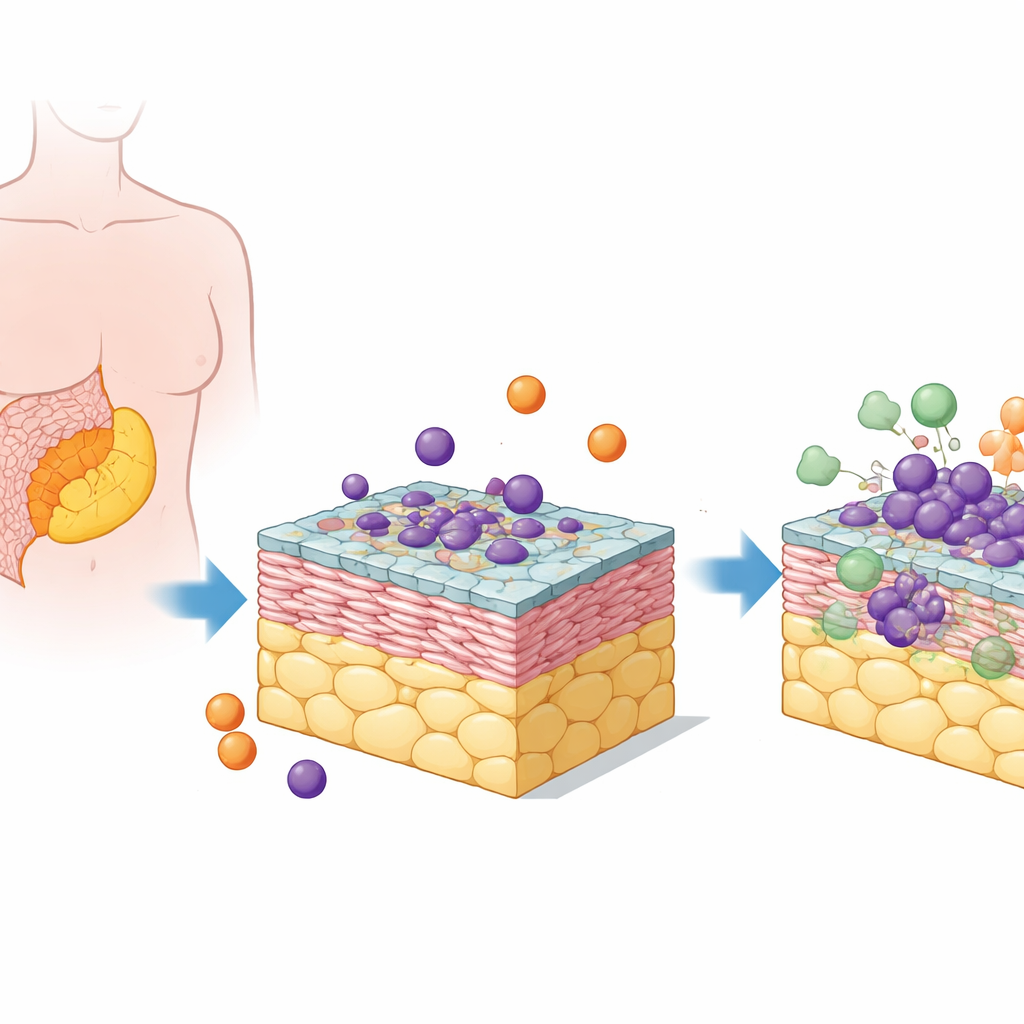
Het bouwen van een klein tumorkwartier
De onderzoekers richtten zich op hooggradig sereus eierstokkanker, de meest voorkomende en dodelijke vorm van de ziekte. De uitzaaiingen groeien vaak in een vetrijk weefsel in de buikholte dat het omentum wordt genoemd. Om deze omgeving na te bootsen, combineerde het team menselijke vetcellen, bindweefselcellen (fibroblasten), een bekleding van mesotheelcellen, eierstokkankercellen en circulerende immuuncellen genaamd monocyten. Deze vijf celtypes werden samengesteld tot gestapelde 3D “pentaculturen” die meer lijken op echte tumorafzettingen dan platte cellagen in een schaaltje.
Verdedigers van het immuunsysteem tot toeschouwers maken
Binnen deze mini‑tumoromgeving rijpten monocyten spontaan uit tot macrofagen—zonder de kunstmatige groeisignalen die normaal in het laboratorium worden toegevoegd. Met gen‑activiteitsprofilering en vergelijking met single‑cellgegevens uit patiënttumoren toonden de onderzoekers aan dat de macrofagen in het model sterk overeenkomen met die in echte eierstokmetastasen. Verschillende kankercellijnen produceerden uiteenlopende mengsels van macrofaagtypen en verschillende architecturen van de mini‑tumoren, wat erop wijst dat genetische en moleculaire verschillen in kankercellen sterk de omliggende immuunomgeving vormen.
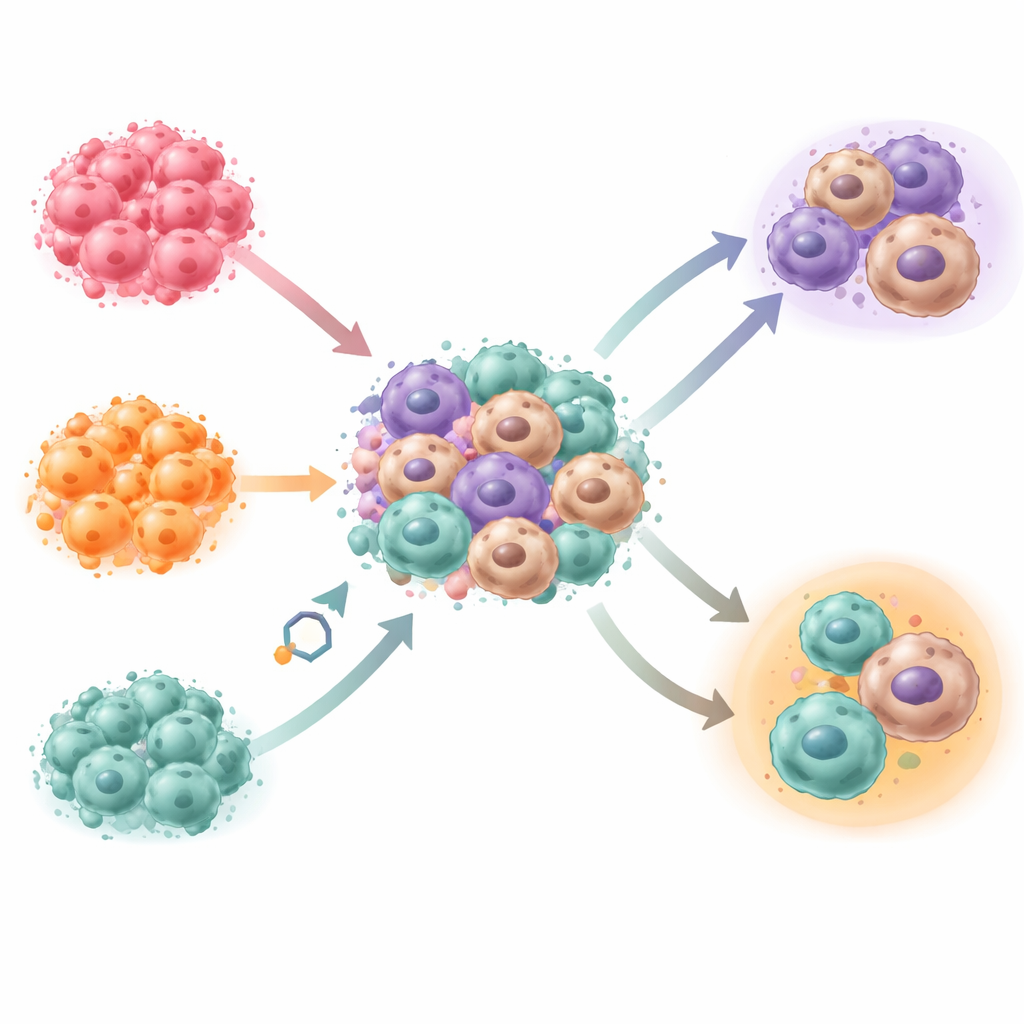
Hoe kankercellen vermijden te worden opgegeten
Macrofagen kunnen kankercellen opslokken en vernietigen, maar tumoren zenden vaak “eet‑me‑niet” signalen uit aan hun oppervlak. Het team onderzocht twee van zulke signalen, CD47 en CD24, op drie eierstokkankercellijnen gekweekt in het 3D‑model. Kankercellen met hogere niveaus van deze signalen werden minder vaak door macrofagen opgegeten. In de pentaculturen werd de ene cellijn bereidelijk gegeten, ontsnapte een andere grotendeels, en vertoonde een derde een gemengd gedrag. Live‑beelden toonden dat macrofagen zich verschillend bewogen en zich dichterbij of verder van kankergroeperingen positioneerden afhankelijk van de cellijn, wat patronen weerspiegelt die in patiëntweefsels worden gezien.
Manieren testen om de immuunaanval te heractiveren
Aangezien deze oppervlaksignalen met antilichaamtherapieën geblokkeerd kunnen worden, behandelden de onderzoekers de modellen met experimentele antilichamen gericht tegen CD47 of CD24. In pentaculturen gebouwd met een specifieke cellijn vergrootte het blokkeren van elk signaal de contacten tussen macrofagen en kankercellen, bevorderde opslokking en verminderde het aantal kankercellen, terwijl andere cellen in het model grotendeels ongemoeid bleven. In een andere cellijn met sterke resistentie had het blokkeren van deze signalen weinig effect, maar het remmen van een afzonderlijke communicatieroute (de TGFβ‑route) verminderde het aantal kankercellen op een manier die nog steeds afhankelijk was van de aanwezigheid van macrofagen—wat wijst op alternatieve, niet‑opslokkende dodingmechanismen zoals toxische cytokineafgifte.
Wat dit voor patiënten betekent
Voor de niet‑specialistische lezer is de kernboodschap dat niet alle eierstokkankers immuuncellen op dezelfde manier manipuleren, zelfs als ze er onder de microscoop hetzelfde uitzien. Door een realistisch vijf‑cel 3D‑model uit menselijk weefsel te bouwen, laat dit werk zien hoe tumoren macrofagen kunnen afstemmen om hen te negeren of aan te vallen, en hoe het blokkeren van specifieke “eet‑me‑niet” signalen die omschakeling soms kan omkeren. Het model bootst patiënttumoren nauwgezet na en vormt daardoor een veelbelovende medium‑throughput testomgeving om uit te zoeken welke immuun‑gerichte middelen waarschijnlijk werken bij welke tumorprofielen. Op de lange termijn zouden zulke op maat gemaakte lab‑systemen kunnen helpen individuele patiënten te koppelen aan therapieën die het best hun eigen immuuncellen tegen eierstokkanker kunnen heractiveren.
Bronvermelding: Malacrida, B., Elorbany, S., Laforêts, F. et al. 3D pentaculture model unveils malignant cell-driven macrophage polarization in high-grade serous ovarian cancer. Nat Commun 17, 2451 (2026). https://doi.org/10.1038/s41467-026-70398-z
Trefwoorden: eierstokkanker, tumormicro-omgeving, macrofagen, immunotherapie, 3D celkweek