Clear Sky Science · nl
Ribosomale modificaties geassocieerd met mesenchymale fatedifferentiatie in de neurale-kamlijn
Hoe piepkleine celfabrieken gezichten en tumoren vormgeven
Onze gezichten en delen van ons zenuwstelsel ontstaan uit een zwervende groep embryo¬cellen die de neurale kam worden genoemd. Deze cellen kunnen zich differentiëren tot bot, kraakbeen, zenuwen en meer. Deze studie toont aan dat hun keuzes niet alleen door genen worden bepaald, maar ook door subtiele chemische aanpassingen van de eiwitproducerende machines in de cel—de ribosomen. Dezelfde moleculaire kenmerken die helpen een normaal gezicht te bouwen, kunnen, wanneer ze verkeerd worden gereguleerd, wijzen op gevaarlijkere vormen van kinder¬kanker.
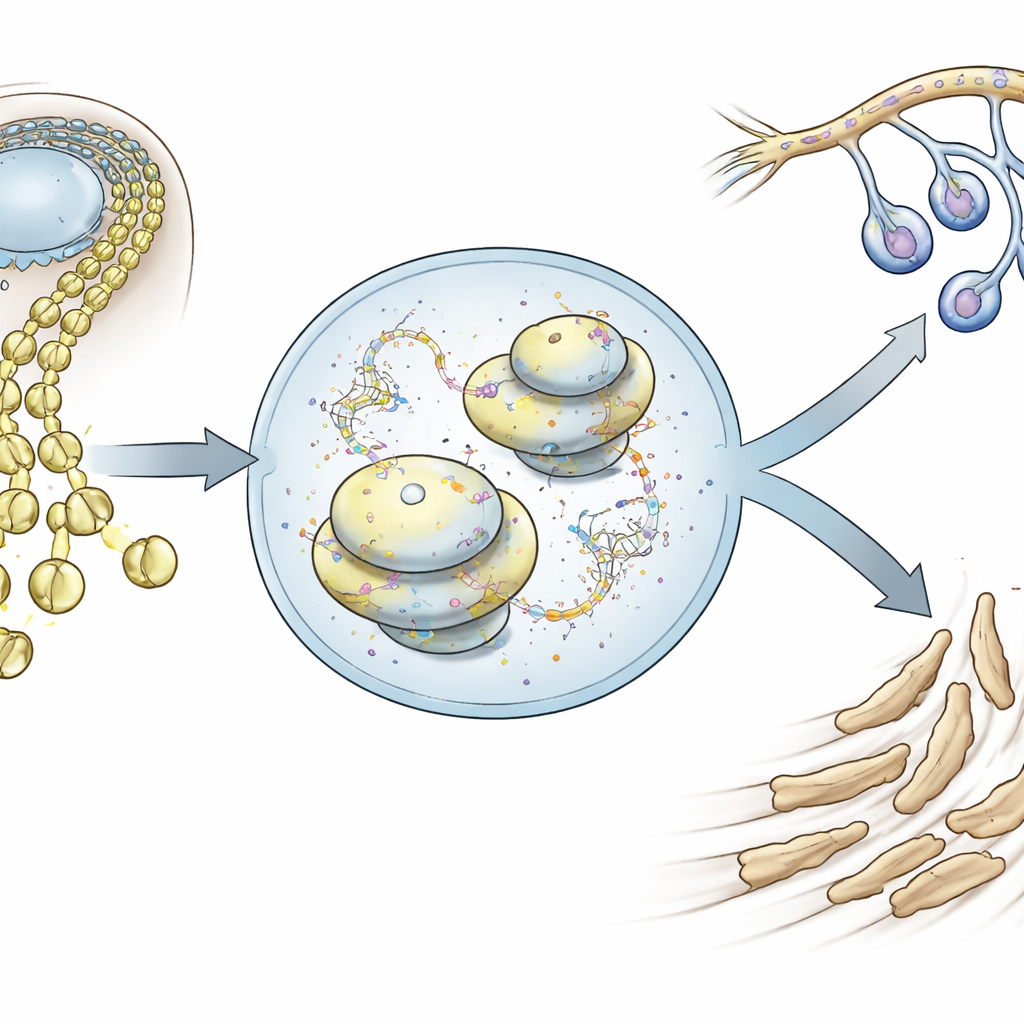
Vormveranderende cellen die het gezicht bouwen
Neurale-kamcellen ontstaan langs het vroege brein en ruggenmerg en migreren vervolgens naar buiten, waar ze uiteindelijk een groot deel van de schedel, kaken en perifere zenuwen vormen. Met single-cell RNA-sequencing in muizenembryo’s volgden de auteurs duizenden individuele craniale neurale-kamcellen terwijl ze de neurale buis verlieten en naar het gezicht trokken. Ze ontdekten dat deze cellen al heel vroeg een subtiele neiging vertonen richting een van twee hoofdtoekomsten: een mesenchymale route die gezichtsbot en kraakbeen vormt, of een neuro-gliale route die neuronen en gliale steuncellen vormt. Deze twee genactiviteitsprogramma’s zijn aanvankelijk door elkaar aanwezig in dezelfde cellen, maar worden onderling exclusief naarmate de ontwikkeling voortschrijdt, waardoor een fate-beslissing wordt afgedwongen.
Eiwitfabriekjes als beslissers
Toen het team bekeek welke genen gekoppeld waren aan de vroege bias richting gezichtsmesenchym, vonden ze twee hoofdgroepen. De ene bevatte bekende factoren die cellen helpen los te maken, te bewegen en van identiteit te veranderen, een proces dat bekendstaat als epitheliale-naar-mesenchymale transitie. De andere, meer verrassende groep draaide om ribosoomassemblage en chemische modificatie van ribosomaal RNA, de kern van de eiwitproducerende machinerie. In plaats van simpelweg meer ribosomen te maken, zetten craniale neurale-kamcellen factoren aan die fijn afstellen hoe ribosomen worden opgebouwd en chemisch gemarkeerd. Het verstoren van de productie van ribosomaal RNA in muizenembryo’s op het moment van de fate-keuze spaarde grotendeels de zich ontwikkelende zenuwen maar remde de gezichtsbeenderen sterk, wat aantoont dat de mesenchymale route bijzonder afhankelijk is van deze ribosomale controle.
Een speciale markering op ribosomaal RNA
Dieper gravend richtten de onderzoekers zich op één nucleotide binnen het 18S ribosomaal RNA, op een plek die cruciaal is voor nauwkeurige eiwitsynthese. In craniale neurale-kamcellen met een bias naar mesenchymale bestemmingen, gaf sequencing herhaaldelijk een foutieve lezing op deze positie—een kenmerk van zware chemische modificatie eerder dan van een echte mutatie. Eerder werk liet zien dat een drietal enzymen hier een complexe modificatie aanbrengt via meerdere stappen. Door menselijk genoom- en RNA-gegevens te combineren met massaspectrometrie van muizenembryonale weefsels, bevestigde de studie dat deze site normaal is in het DNA maar chemisch veranderd in het RNA in variërende mate, en dat de verhouding van deze gemodificeerde vorm verschilt tussen hersen- en gezichtweefsels. Het overexpressen of uitzetten van de enzymen die deze modificatie bouwen in celkweken en in muizenembryo’s verstoorde de neurale-kamontwikkeling en produceerde opvallende craniofaciële afwijkingen, waarmee werd onderstreept dat precieze niveaus van dit RNA-merkteken cellen helpen richting de skeletvormende route te sturen.
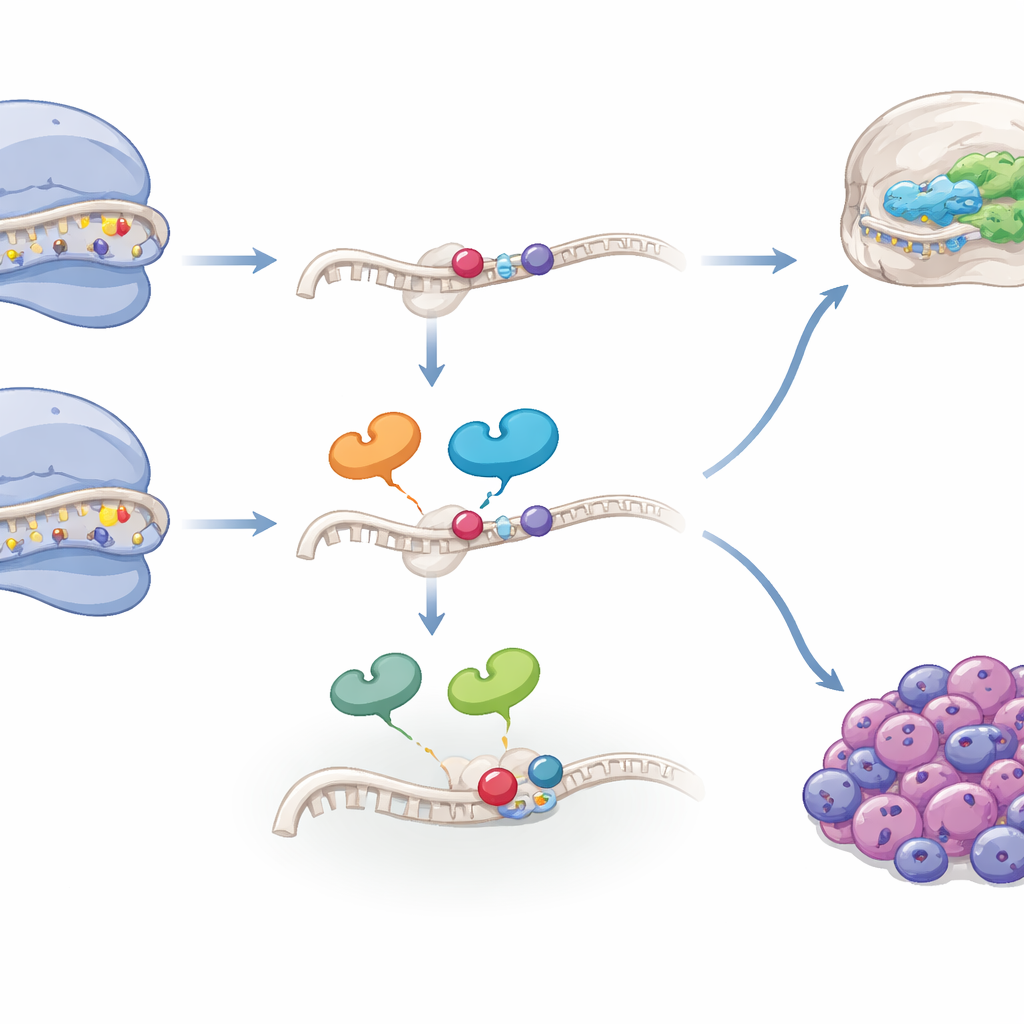
Van ontwikkeling naar kankerrisico
Aangezien neurale-kamcellen ook tumoren zoals neuroblastoom kunnen voortbrengen, onderzochten de auteurs of dezelfde ribosomale kenmerken in kanker voorkomen. Analyse van single-cell en bulk RNA-gegevens uit meerdere neuroblastoom- en hersentumorcohorten toonde aan dat een ribosomaal "controle en RNA-modificatie" genhandtekening verrijkt is in tumorcelsubpopulaties met meer mesenchymale eigenschappen—toestanden die vaak samenhangen met therapieresistentie en slechte prognose. In meerdere patiëntcohorten voorspelden hoge niveaus van deze handtekening sterk slechtere overleving, met name bij neuroblastoomgevallen zonder amplificatie van het bekende risicogen MYCN. Specifieke componenten, zoals het assemblagefactor WDR74 en het modificatie-enzym TSR3, waren verhoogd in agressieve cellijnen en maakten deze cellen gevoeliger voor medicijnen die het ribosoom belasten. Intrigerend genoeg deden tumoren met zeer lage of zeer hoge niveaus van de sleutel-RNA-modificatie op de aangegeven positie het slechter dan tumoren met intermediaire niveaus, wat suggereert dat zowel tekort als overschot van deze gespecialiseerde ribosoompool schadelijk kan zijn.
Wat dit betekent voor gezichten en kinder¬kankers
Gezamenlijk suggereren deze bevindingen dat ribosomen niet slechts passieve eiwitfabrieken zijn maar afgestemde apparaten waarvan de chemische samenstelling helpt bepalen hoe embryo¬cellen het gezicht opbouwen en hoe sommige tumoren zich gedragen. In neurale-kamcellen lijkt een specifieke chemische markering op ribosomaal RNA de productie te bevorderen van eiwitten die nodig zijn voor de vorming van gezichtsbot en kraakbeen, terwijl de ontregeling ervan in kanker gekoppeld is aan gevaarlijkere, vormveranderende tumorcellen. Begrijpen en mogelijk gericht beïnvloeden van deze ribosomale “fijnafstemming” kan nieuwe wegen openen om craniofaciële misvormingen te voorkomen en om hoogrisico-neuroblastomen te identificeren of te behandelen.
Bronvermelding: Poverennaya, I., Murtazina, A., Li, L. et al. Ribosomal modifications are associated with mesenchymal fate selection in the neural crest lineage. Nat Commun 17, 2326 (2026). https://doi.org/10.1038/s41467-026-70375-6
Trefwoorden: neurale kamontwikkeling, ribosoommodificaties, craniofaciële vorming, neuroblastoom, gespecialiseerde ribosomen