Clear Sky Science · nl
siRNA-nanodeeltjes gericht op Tudor domein-bevattend eiwit 9 verminderen Pseudomonas aeruginosa-longschade in preklinische modellen door neutrofiel-cuproptose te bevorderen
De eerste verdedigingslinie van het lichaam omvormen tot gerichte bondgenoten
Pneumonie veroorzaakt door de bacterie Pseudomonas aeruginosa is berucht vanwege de moeilijkheid van behandeling, vooral bij mensen met een verzwakt immuunsysteem of beschadigde longen. Deze studie onderzoekt een nieuwe manier om de eigen immuuncellen van het lichaam, neutrofielen genoemd, veiliger en effectiever infecties te laten opruimen. Door kleine stukjes genetisch materiaal in speciaal ontworpen nanodeeltjes af te leveren, programmeren de onderzoekers neutrofielen zodanig dat ze op het juiste tijdstip en de juiste plaats afsterven, waardoor longschade afneemt terwijl de bacteriën alsnog worden bestreden.
Waarom deze bacterie zo moeilijk te verslaan is
Pseudomonas aeruginosa is een zeer aanpasbaar micro-organisme dat veel antibiotica kan weerstaan en beschermende biofilms kan vormen, waardoor longinfecties moeilijk te beheersen zijn. Als reactie roept het lichaam grote aantallen neutrofielen op, witte bloedcellen die als eerste reageren. Hoewel ze essentieel zijn voor het doden van microben, kan een overmaat aan neutrofielen — en hun vertraagde verwijdering uit de longen — averechts werken, met zwelling, vochtophoping en weefselschade tot gevolg. Huidige behandelingen richten zich grotendeels op het direct aanvallen van de bacterie en laten weinig mogelijkheden over om de immuunreactie zelf op een veilige manier bij te sturen.
Een verrassend gen in neutrofielen
Het team begon met het onderzoeken van neutrofielen genomen uit het longvocht van patiënten met pneumonie, en vergeleek die van Pseudomonas-geïnfecteerden met patiënten met andere vormen van pneumonie of zonder pneumonie. Met RNA-sequencing ontdekten ze dat een gen genaamd TDRD9 sterk was aangezet in neutrofielen van Pseudomonas-patiënten. TDRD9 was eerder vooral bekend vanwege rollen in de spermaontwikkeling, niet in longziekten, maar de verhoogde niveaus kwamen consequent naar voren in zowel menselijke monsters als geïnfecteerde muizen. Dit suggereerde dat TDRD9 schadelijk neutrofielgedrag tijdens ernstige bacteriële longinfecties zou kunnen aansturen.
Neutrofielafsterving inzetten voor herstel
Neutrofielen sterven normaal gesproken op gecontroleerde wijze nadat ze hun werk hebben gedaan, waardoor ontsteking kan oplossen. De onderzoekers concentreerden zich op een recent erkende vorm van celdood genaamd cuproptose, die afhankelijk is van koper binnen cellen. In muizen en menselijke neutrofielen geïnfecteerd met Pseudomonas vonden ze dat TDRD9 neutrofielen hielp te beschermen tegen cuproptose, waardoor ze langer leefden in de ontstoken long. Wanneer TDRD9 doelbewust werd verlaagd, raakten neutrofielen vatbaarder voor deze kopergeassocieerde celdood en verbeterde de algehele longschade: er was minder vocht in de longen, minder ontstekingsmoleculen en lagere bacterietellingen. Mechanistische experimenten toonden aan dat TDRD9 werkt via een signaalketen met de eiwitten PD-L1, CD80 en het p38 MAPK-pad, een bekende regelaar van stressreacties binnen cellen.
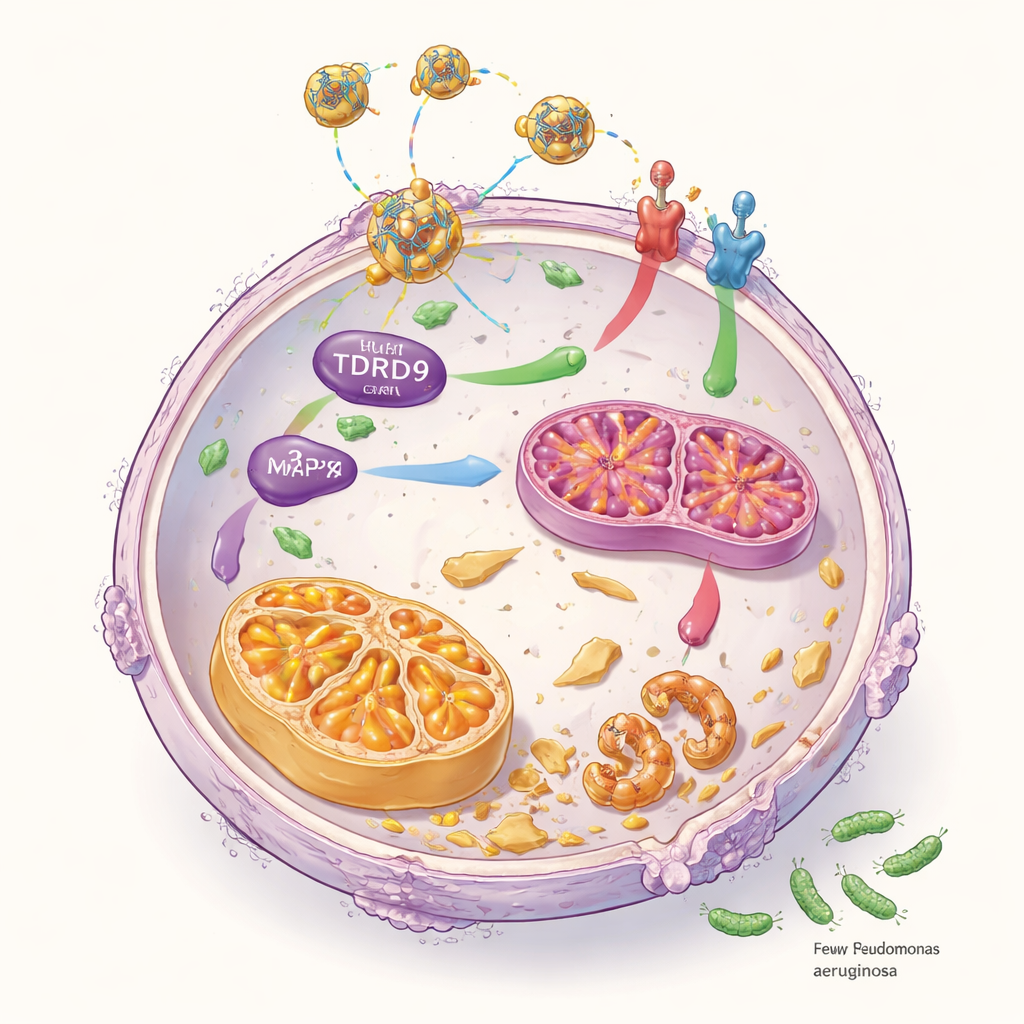
Slimme nanodeeltjes voor gerichte genstillegging
Om deze inzichten tot een potentiële therapie te maken, bouwden de wetenschappers een afleveringssysteem op basis van nanodeeltjes bekleed met hyaluronzuur, een suiker die hen helpt neutrofielen te bereiken via een oppervlaktereceptor genaamd CD44. In elk nanodeeltje zit een small interfering RNA (siRNA) dat specifiek TDRD9 blokkeert. In laboratoriumtesten werden deze deeltjes gemakkelijk opgenomen door menselijke neutrofielen en verlaagden ze efficiënt TDRD9-niveaus. Bij geïnfecteerde muizen verminderde intraveneuze behandeling met de TDRD9-gerichte nanodeeltjes de bacteriële lading, longzwelling en ontstekingssignalen zonder aantoonbare lever- of niertoxiteit. De neutrofielen vertoonden veranderingen die consistent waren met versterkte cuproptose en een rustiger ontstekingsmilieu.
Mensachtige longen naar het lab brengen
Om de kloof tussen diermodellen en menselijke ziekte te overbruggen, kweekte het team ook driedimensionale menselijke longorganoïden — kleine weefselachtige structuren afgeleid van niet-kankergezond longweefsel. Wanneer deze organoïden werden blootgesteld aan Pseudomonas, ontwikkelden ze structurele schade, ontsteking en celdood. Behandeling met TDRD9-gerichte nanodeeltjes remde bacteriële groei, verlaagde ontstekingsmoleculen en verminderde aanwijzingen voor celdood, wat suggereert dat de benadering menselijke longweefsels kan helpen beschermen tegen infectiegedreven schade.
Wat dit voor patiënten zou kunnen betekenen
Al met al laat de studie zien dat het dempen van de TDRD9-route in neutrofielen, met precies afgeleverde siRNA-nanodeeltjes, een gecontroleerde vorm van celdood kan bevorderen die helpt overtollige neutrofielen op te ruimen en longschade bij ernstige Pseudomonas-infecties vermindert. In plaats van alleen maar meer antibiotica in te zetten, stemt deze strategie de immuunrespons zelf fijner af. Hoewel er meer onderzoek nodig is om langetermijnveiligheid en effectiviteit bij mensen te bevestigen, wijzen de bevindingen op een toekomst waarin slimme nanodeeltjes overijverige immuuncellen veranderen van schadebronnen in partners bij genezing.
Bronvermelding: Zhang, W., Li, H., Jia, H. et al. Tudor domain-containing protein 9-targeting siRNA nanoparticles alleviate Pseudomonas aeruginosa lung injury in preclinical models by promoting neutrophil cuproptosis. Nat Commun 17, 2277 (2026). https://doi.org/10.1038/s41467-026-70349-8
Trefwoorden: Pseudomonas aeruginosa pneumonie, neutrofielen, nanodeeltjestherapie, siRNA-afgifte, cuproptose