Clear Sky Science · nl
Beheersing van lysosoomfunctie door het GTPase-activerende eiwit TBC1D9B en zijn bindpartner TMEM55B
Hoe cellulaire recyclingscentra het evenwicht bewaren
In elke cel bevinden zich kleine blaasjeachtige structuren, lysosomen, die fungeren als recyclingscentra en als regelknoppen voor groei. Wanneer ze goed functioneren, worden versleten onderdelen afgebroken en hergebruikt; wanneer ze falen, hopen afvalstoffen zich op en kunnen ziekten ontstaan, waaronder neurodegeneratie en kanker. Deze studie onthult hoe twee weinig bekende eiwitten helpen lysosomen te schakelen tussen een rondzwervende, groeibevorderende toestand en een gecentreerde, afvalverwijderende modus, en werpt licht op hoe cellen zich aanpassen aan overvloed en schaarste.
Recyclingscentra verplaatsen door de cel
Lysosomen liggen niet vast op één plek. Ze reizen langs interne sporen, naar buiten getrokken door een reeks moleculaire motoren en naar binnen getrokken door een andere. Hun plaats in de cel is belangrijk: bij overvloed aan voedingsstoffen verspreiden lysosomen zich naar de buitenste delen van de cel en ondersteunen ze groeisignalen; bij gebrek aan voedsel trekken ze naar het centrum, worden zuurder en verhogen ze de afbraak van celmateriaal. Een klein schakelachtig eiwit genaamd ARL8 staat bekend om lysosomen naar buiten te duwen, maar tot nu toe was er geen specifieke rem geïdentificeerd om dit tegen te gaan. De auteurs vermoedden dat zo’n rem cruciaal zou zijn om cellen snel in een bewaringsmodus te laten overschakelen tijdens verhongering.
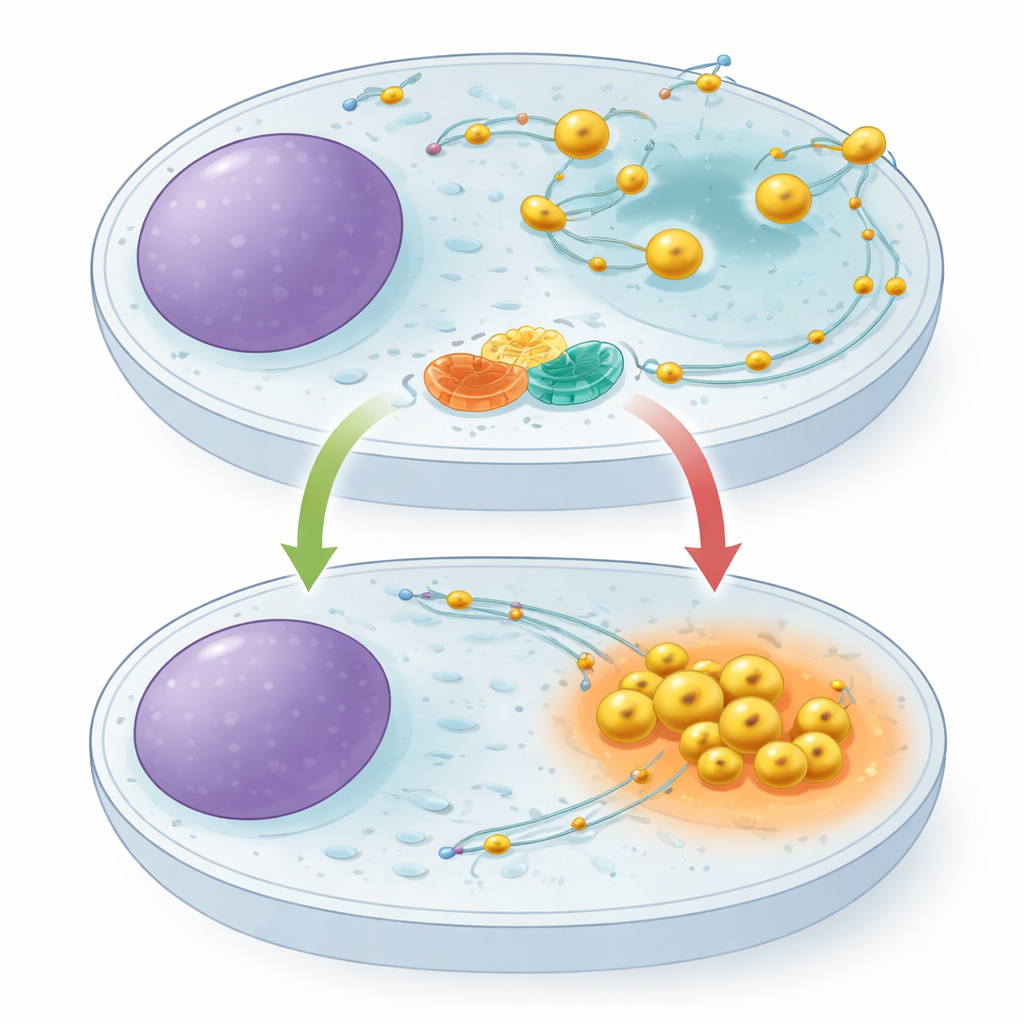
Een moleculair partnerschap aan het lysosoomoppervlak
Met eiwitvismethoden en massaspectrometrie ontdekten de onderzoekers dat een eiwit met de naam TBC1D9B bindt aan een lysosomaal membraaneiwit genaamd TMEM55B. TMEM55B bevindt zich dwars door de buitenste rand van het lysosoom, terwijl TBC1D9B grotendeels oplosbaar is en zich aan het membraan kan vasthechten. Het team toonde aan dat deze twee een direct complex vormen: gezuiverd TBC1D9B hechtte in reageerbuizen aan het blootliggende deel van TMEM55B, en gelabelde versies van de eiwitten trokken elkaar uit celextracten. Zorgvuldige kaartlegging van eiwitsegmenten liet zien dat meerdere regio's van TBC1D9B contact maken met TMEM55B, waardoor TBC1D9B op het lysosoomoppervlak wordt gepositioneerd zonder het deel van het eiwit dat verantwoordelijk is voor zijn katalytische activiteit te blokkeren.
Wanneer de rem faalt, gaan lysosomen uit de bocht
Om te achterhalen wat dit partnerschap doet, verwijderden de auteurs met CRISPR-editing ofwel TMEM55B ofwel TBC1D9B uit menselijke cellen. In beide gevallen clusterden lysosomen niet meer in de buurt van de kern maar verspreidden ze zich naar de celrand en bewogen ze sneller langs hun sporen, wat lijkt op cellen die voortdurend gevoed worden. Herintroductie van normaal TBC1D9B herstelde de juiste positionering, maar een versie zonder katalytische werking deed dat niet, wat aangeeft dat zijn enzymatische activiteit essentieel is. Wanneer de cellen werden uitgehongerd, trokken controlecellen hun lysosomen naar binnen en verhoogden ze hun verteringskracht, zoals bleek uit een toename van belangrijke enzymactiviteiten en verbeterde afbraak van testcargo. Cellen zonder TMEM55B of TBC1D9B deden dit niet: hun lysosomen bleven periferaal en hun afbrekende reactie op verhongering was afgezwakt. Autofagie, het proces waarbij cellen beschadigde componenten zelf verteren, was ook aangetast, met minder efficiënte verwerking van een autofagie‑reporter en ophoping van het adaptereiwit p62.
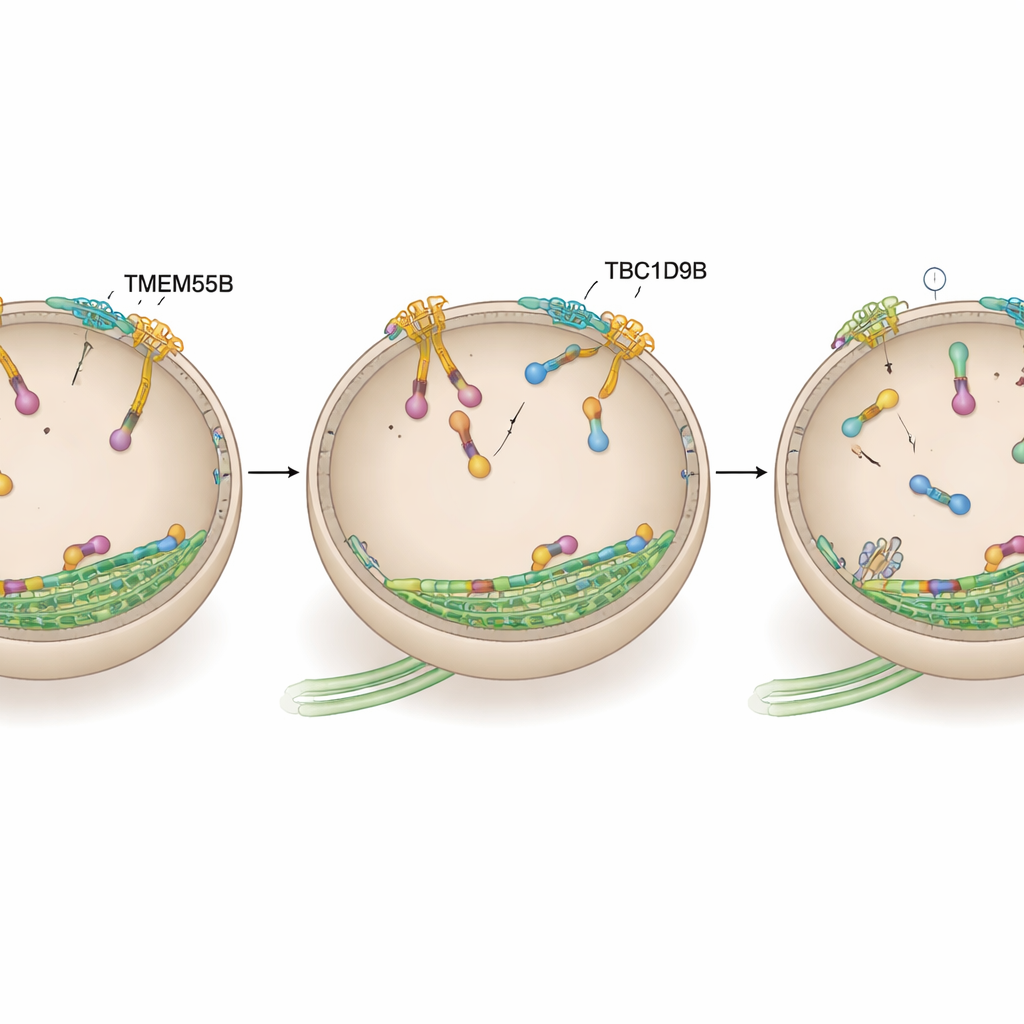
De lysosoommotor uitschakelen
Het team vroeg zich vervolgens af of TBC1D9B zijn effecten uitoefent door direct op ARL8 te werken, de schakelaar die naar buiten stuurt. Met proximiteitslabeling in menselijke neuronen en bindingstests in cellijnen en met gezuiverde eiwitten toonden ze aan dat TBC1D9B selectief bindt aan de actieve, GTP‑geladen vorm van het ARL8B‑variant, maar niet aan de inactieve vorm of aan het nauw verwante ARL8A. Structurele modellering voorspelde dat sleutelresiduen in TBC1D9B contact maken met het GTP‑pocket van ARL8B. In biochemische assays versnelde TBC1D9B de hydrolyse van GTP gebonden aan ARL8B, waardoor het eiwit effectief van de “aan” naar de “uit” staat werd omgezet; een gemuteerde versie van TBC1D9B zonder deze residuen kon dat niet meer. In overeenstemming hiermee toonden cellen zonder TMEM55B of TBC1D9B verhoogde ARL8B‑niveaus op lysosomen, terwijl overexpressie van TBC1D9B lysosomen terug naar het centrum trok, vergelijkbaar met het terugschakelen van ARL8B‑activiteit.
Een nieuwe regelknop voor cellair onderhoud
Ten slotte testten de auteurs of deze ARL8B‑rem de cellulaire veranderingen verklaart die optreden als TBC1D9B ontbreekt. Toen ARL8B werd uitgezet, bleven lysosomen ongeacht de aanwezigheid van TMEM55B of TBC1D9B nabij de kern geclusterd, en werden de defecten in autofagie veroorzaakt door verlies van TBC1D9B grotendeels opgeheven. Gezamenlijk ondersteunen de gegevens een model waarin TMEM55B TBC1D9B naar lysosomen rekruteert, waar het ARL8B inactiveert en lysosomen in staat stelt over te schakelen van een verspreide, groeiondersteunende toestand naar een gecentraliseerde, verteringsgerichte toestand. Voor niet‑specialisten betekent dit dat de studie een belangrijke draaiknop heeft ontdekt die cellen gebruiken om te beslissen wanneer ze agressiever moeten recyclen, een proces met implicaties voor aandoeningen met afvalophoping in de hersenen, stofwisseling en kanker.
Bronvermelding: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
Trefwoorden: lysosomen, autofagie, celsignalering, organeltransport, neurodegeneratie