Clear Sky Science · nl
SLIT3-fragmenten orkestreren neurovasculaire uitbreiding en thermogenese in bruin vetweefsel
Hoe ons lichaam’s “goede vet” ons helpt warm te blijven
Wanneer we de kou ingaan, werkt ons lichaam snel om ons warm te houden. Een belangrijke speler in deze reactie is bruin vet, een speciaal soort vet dat calorieën verbrandt om warmte te produceren. Deze studie onthult hoe bruin vet zijn fijne bloedvaten en zenuwvezels organiseert om warmteproductie te versterken, en legt een verborgen communicatiesysteem bloot dat mogelijk kan worden aangewend om het metabolisme te verbeteren en obesitasgerelateerde aandoeningen te behandelen.
Een verborgen kachel in het lichaam
Bruin vetweefsel functioneert als een interne kachel. In tegenstelling tot wit vet dat energie opslaat, verbruikt bruin vet brandstof om warmte te genereren wanneer we aan lage temperaturen worden blootgesteld. Om dit efficiënt te doen, hebben bruine vetcellen een rijke bloedtoevoer nodig voor zuurstof en voedingsstoffen, en een dicht netwerk van sympathische zenuwen die aangeven wanneer de warmte opgevoerd moet worden. Bij kou breiden deze vaten en zenuwen zich opvallend uit. Tot nu toe was onduidelijk hoe deze verschillende onderdelen van het weefsel hun groei zo nauwkeurig coördineren.
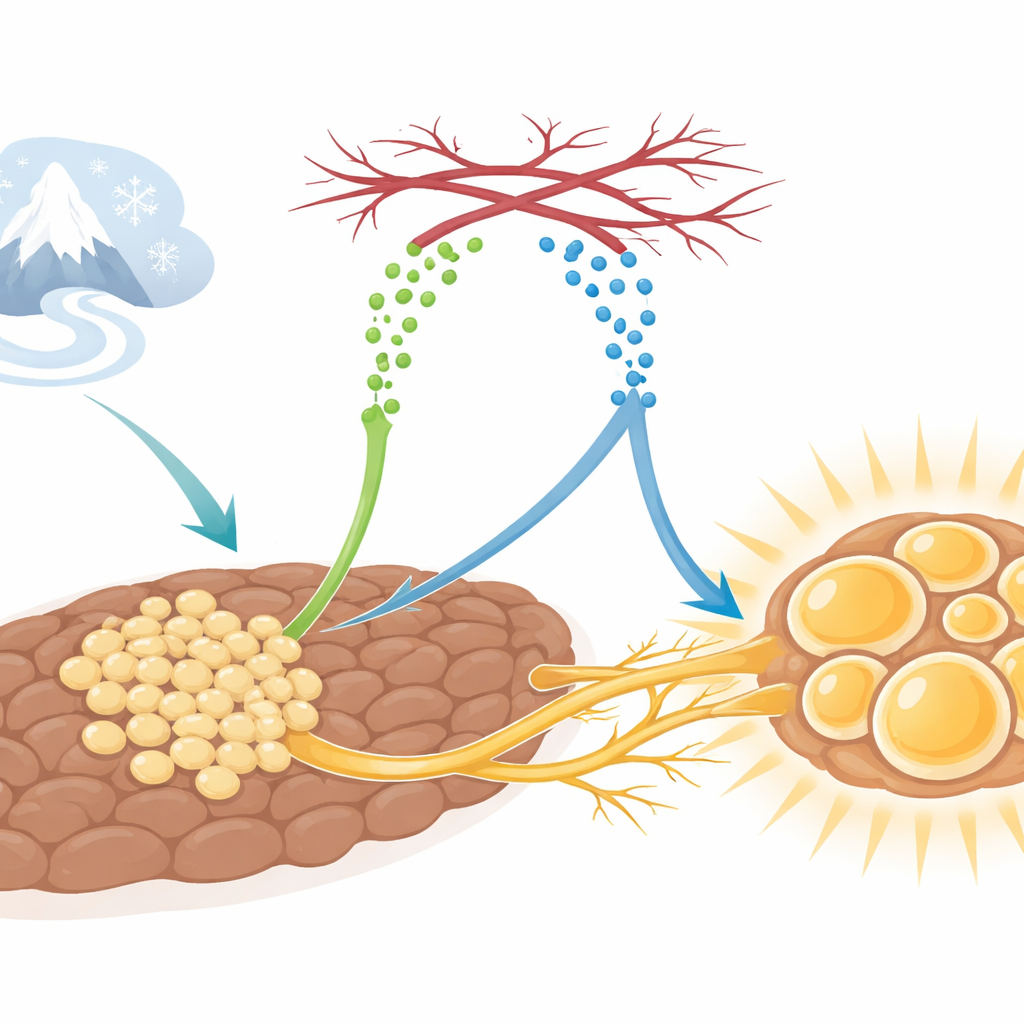
Het boodschappereiwit dat alles in gang zet
De onderzoekers ontdekten dat een eiwit genaamd SLIT3, geproduceerd door onrijpe vetcellen die adipocytprogenitors worden genoemd, centraal staat in deze coördinatie. Bij muizen die aan kou werden blootgesteld, stijgt het SLIT3-gehalte in bruin vet. Wanneer het team SLIT3 specifiek in bruin vet of in deze progenitorcellen blokkeerde, hadden de dieren moeite om hun lichaamstemperatuur in de kou te behouden. Hun bruin vet werd ‘‘witter’’, met grotere vetdruppels, lagere expressie van warmteproducerende genen zoals Ucp1, en verminderde energieverbruik, ondanks onveranderde voedselinname en activiteitsniveaus. Dit duidde op SLIT3 als een belangrijke organisator van de reactie van bruin vet op kou — niet door het basisapparaat binnen elke cel te veranderen, maar door de omliggende weefselomgeving te vormen.
Bloedvaten en zenuwdraden samen opbouwen
Nader onderzoek toonde aan dat bruin vet zonder SLIT3 minder kleine bloedvaten en minder sympathische zenuwvezels had die door het weefsel liepen. Driedimensionale beeldvorming bevestigde dat het zenuwnetwerk duidelijk dunner was. Belangrijk was dat, wanneer het gebruikelijke zenuwsignaal werd omzeild met een medicijn dat bruin vet direct activeert, de cellen normaal reageerden. Dit toonde aan dat SLIT3 niet nodig is voor de vetcellen om brandstof te verbranden, maar wel voor het bouwen van de neurovasculaire ‘‘bekabeling’’ waarmee de hersenen ze aansturen. Het team identificeerde adipocytprogenitors als de belangrijkste lokale bron van SLIT3 en toonde aan dat het verwijderen van SLIT3 alleen in deze cellen al voldoende was om vaatgroei, zenuwgroei en warmtevorming tijdens koude-expositie te verminderen.
Eén eiwit, twee stukken, twee taken
SLIT3 werkt niet als een enkele, statische signaalmolecuul. De onderzoekers lieten zien dat een enzym genaamd BMP1 SLIT3 in twee afzonderlijke fragmenten knipt met verschillende rollen. Het N-terminale fragment (SLIT3-N) stimuleert vooral de groei van haarvaten, werkend via receptoren op endotheelcellen die bloedvaten bekleden. Het C-terminale fragment (SLIT3-C) bevordert primair de uitbreiding van sympathische zenuwen. Ze identificeerden een receptor genaamd PLXNA1 op zenuwvezels als een directe aanhechtingspartner voor SLIT3-C, ondersteund door biochemische bindingsproeven en computergestuurde structurele modellen. Wanneer PLXNA1 werd verminderd, ging het vermogen van SLIT3 of SLIT3-C om zenuwgroei te bevorderen en de temperatuur van bruin vet te verhogen verloren, en daalden zowel de algehele zenuwdichtheid als de noradrenalineniveaus in het weefsel scherp.
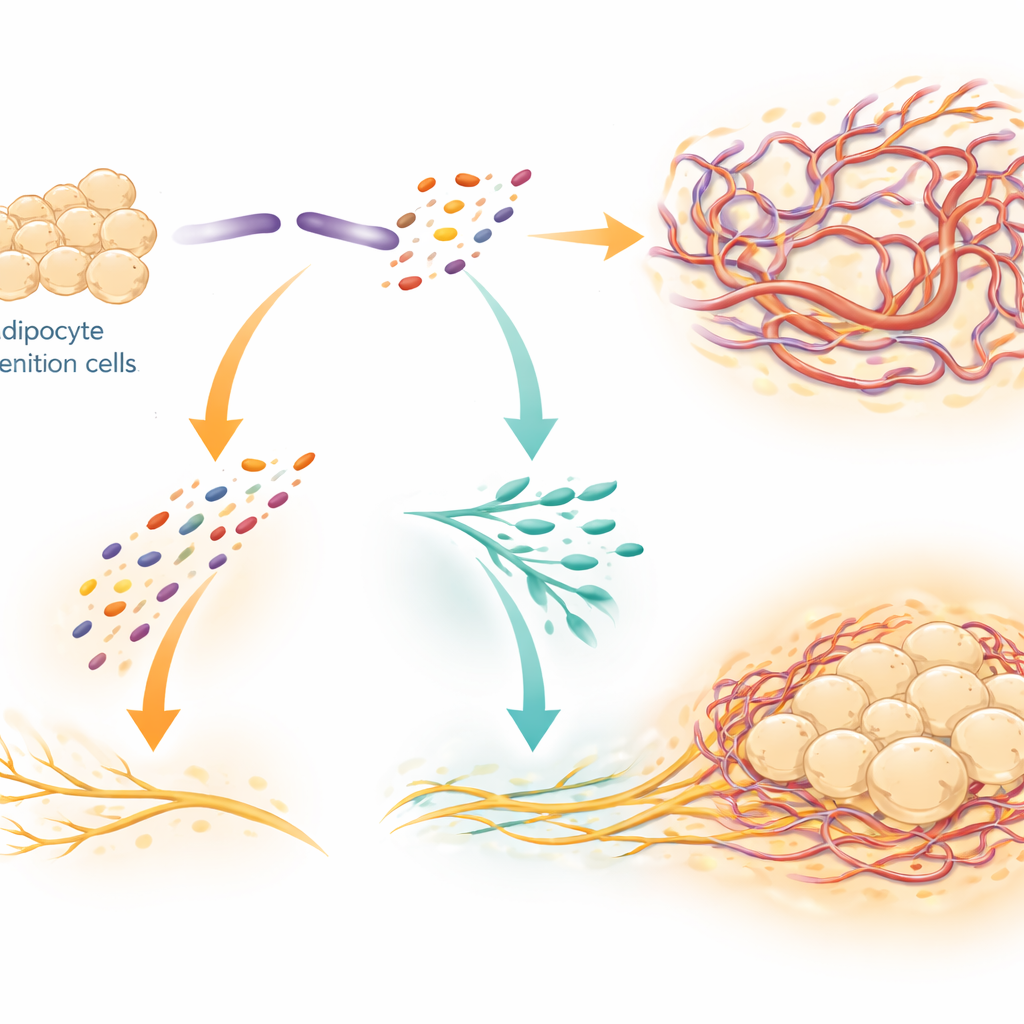
Verbindingen met menselijk metabolisme en gezondheid
Om te onderzoeken of dit systeem ook bij mensen van belang is, analyseerden de auteurs vetmonsters uit grote menselijke obesitascohorten. Hogere SLIT3-expressie in adipose weefsels werd geassocieerd met gezondere profielen: meer van het hormoon adiponectine, minder ontstekingsbevorderende immuuncellen in visceraal vet, betere bloedsuikercontrole en hogere niveaus van het gunstige adipokine omentine. Genetische studies in ander werk hebben ook varianten nabij SLIT3 en zijn receptor PLXNA1 gekoppeld aan obesitas en insulineresistentie. Samen suggereren deze bevindingen dat de SLIT3-route kan bijdragen aan het behoud van gezond vetweefsel en metabole balans bij mensen.
Wat dit betekent voor warm blijven en gezond blijven
Samengevat laat de studie zien dat onrijpe vetcellen in bruin vet meer doen dan alleen volwassen vetcellen vormen; ze vormen actief het ondersteunende netwerk van het weefsel. Door SLIT3 vrij te geven en toe te staan dat het in twee fragmenten wordt gesplitst, stimuleren ze onafhankelijk en toch synchroon de groei van bloedvaten en zenuwen die nodig zijn voor effectieve warmteproductie. Dit fijn afgestemde ‘‘twee-in-één’’ signaleringssysteem zorgt ervoor dat bruin vet snel kan opschalen wanneer de omgeving meer warmte vereist. Op de lange termijn kan begrip van en veilig gebruikmaken van deze route nieuwe wegen openen om energieverbruik te verhogen, de gezondheid van vetweefsel te verbeteren en metabole ziekten te bestrijden.
Bronvermelding: Serdan, T.D.A., Cervantes, H., Frank, B. et al. SLIT3 fragments orchestrate neurovascular expansion and thermogenesis in brown adipose tissue. Nat Commun 17, 2445 (2026). https://doi.org/10.1038/s41467-026-70310-9
Trefwoorden: bruin vetweefsel, thermogenese, neurovasculair herstructureren, SLIT3-signaleringsweg, metabole gezondheid