Clear Sky Science · nl
Activatie van NF-κB in astrocyten belemmert wondgenezing na traumatisch hersenletsel bij mannelijke muizen
Waarom hersenkneuzingen niet altijd netjes genezen
Wanneer iemand een klap op het hoofd krijgt, is de zichtbare verwonding aan de buitenkant slechts een deel van het verhaal. Diep in de hersenen ontvouwt zich een complex herstelproces dat kan bepalen of iemand goed herstelt of blijvende problemen krijgt met denken, stemming of beweging. Deze studie bij mannelijke muizen onthult hoe een belangrijke stresstrap in ondersteunende cellen, astrocyten genoemd, een normaal herstel kan veranderen in een reactie die de schade na traumatisch hersenletsel juist verergert.
De verborgen eerstehulpverleners van de hersenen
Astrocyten zijn stervormige cellen die neuronen en bloedvaten omringen en helpen de interne omgeving van de hersenen stabiel te houden. Na een hoofdtrauma veranderen ze snel van vorm en gedrag, vormen ze een barrière rond het beschadigde gebied en helpen ze weefsel te herbouwen. De onderzoekers richtten zich op een moleculaire schakelaar in deze cellen, NF-κB, die bekendstaat om het regelen van ontsteking in veel weefsels. Ze vroegen zich af of deze schakelaar, na een gesloten hoofdtrauma vergelijkbaar met veelvoorkomende menselijke hersenschuddingen en kneuzingen, de genezing van de hersenen helpt of juist schaadt.
Een stressschakelaar die oplicht na impact
Door genactiviteit in muizenhersenen na letsel te analyseren, vond het team een piek in genen die gekoppeld zijn aan ontsteking en NF-κB-signalisatie, vooral drie tot zeven dagen na het trauma, wanneer secundaire schade toeneemt. Met reporter-muizen lieten ze zien dat NF-κB-activatie zich niet door de hele hersenen verspreidde maar geconcentreerd was rond de inslagplek. Daar was het vooral actief in microglia (de immuunsentinels van de hersenen) en in astrocyten die de rand van de wond vormen. Deze timing en locatie suggereerden dat NF-κB in astrocyten een cruciale regulator kan zijn van hoe de hersenen hun litteken organiseren en de immuunreactie controleren.
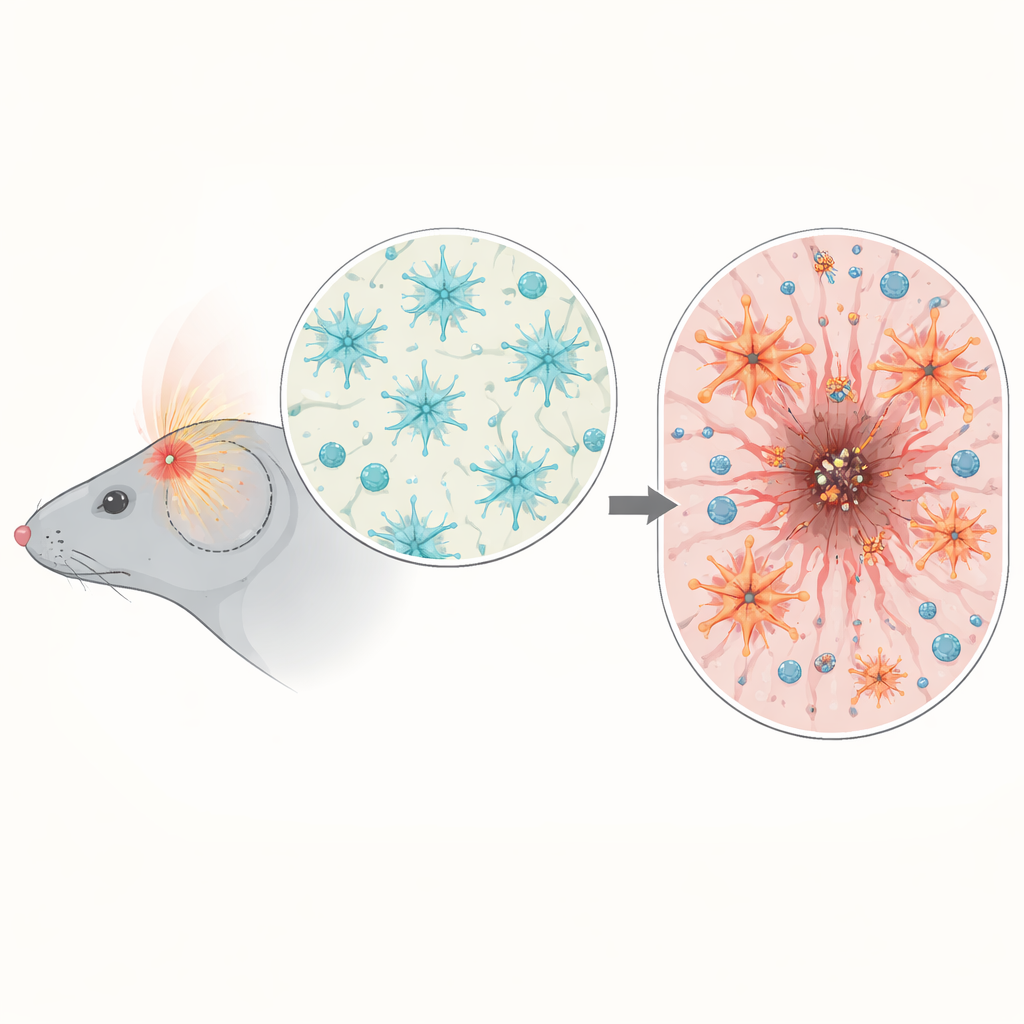
Astrocyten te sterk aangezet
Om oorzaak en gevolg te testen, ontwikkelden de wetenschappers muizen waarbij NF-κB in astrocyten kunstmatig versterkt of verzwakt kon worden, maar pas nadat de hersenontwikkeling voltooid was. Toen deze muizen een hoofdtrauma ondergingen, verloren die met overactief NF-κB in astrocyten meer gewicht, hadden slechtere vroege neurologische scores en toonden grotere, langduriger aanwezige hersenletsels in zowel weefselsecties als MRI-scans. In plaats van een nette, goed afgebakende littekenrand die de beschadigde kern afschermt, produceerden hun astrocyten een dikke, ongeordende grens die de wond in de loop van de tijd niet deed krimpen. De normale balans van ondersteunende matrixeiwitten rond het letsel raakte verstoord, en een belangrijke buitenbarrièrestructuur, het gliale limitans, ontwikkelde zich slecht, waardoor de omliggende hersenen minder beschermd waren.
Wanneer herstelprogramma's ontsporen
Dieper ingaan op de moleculaire details, isoleerde het team astrocyten en nabijgelegen immuuncellen voor gen-voor-gen analyse. Bij gezonde dieren onderdrukt letsel normaal gesproken sommige alledaagse huishoudelijke functies van astrocyten terwijl genen worden aangezet die wondsluiting en regeneratie ondersteunen. In tegenstelling daarmee zagen astrocyten met chronisch actief NF-κB er al "gewond" uit zelfs vóór het trauma, en na impact slaagden ze er niet in om gunstige herstelprogramma's volledig in te schakelen, zoals die geassocieerd met een gecontroleerde transformatie die cellen helpt een effectieve grens te vormen. In plaats daarvan gaven ze sterk de voorkeur aan ontstekingsgenen, namen kenmerken aan van een toxische astrocyttoestand die is gekoppeld aan veroudering en neurodegeneratieve ziekten, en toonden ze tekenen van een "senescentie-achtige" secretorische profiel die geassocieerd wordt met chronische, niet-oplossende wonden.
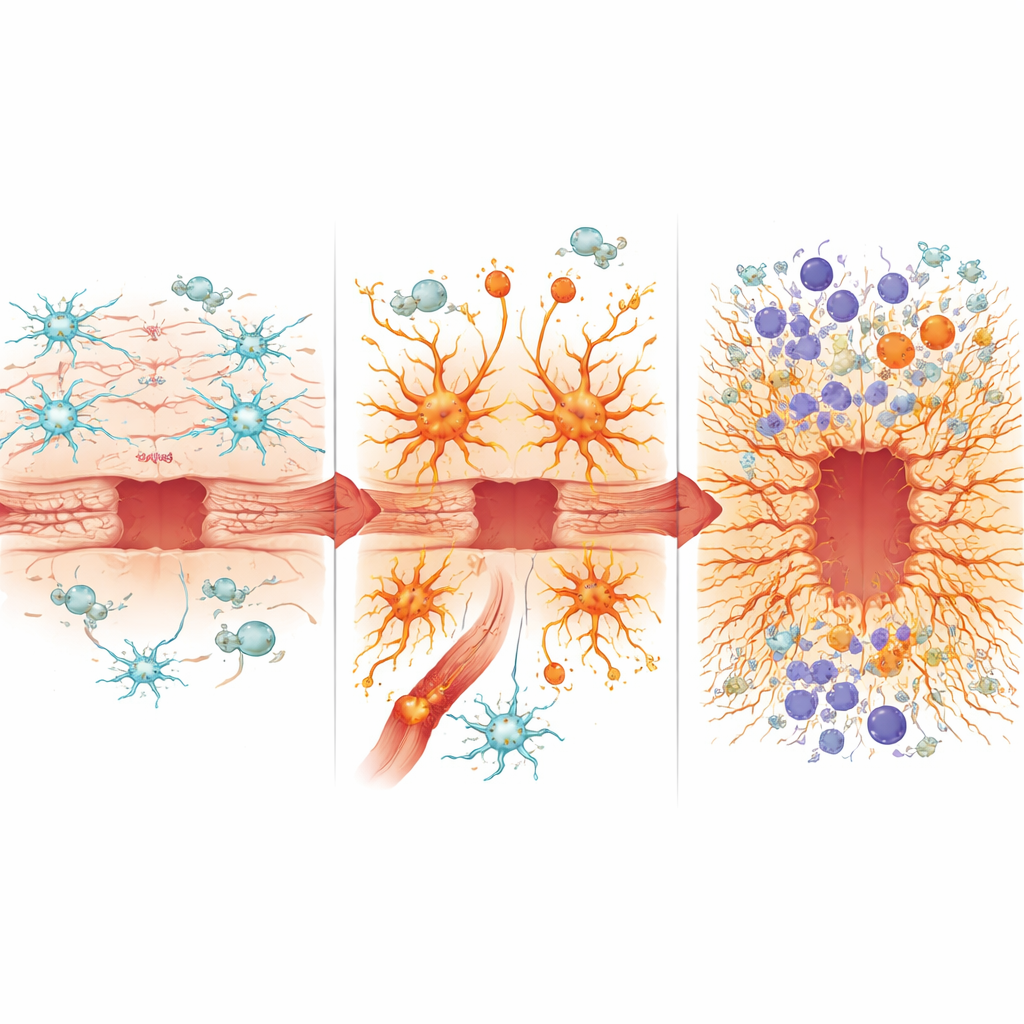
Het aanwakkeren van het immuuvuur
Deze verkeerd geprogrammeerde astrocyten veranderden ook het immuunlandschap van de hersenen. De bloed-hersenbarrière werd lekkerder, waardoor meer perifere immuuncellen binnenkwamen. Muizen met overactief NF-κB in astrocyten vertoonden zwaardere infiltratie van ontstekingsbevorderende myeloïde cellen en veranderde samenstellingen van neutrofielen, monocyten en dendritische cellen, evenals verhoogde aantallen cytotoxische T-cellen die het weefsel verder kunnen beschadigen. Immuuncellen in deze omgeving vertoonden sterkere signalen gedreven door interferon- en inflammasoomroutes, beide geassocieerd met agressieve, potentieel neurotoxische ontsteking. Tegelijkertijd waren de niveaus van verschillende beschermende of pro-herstel eiwitten, zoals osteopontine, verlaagd, terwijl andere gerelateerd aan oxidatieve stress, ijzerstapeling en littekenvorming, waaronder heemoxygenase-1 en lipocaline-2, verhoogd waren. De verhouding tussen osteopontine en lipocaline-2 kwam naar voren als een eenvoudige marker die samenhing met beter of slechter herstel bij de verschillende muizenstammen.
Wat dit betekent voor herstel na hoofdtrauma
Gezamenlijk tonen de bevindingen aan dat wanneer de NF-κB-stresstrap in astrocyten chronisch verhoogd is, deze cellen verschuiven van het ondersteunen van georganiseerd herstel naar het veroorzaken van chaotische littekenvorming en langdurige ontsteking. In plaats van een schone grens te bouwen die de schade beperkt en weefselremodellering mogelijk maakt, helpen ze een lekkende, ontstekingsrijke nis te creëren die het letsel vergroot en de lange termijnuitkomst schaadt. Hoewel het werk is uitgevoerd bij mannelijke muizen, wijst het op astrocyt-NF-κB als een veelbelovend doelwit voor therapieën die gericht zijn op het verbeteren van herstel na traumatisch hersenletsel en suggereert het dat bloedspiegels van moleculen zoals osteopontine en lipocaline-2 mogelijk ooit clinici kunnen helpen bij het volgen van hoe goed iemands hersenen genezen.
Bronvermelding: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
Trefwoorden: traumatisch hersenletsel, astrocyten, neuroinflammatie, vorming van hersennaad, NF-kappa B