Clear Sky Science · nl
NAA40 en NAC werken samen bij cotranslationele histonacetylatie in mensen
Hoe cellen hun genetische schakelaars fijnafstellen
In elke menselijke cel worden nieuwgevormde eiwitten chemisch aangepast terwijl ze uit de eiwitmakerige machines van de cel, de ribosomen, tevoorschijn komen. Deze kleine aanpassingen bepalen waar een eiwit naartoe gaat, hoe lang het blijft bestaan en zelfs hoe onze genen aan- of uitgezet worden. Dit artikel richt zich op een zeer specifiek eiwit, NAA40, en een hulpcomplex genaamd NAC, en onthult hoe zij samen op het ribosoom werken om histoneiwitten te modificeren—de spoelen waar DNA omheen is gewikkeld—en daarmee genactiviteit en mogelijk kankervorming beïnvloeden.
Een klein kapje dat het gedrag van histonen verandert
Veel menselijke eiwitten krijgen een kleine chemische kap aan hun beginzijde, een proces dat N-terminale acetylatie wordt genoemd. Histonen H2A en H4, die helpen DNA in chromatine te verpakken, zijn vrijwel altijd op deze manier gekapt. NAA40 is ongewoon onder enzymen omdat het zich bijna exclusief specialiseert in het toevoegen van deze kap aan juist deze histonen terwijl ze worden geproduceerd. Deze acetylatie concurreert met andere chemische labels zoals fosforylering en methylatie op hetzelfde histongebied, zodat de activiteit van NAA40 kan verschuiven hoe strak DNA is verpakt en hoe genen worden gereguleerd. Belangrijk is dat veranderde niveaus van NAA40 in verband zijn gebracht met verschillende vormen van kanker, waardoor het een beloftevolle doelwit voor nieuwe therapieën vormt.
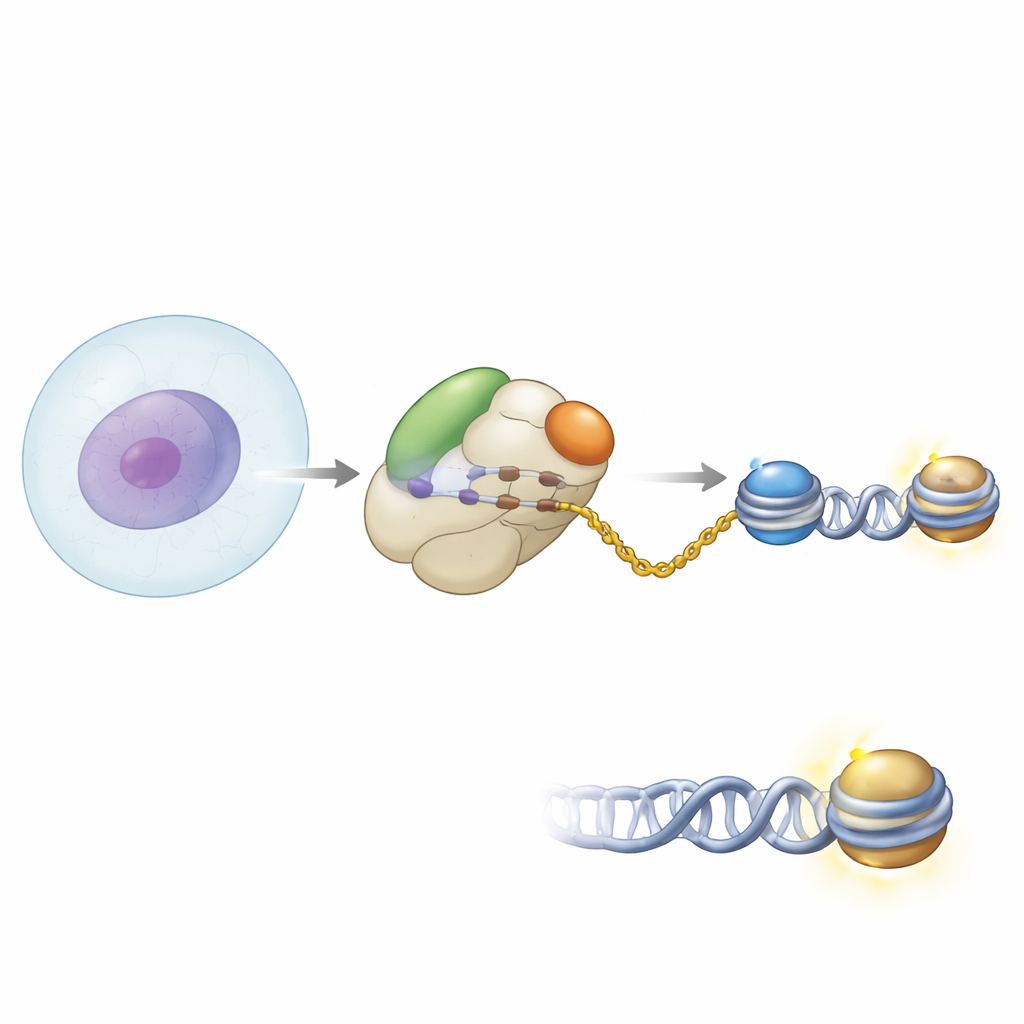
Samenwerking bij de poort van de eiwitfabriek
De auteurs gebruikten biochemische methoden en hogeresolutie cryo-elektronenmicroscopie om te zien hoe NAA40 op het menselijke ribosoom gepositioneerd is. Ze vonden dat NAA40 precies bij de uitgang van de tunnel zit waar pasgevormde polypeptideketens naar buiten komen. Daar werkt het niet alleen: het bindt naast het nascent polypeptide–associated complex, of NAC, een veelvoorkomende ribosoomgebonden helper die over nieuwe eiwitten waakt tijdens hun verschijning. Structurele momentopnames toonden dat NAA40 aan het ribosoom verankerd is door een unieke positief geladen helix-segment aan zijn eigen begin, terwijl NAC via een van zijn subunits aan het ribosoomoppervlak vastzit. Een flexibele domein van NAC reikt over om contact te maken met NAA40 en vormt zo feitelijk een brug tussen het enzym en het ribosoom.
Waarom NAC nodig is voor histoonafstemming
Om te testen hoe belangrijk deze samenwerking is, reconstrueerden de onderzoekers deze interacties met gezuiverde componenten in reageerbuizen. Ze observeerden dat NAA40 alleen slechts zwak aan ribosomen bindt, maar wanneer NAC aanwezig is, wordt die ribosoombinding veel sterker. Als ze een specifiek “UBA”-gebied van NAC verwijderden dat NAA40 raakt, verdween deze versterkte binding. In menselijke cellen leidde uitputting van NAC tot verminderde NAA40-afhankelijke acetylatie van histon H4 en een overeenkomstige stijging van een concurrerend fosforyleringsmerkje op dezelfde histoontail. Deze verandering trad op zonder dat de hoeveelheid of locatie van NAA40 zelf veranderde, wat aangeeft dat de belangrijkste rol van NAC is om NAA40 correct naar vertalende ribosomen te rekruteren en te positioneren zodat histonen efficiënt kunnen worden gemodificeerd zodra ze worden gemaakt.
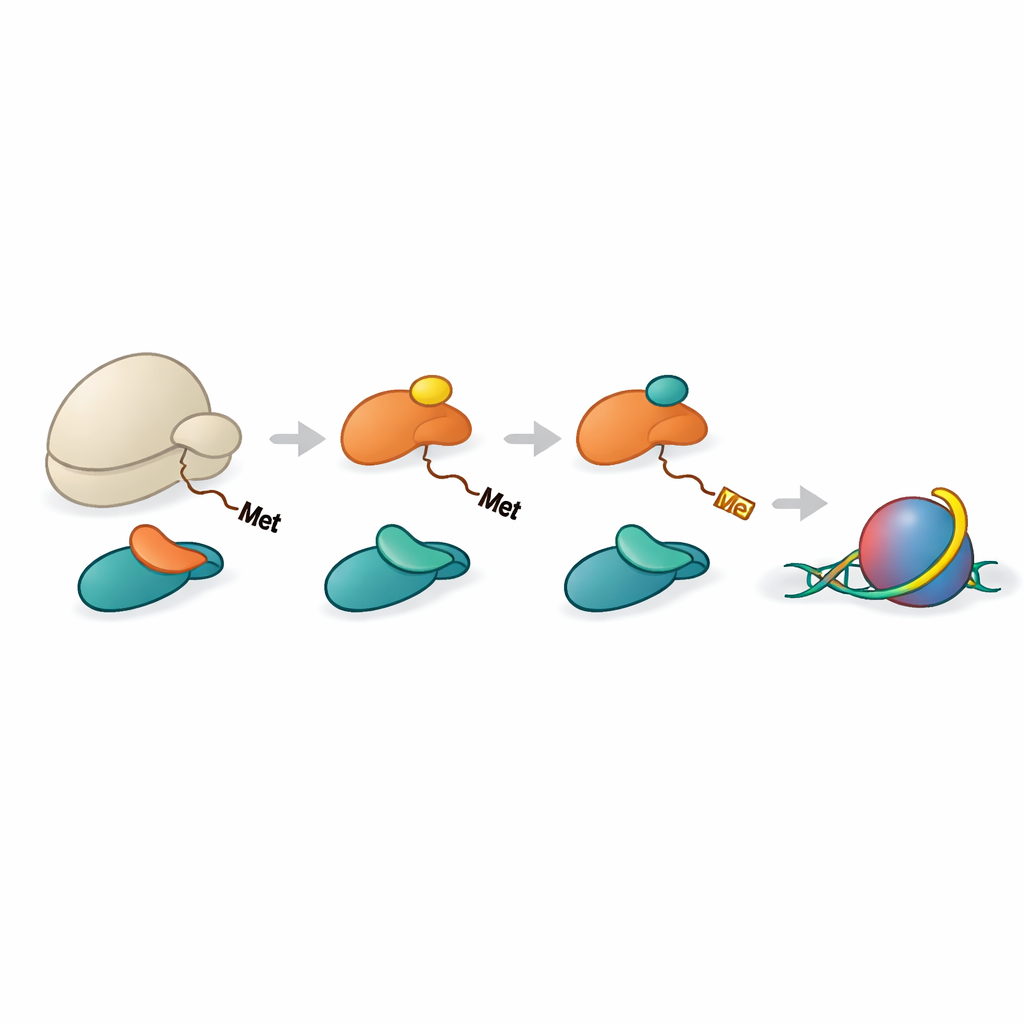
Een gecoördineerde productielijn voor histoonverwerking
Histonen H2A en H4 moeten eerst hun initiële methionine-aminozuur verliezen voordat NAA40 ze kan herkennen. Een ander enzym, METAP1, voert deze trimming uit. Het team toonde aan dat NAC kan helpen METAP1 en NAA40 samen met het ribosoom te brengen, waardoor een multi-enzymcomplex bij de peptidetunneluitgang ontstaat. Hogeresolutiestructuren van gereconstrueerde complexen toonden METAP1 en NAA40 zij-aan-zij gebonden aan het ribosoom, met hun actieve centra op vrijwel gelijke afstanden van de uitgangstunnel. Deze geometrie betekent dat, zodra een histoontail net een dozijn of zo aminozuren buiten het ribosoom uitsteekt, METAP1 het start-methionine kan verwijderen en NAA40 onmiddellijk de acetylkap kan toevoegen, waardoor elke vertraging tussen de twee stappen wordt geminimaliseerd.
Gevolgen voor gencontrole en kanker
Samengevat laat de studie zien dat NAA40 niet simpelweg door de cel zwemt op zoek naar histonen om te modificeren. In plaats daarvan wordt het door NAC aan het ribosoom gedockt en maakt het deel uit van een geordend verwerkingsstation dat histonen voorbereidt op het moment dat ze worden gesynthetiseerd. Door het verlies van methionine en het toevoegen van acetyl strak te koppelen, zorgt de cel ervoor dat histon H2A, H4 en de aan DNA-schade gebonden variant H2A.X snel een acetylmerk krijgen dat chromatinestructuur en genexpressie kan vormen. Omdat verstoringen in deze vroege histoonmarkering stap kankerverwekkende groei kunnen bevorderen, biedt inzicht in de precieze ordening van NAA40, NAC en METAP1 op het ribosoom een structurele blauwdruk die het ontwerp van medicijnen kan sturen die gericht zijn op het fijnregelen van dit cruciale epigenetische controlepunt.
Bronvermelding: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Trefwoorden: histonacetylatie, NAA40, ribosoom, nascent polypeptide-associated complex, epigenetische regeling